Furosemide Vitabalans Annex I_II_ro
|
|
|
- Ernest Albu
- 4 ani în urmă
- Vzualizari:
Transcriere
1 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1
2 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma farmaceutică Mod de administrare Republica Cehă Danemarca Estonia Finlanda Ungaria Letonia Lituania Norvegia Polonia Furosemide Vitabalans 40 mg tablety 40 mg tableta Orală Furosemid Vitabalans 40 mg tableta Orală Furosemide Vitabalans 40 mg tabletes 40 mg tableta Orală Republica Furosemid Vitabalans mg tableta Orală 2
3 Slovacă Slovenia Suedia mg tablety Furosemid Vitabalans 40 mg tablete 40 mg tableta Orală 3
4 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4
5 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi denumirile asociate (vezi Anexa I) Furosemida este un diuretic de ansă care acţionează de-a lungul întregului nefron, cu excepţia tubului contort distal. Furosemida este autorizată în Uniunea Europeană (UE) de peste 40 de ani. Cererea de autorizaţie de introducere pe piaţă prin procedura descentralizată pentru Furosemide Vitabalans a fost depusă în conformitate cu articolul 10a din Directiva 2001/83/CE, aceasta fiind o cerere pentru utilizare bine stabilită. Prin urmare, cererea pentru Furosemide Vitabalans se bazează pe date bibliografice publice, deoarece este posibilă înlocuirea rezultatelor testelor preclinice şi ale studiilor clinice cu trimiteri detaliate la literatura ştiinţifică publicată (informaţii disponibile în domeniul public) în cazul în care se poate demonstra că substanţele active ale medicamentului sunt în uz medical bine stabilit în Comunitate de cel puţin zece ani şi prezintă o eficacitate recunoscută şi un nivel acceptabil de siguranţă. Furosemida se utilizează la scară largă în practica clinică, iar în cursul procedurii descentralizate o serie de lucrări publicate au fost prezentate pentru a-i susţine eficacitatea şi siguranţa. Prezentarea generală nonclinică a făcut trimitere la 29 de publicaţii, apărute până în anul 2010, care descriu studii farmacodinamice, de farmacologie generală, farmacocinetice şi toxicologice. Partea clinică a dosarului a făcut trimitere la 77 de publicaţii, apărute până în anul 2009, care susţin efectul furosemidei în tratamentul edemului asociat cu insuficienţa cardiacă congestivă, al cirozei hepatice şi al insuficienţei renale, inclusiv al sindromului nefrotic şi al hipertensiunii arteriale uşoare până la moderate. Partea II punctul 1 litera d) din anexa I la Directiva 2001/83/CE prevede că rapoartele nonclinice şi/sau clinice trebuie să explice relevanţa datelor prezentate cu privire la un produs diferit de produsul prevăzut pentru introducerea pe piaţă. Trebuie să se stabilească dacă produsul studiat poate fi considerat ca fiind similar cu produsul pentru care se va acorda autorizaţia de introducere pe piaţă, în ciuda diferenţelor existente. În cursul procedurii descentralizate, Polonia şi Lituania au considerat că datele bibliografice privind farmacocinetica furosemidei, prezentate în dosarul pentru autorizaţia de introducere pe piaţă, nu pot fi aplicate pentru Furosemide Vitabalans şi trebuie considerate ca fiind insuficiente. Lipsa datelor privind biodisponibilitatea produsului ar putea conduce la modificări neprevăzute în răspunsul farmacodinamic şi la eşec terapeutic, precum şi la apariţia unor efecte toxice. Procedura descentralizată a fost încheiată în ziua 210, majoritatea statelor membre interesate fiind de acord cu concluziile raportului de evaluare al statului membru de referinţă, cu excepţia Poloniei şi a Lituaniei, care au invocat un risc major potenţial pentru sănătatea publică. Prin urmare, la nivelul CMD(h) a fost iniţiată o sesizare, iar solicitantului i s-a cerut să prezinte justificări privind faptul că literatura de specialitate furnizată în susţinerea cererii sale era aplicabilă produsului pentru care se depusese cererea şi să demonstreze că expunerea potenţial mai redusă sau mai ridicată la furosemidă când este utilizat Furosemide Vitabalans în comparaţie cu expunerea obţinută ca urmare a administrării produsului utilizat în studiile clinice pivot descrise în literatura de specialitate prezentată, nu ar influenţa eficacitatea sau siguranţa. Motivul serios de îngrijorare invocat de Polonia şi de Lituania nu a putut fi soluţionat în cursul sesizării CMD(h) şi, prin urmare, a fost sesizat CHMP. Pentru a demonstra relevanţa datelor bibliografice utilizate în susţinerea cererii pentru Furosemide Vitabalans, solicitantul a făcut trimitere la: 5
6 Date farmaceutice Argumentul solicitantului privind faptul că metodele tradiţionale de fabricaţie, precum şi excipienţii utilizaţi la scară largă în formulele comprimatelor nu ar provoca o expunere potenţial mai redusă sau mai ridicată la furosemidă când este utilizat Furosemide Vitabalans (în comparaţie cu expunerea obţinută în urma administrării altor comprimate care conţin furosemidă 40 mg) nu poate fi considerat o dovadă suficientă pentru a face legătura între produsul pentru care s-a depus cererea şi alte produse care conţin furosemidă descrise în literatura de specialitate. În plus, solicitantul a furnizat un set de profiluri de dizolvare care compară Furosemide Vitabalans cu alte nouă comprimate care conţin furosemidă 40 mg. CHMP a considerat că rezultatele acestui studiu, care arată că Furosemide Vitabalans prezintă un profil de dizolvare similar cu al celorlalte produse care conţin furosemidă prezentate, nu au fost suficiente pentru a demonstra eficacitatea şi siguranţa produsului pentru care s- a depus cererea. Într-adevăr, furosemida este o substanţă activă cu solubilitate redusă şi permeabilitate redusă (clasa IV SCB), ceea ce nu susţine o extrapolare bazată pe date farmaceutice. Ar fi necesare date suplimentare pentru a susţine relevanţa datelor bibliografice şi pentru a demonstra siguranţa şi eficacitatea Furosemide Vitabalans. În plus, datele in vitro nu pot fi singura dovadă a faptului că datele clinice din studiile prezentate sunt aplicabile pentru Furosemide Vitabalans. Date farmacocinetice În răspunsul către CHMP, solicitantul a făcut trimiteri suplimentare la datele farmacocinetice publicate care prezintă parametrii farmacocinetici ai unor formule de comprimate similare cu Furosemide Vitabalans, precum şi formule diferite (de exemplu, comprimat de 20 mg). Rezultatele au arătat că absorbţia furosemidei este foarte variabilă (valoarea ASC variază de la 793,8 la ng*h/ml, valoarea C max de la 283,6 la ng/ml, şi anume o diferenţă de aproape zece ori pentru valorile C max ). CHMP a considerat că un interval larg de valori farmacocinetice pentru diferite produse care conţin furosemidă 40 mg nu dovedeşte că parametrii farmacocinetici pentru Furosemide Vitabalans se vor situa în acelaşi interval. Parametrii farmacocinetici disponibili în literatura de specialitate nu sunt suficienţi pentru a afirma că Furosemide Vitabalans ar avea o biodisponibilitate similară. În plus, dat fiind faptul că furosemida este un compus foarte variabil, a fost considerată necesară prezentarea datelor in vivo pentru a caracteriza farmacocinetica produsului, împreună cu justificarea care ar permite stabilirea unei legături cu datele publicate. Date clinice Pentru a susţine eficacitatea şi siguranţa Furosemide Vitabalans, solicitantul a făcut trimitere doar la studii publicate. Studiul pentru susţinerea siguranţei furosemidei (Dormans et al. 1 ) prezentat de solicitant nu a fost considerat relevant de către CHMP, deoarece furosemida din acest studiu a fost administrată intravenos, iar Furosemide Vitabalans este destinat administrării orale sub forma unui comprimat de 40 mg. Argumentele solicitantului, care a afirmat că nu există nicio corelare între cantitatea de furosemidă absorbită şi diureză şi că formulele cu eliberare controlată şi cele cu eliberare imediată produc aproape aceeaşi diureză, nu au fost considerate suficiente pentru a dovedi eficacitatea Furosemide Vitabalans. Prin urmare, datele din literatura de specialitate prezentate de solicitant în susţinerea siguranţei şi a eficacităţii furosemidei nu au furnizat dovezi suficiente ale faptului că parametrii farmacocinetici ai Furosemide Vitabalans permit utilizarea sa în condiţii de siguranţă şi eficacitate la acelaşi dozaj şi pentru aceleaşi indicaţii pentru care s-a depus cererea. 1 Dormans et al. Diuretic efficacy of high dose furosemide pharmacokinetics and pharmacodynamics in health and disease - an update (Eficacitatea diuretică a farmacocineticii şi farmacodinamicii dozei ridicate de furosemidă - o actualizare). J Pharmacokineti Biopharm, 1989 Feb;17(1):1-46 6
7 Concluzie generală Pe baza datelor bibliografice prezentate, analizate împreună cu datele farmaceutice, solicitantul nu a reuşit să stabilească relevanţa acestor date pentru a demonstra siguranţa şi eficacitatea pentru Furosemide Vitabalans. Procedura de reexaminare În urma adoptării avizului şi recomandărilor de către CHMP în timpul reuniunii CHMP din luna octombrie 2012, a fost primită o solicitare de reexaminare de la solicitantul la 12 noiembrie Motivele detaliate pentru reexaminare au fost prezentate la 21 decembrie La cererea solicitantului, a fost convocată o reuniune ad-hoc a experţilor la 13 februarie Motivele detaliate pentru reexaminare, prezentate de solicitant Solicitantul şi-a exprimat dezacordul privind unele aspecte procedurale ale procedurii recunoaşterii reciproce, ale procedurii CMD(h) şi ale procedurii de sesizare în temeiul articolului 29 alineatul (4) din Directiva 2001/83/CE. Cu toate acestea, s-a reţinut faptul că CHMP este un comitet ştiinţific şi că, atâta timp cât acesta funcţionează în cadrul legal, nu poate discuta calităţile specifice ale aspectelor procedurale şi juridice ale procedurilor administrative prevăzute în legislaţie. Astfel, consideraţiile de natură procedurală şi juridică nu intră în atribuţiile CHMP şi, prin urmare, reexaminarea procedurii de sesizare în temeiul articolului 29 alineatul (4) din Directiva 2001/83/CE s-a concentrat doar asupra punctelor cu caracter ştiinţific care au fost abordate în motivele pentru reexaminare. Solicitantul şi-a exprimat dezacordul faţă de avizul CHMP, concentrându-şi motivele ştiinţifice asupra următoarelor puncte, pentru care solicitantul a argumentat că nu fuseseră prezentate justificări sau dovezi clare care să explice: modul în care produsul care conţine furosemidă 40 mg, pentru care s-a depus cererea, ar constitui un risc major potenţial pentru sănătatea publică motivul pentru care siguranţa şi eficacitatea produsului care conţine furosemidă 40 mg, pentru care s-a depus cererea, ar fi foarte diferite faţă de alte produse care conţin furosemidă 40 mg motivul pentru care parametrii farmacocinetici ai produsului care conţine furosemidă 40 mg, pentru care s-a depus cererea, ar fi diferiţi de parametrii farmacocinetici ai altor produse care conţin furosemidă, care au fost descrişi în literatura de specialitate, şi modul în care această diferenţă ar putea constitui un risc major potenţial concret pentru sănătatea publică. Concluzia CHMP privind motivele pentru reexaminare După cum s-a menţionat anterior, anexa I la Directiva 2001/83/CE prevede că rapoartele nonclinice şi/sau clinice trebuie să explice relevanţa datelor prezentate cu privire la un produs diferit de produsul prevăzut pentru introducerea pe piaţă. Trebuie să se stabilească dacă produsul studiat poate fi considerat ca fiind similar cu produsele pentru care se va acorda autorizaţia de introducere pe piaţă, în ciuda diferenelor existente. A fost considerată necesară o abordare ştiinţifică acceptată, cum ar fi demonstrarea unor farmacocinetici comparabile, pentru a stabili legătura între Furosemide Vitabalans şi un produs similar. În plus, s-a mai reţinut că, în conformitate cu Ghidul privind definirea unui risc major potenţial pentru sănătatea publică, se poate considera că există un risc major potenţial pentru sănătatea publică asociat unui anumit medicament dacă datele prezentate în susţinerea eficacităţii terapeutice nu furnizează o 7
8 justificare solidă a afirmaţiilor privind eficacitatea şi/sau dacă datele privind siguranţa clinică nu asigură o susţinere adecvată a concluziei că toate aspectele potenţiale de siguranţă au fost analizate în mod corect şi adecvat. În opinia CHMP, solicitantul nu a demonstrat în mod adecvat că literatura de specialitate prezentată privind furosemida se aplică direct la Furosemide Vitabalans. Argumentul solicitantului privind faptul că metodele tradiţionale de fabricaţie, precum şi excipienţii utilizaţi la scară largă sunt dovezi suficiente pentru a demonstra legătura între Furosemide Vitabalans şi alte produse care conţin furosemidă nu poate fi acceptat. Se aprobă faptul că metoda de fabricaţie este descrisă în mod adecvat; totuşi, un proces de fabricaţie robust reprezintă doar baza pentru investigaţii suplimentare privind eficacitatea şi siguranţa produsului pentru care s-a depus cererea şi nu poate fi acceptat ca dovadă a echivalenţei cu un produs autorizat. De asemenea, solicitantul a argumentat că profilul de dizolvare împreună cu echivalenţa farmaceutică evidentă demonstrează legătura între Furosemide Vitabalans şi alte produse autorizate care conţin furosemidă 40 mg. După cum s-a discutat anterior, datele in vitro care demonstrează similitudinea profilurilor de dizolvare dintre Furosemide Vitabalans şi alte produse care conţin furosemidă nu dovedesc că biodisponibilitatea acestor produse ar fi similară, în special în cazul unei substanţe farmaceutice de clasă IV SCB (solubilitate redusă, permeabilitate redusă). Nu este posibil să se concluzioneze că parametrii farmacocinetici pentru Furosemide Vitabalans se vor situa în acelaşi interval cu cei ai altor comprimate de furosemidă 40 mg la care se face trimitere, doar pe baza datelor din literatura de specialitate publicată. Nu poate fi exclusă posibilitatea ca biodisponibilitatea produsului pentru care s-a depus cererea să fie mai redusă sau mai ridicată decât biodisponibilitatea acestor produse. Prin urmare, nu se poate concluziona că eficacitatea şi siguranţa pentru Furosemide Vitabalans vor fi similare cu eficacitatea şi siguranţa produselor care conţin furosemidă din literatura de specialitate prezentată. În plus, în cazul medicamentelor cu variabilitate ridicată, astfel cum este produsul pentru care s-a depus cererea, se consideră necesar să se investigheze comportamentul farmacocinetic pentru excluderea oricărei alte variaţii potenţiale asociate produsului. Într-adevăr, nu se poate exclude faptul că formula produsului pentru care s-a depus cererea ar putea avea un comportament diferit din punct de vedere farmacocinetic, în comparaţie cu produsele care conţin furosemidă din literatura de specialitate prezentată. Dosarul prezentat de solicitant nu a inclus niciun fel de date clinice in vivo care ar fi putut să demonstreze că profilul farmacocinetic pentru Furosemide Vitabalans este similar cu cel al produselor care conţin furosemidă din literatura de specialitate prezentată. În opinia CHMP, pentru a afirma aceeaşi indicaţie, ar fi trebuit demonstrată comparabilitatea biodisponibilităţii dintre produsul pentru care s-a depus cererea şi un produs din literatura de specialitate prezentată. Prin urmare, CHMP a concluzionat că eficacitatea Furosemide Vitabalans nu a fost demonstrată pentru indicaţiile pentru care s-a depus cererea şi acest fapt constituie un risc major potenţial pentru sănătatea publică. Reuniunea ad-hoc a experţilor La cererea solicitantului, a fost convocată o reuniune ad-hoc. Grupul de experţi ad-hoc a considerat că literatura de specialitate publicată şi datele privind dizolvarea furnizate de solicitant nu erau suficiente pentru a demonstra siguranţa şi eficacitatea pentru Furosemide Vitabalans. Grupul a considerat că metodele de fabricaţie sau datele privind dizolvarea nu puteau să prevadă modul în care produsul se va comporta in vivo. S-a considerat că sunt necesare date in vivo mai ales în cazul unui medicament care prezintă un interval atât de mare al valorilor farmacocinetice. Unul dintre factorii care influenţează variabilitatea farmacocinetică a furosemidei este tocmai procesul de absorbţie care depinde de 8
9 proprietăţile intrinseci ale acestei substanţe/solubilitate redusă, permeabilitate redusă, asociate cu efecte necunoscute ale formulei. Argumentele solicitantului conform cărora nu există nicio corelare între cantitatea de furosemidă absorbită şi diureză, iar formulele cu eliberare controlată şi cele cu eliberare imediată produc aproape aceeaşi diureză, nu au fost considerate suficiente de către grupul de experţi pentru a dovedi siguranţa şi eficacitatea pentru Furosemide Vitabalans. Mai mult, grupul a considerat că există un motiv de îngrijorare privind siguranţa la introducerea pe piaţă a unui produs pentru o astfel de indicaţie (insuficienţă cardiacă) în condiţiile în care eficacitatea nu a fost demonstrată. Având în vedere variabilitatea predictibilă a produsului, principalul risc asociat cu furosemida ar fi lipsa eficacităţii acesteia. Pe baza datelor bibliografice prezentate, analizate împreună cu datele farmaceutice, solicitantul nu a reuşit să stabilească relevanţa acestor date pentru a demonstra siguranţa şi eficacitatea pentru Furosemide Vitabalans. Motive pentru refuz Pe baza datelor bibliografice prezentate, analizate împreună cu documentaţia farmaceutică suplimentară, solicitantul nu a reuşit să stabilească relevanţa acestor date pentru a demonstra siguranţa şi eficacitatea pentru Furosemide Vitabalans şi denumirile asociate. Întrucât Comitetul a analizat notificarea privind sesizarea iniţiată de Estonia, în temeiul articolului 29 alineatul (4) din Directiva 2001/83/CE. Polonia şi Lituania au considerat că acordarea autorizaţiei de introducere pe piaţă constituie un risc major potenţial pentru sănătatea publică. Solicitantul nu a demonstrat în mod suficient că o expunere potenţial mai redusă sau mai ridicată la furosemidă nu ar influenţa eficacitatea sau siguranţa. Datele furnizate nu demonstrează faptul că Furosemide Vitabalans este similar cu produsele descrise în literatura de specialitate prezentată. Având în vedere această lipsă de dovezi, comitetul a considerat că motivele de îngrijorare invocate de statele membre cu privire la riscul major potenţial pentru sănătatea publică sunt justificate. CHMP a recomandat refuzul acordării autorizaţiei de introducere pe piaţă pentru Furosemide Vitabalans şi denumirile asociate (vezi Anexa I). 9
Furosemide Vitabalans Annex I_II_ro
 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Microsoft Word - RO_EMEA
 ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
EMA ENRO
 Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Enurace Annexes I-II-III
 ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
Milnacipran Pierre Fabre Medicament, INN: milnacipran
 ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
EMA ENRO
 Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
EllaOne,INN-ulipristal acetate
 Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă d
 Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
SPC in English
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
COMISIA EUROPEANĂ Bruxelles, C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din de completare a Regulamentului (UE) nr
 COMISIA EUROPEANĂ Bruxelles, 30.4.2018 C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 30.4.2018 de completare a Regulamentului (UE) nr. 1143/2014 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 30.4.2018 C(2018) 2526 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 30.4.2018 de completare a Regulamentului (UE) nr. 1143/2014 al Parlamentului European și al Consiliului
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
Microsoft Word - Lansoprazole_Annex_I-III_ro
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COM
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI LOMEXIN 20 mg/g cremă 2. COMPOZIŢIA
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI LOMEXIN 20 mg/g cremă 2. COMPOZIŢIA
Microsoft Word - 663E5DA5.doc
 Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
Ghid Privind aplicarea regimului de avizare în temeiul articolului 4 alineatul (3) din Regulamentul privind agențiile de rating de credit 20/05/2019 E
 Ghid Privind aplicarea regimului de avizare în temeiul articolului 4 alineatul (3) din Regulamentul privind agențiile de rating de credit 20/05/2019 ESMA33-9-282 RO Cuprins I. Domeniu de aplicare... 3
Ghid Privind aplicarea regimului de avizare în temeiul articolului 4 alineatul (3) din Regulamentul privind agențiile de rating de credit 20/05/2019 ESMA33-9-282 RO Cuprins I. Domeniu de aplicare... 3
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1
 Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologie
 MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
Microsoft Word - decizia docx
 1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
Quality Review of Documents human product information template version 8 clean
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10459/2017/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI ACEVIREX 50 mg/g cremă
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10459/2017/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI ACEVIREX 50 mg/g cremă
RCP_4839_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
REGULAMENTUL DE PUNERE ÎN APLICARE (UE) 2016/ AL COMISIEI - din 16 octombrie de stabilire a unor standarde tehnice de
 28.1.2016 L 21/45 REGULAMENTUL DE PUNERE ÎN APLICARE (UE) 2016/100 AL COMISIEI din 16 octombrie 2015 de stabilire a unor standarde tehnice de punere în aplicare care specifică procedura de adoptare a deciziei
28.1.2016 L 21/45 REGULAMENTUL DE PUNERE ÎN APLICARE (UE) 2016/100 AL COMISIEI din 16 octombrie 2015 de stabilire a unor standarde tehnice de punere în aplicare care specifică procedura de adoptare a deciziei
Recomandarea Comisiei din 18 iulie 2018 privind orientările pentru implementarea armonizată a Sistemului european de management al traficului feroviar
 19.7.2018 RO Jurnalul Oficial al Uniunii Europene C 253/1 I (Rezoluții, recomandări și avize) RECOMANDĂRI COMISIA EUROPEANĂ RECOMANDAREA COMISIEI din 18 iulie 2018 privind orientările pentru implementarea
19.7.2018 RO Jurnalul Oficial al Uniunii Europene C 253/1 I (Rezoluții, recomandări și avize) RECOMANDĂRI COMISIA EUROPEANĂ RECOMANDAREA COMISIEI din 18 iulie 2018 privind orientările pentru implementarea
COMISIA EUROPEANĂ Bruxelles, COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea
 COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
Componen
 Anexa nr.1 la Hotărârea nr. 17 / 11.10.2007 REGULAMENTUL DE ORGANIZARE ŞI FUNCŢIONARE AL COMITETULUI REGIONAL DE EVALUARE STRATEGICĂ ŞI CORELARE CENTRU CAPITOLUL I Definiţii aplicabile Comitetului Regional
Anexa nr.1 la Hotărârea nr. 17 / 11.10.2007 REGULAMENTUL DE ORGANIZARE ŞI FUNCŢIONARE AL COMITETULUI REGIONAL DE EVALUARE STRATEGICĂ ŞI CORELARE CENTRU CAPITOLUL I Definiţii aplicabile Comitetului Regional
Microsoft Word - decizie_2198_a.doc
 În conformitate cu prevederile art. 266 alin. (2) din Ordonanţa de urgenţă a Guvernului nr. 34/2006 privind atribuirea contractelor de achiziţie publică, a contractelor de concesiune de lucrări publice
În conformitate cu prevederile art. 266 alin. (2) din Ordonanţa de urgenţă a Guvernului nr. 34/2006 privind atribuirea contractelor de achiziţie publică, a contractelor de concesiune de lucrări publice
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
Anexe PO concurs
 B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
EUIPO NOTES-RO Mod /2016 Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale
 Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale 1.1 Utilizarea formularului Formularul se poate obţine gratuit de la EUIPO şi poate
Note privind formularul de cerere pentru o declaraţie de anulare a unei mărci a Uniunii Europene 1. Observaţii generale 1.1 Utilizarea formularului Formularul se poate obţine gratuit de la EUIPO şi poate
ANEXA nr
 ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunarea de Jos din Galati 1.2 Facultatea / Departamentul Medicina si Farmacie / Stiinte
ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunarea de Jos din Galati 1.2 Facultatea / Departamentul Medicina si Farmacie / Stiinte
COMISIA EUROPEANĂ Bruxelles, COM(2017) 769 final 2017/0347 (COD) Propunere de REGULAMENT AL PARLAMENTULUI EUROPEAN ŞI AL CONSILIULUI de abr
 COMISIA EUROPEANĂ Bruxelles, 19.12.2017 COM(2017) 769 final 2017/0347 (COD) Propunere de REGULAMENT AL PARLAMENTULUI EUROPEAN ŞI AL CONSILIULUI de abrogare a Regulamentului (UE) nr. 256/2014 al Parlamentului
COMISIA EUROPEANĂ Bruxelles, 19.12.2017 COM(2017) 769 final 2017/0347 (COD) Propunere de REGULAMENT AL PARLAMENTULUI EUROPEAN ŞI AL CONSILIULUI de abrogare a Regulamentului (UE) nr. 256/2014 al Parlamentului
PowerPoint Presentation
 Aspecte practice si exemple pentru aplicarea Regulamentului (UE) nr. 528/2012 Irina Tănase Seminar APDCR, 8 iunie 2017 Obligatii sub BPR REACH si BPR Cum se aplică REACH În conformitate cu art 15 din substanțelor
Aspecte practice si exemple pentru aplicarea Regulamentului (UE) nr. 528/2012 Irina Tănase Seminar APDCR, 8 iunie 2017 Obligatii sub BPR REACH si BPR Cum se aplică REACH În conformitate cu art 15 din substanțelor
Lineamientos para la Evaluación
 Ghid privind Raportarea, Monitorizarea și Evaluarea proiectelor finanțate în cadrul programului Maratonul Justiției 1. Introducere Sumarul cerințelor de raportare: a. Rapoartele narative finale b. Rapoartele
Ghid privind Raportarea, Monitorizarea și Evaluarea proiectelor finanțate în cadrul programului Maratonul Justiției 1. Introducere Sumarul cerințelor de raportare: a. Rapoartele narative finale b. Rapoartele
Microsoft Word _ANEXA_II_CRESC - final.doc
 Anexa nr.2 REGULAMENT - CADRU DE ORGANIZARE ŞI FUNCŢIONARE AL COMITETULUI REGIONAL DE EVALUARE STRATEGICĂ ŞI CORELARE CAPITOLUL I Definiţii aplicabile Comitetului Regional de Evaluare Strategică şi Corelare
Anexa nr.2 REGULAMENT - CADRU DE ORGANIZARE ŞI FUNCŢIONARE AL COMITETULUI REGIONAL DE EVALUARE STRATEGICĂ ŞI CORELARE CAPITOLUL I Definiţii aplicabile Comitetului Regional de Evaluare Strategică şi Corelare
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
FAQs as published on the web - EN version
 13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
COMISIA EUROPEANĂ Bruxelles, COM(2011) 377 final 2011/0164 (NLE) Propunere de DIRECTIVĂ A CONSILIULUI de modificare a Directivei 76/768/CEE
 COMISIA EUROPEANĂ Bruxelles, 23.6.2011 COM(2011) 377 final 2011/0164 (NLE) Propunere de DIRECTIVĂ A CONSILIULUI de modificare a Directivei 76/768/CEE cu privire la produsele cosmetice, în scopul adaptării
COMISIA EUROPEANĂ Bruxelles, 23.6.2011 COM(2011) 377 final 2011/0164 (NLE) Propunere de DIRECTIVĂ A CONSILIULUI de modificare a Directivei 76/768/CEE cu privire la produsele cosmetice, în scopul adaptării
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7029/2014/01-02-03-04-05 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Avodart 0,5 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7029/2014/01-02-03-04-05 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Avodart 0,5 mg
1
 1 C U P R I N S Articolul 1. Dispoziții generale 3 Articolul 2. Taxa de înregistrare și taxa arbitrală 3 Articolul 3. Reguli privind taxa arbitrală 4 Articolul 4. Avansarea taxei arbitrale 5 Articolul
1 C U P R I N S Articolul 1. Dispoziții generale 3 Articolul 2. Taxa de înregistrare și taxa arbitrală 3 Articolul 3. Reguli privind taxa arbitrală 4 Articolul 4. Avansarea taxei arbitrale 5 Articolul
untitled
 CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleos nr.6, Sector 3,..., România, CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642 www.cnsc.ro În conformitate
CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleos nr.6, Sector 3,..., România, CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642 www.cnsc.ro În conformitate
ANEXA nr
 ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galaţi 1.2 Facultatea / Departamentul Medicină şi Farmacie / Ştiinţe
ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galaţi 1.2 Facultatea / Departamentul Medicină şi Farmacie / Ştiinţe
C(2015)6507/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la
 Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
Microsoft Word - decizie_2149_a.doc
 CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleus nr.6 Sector 3,... România,CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642, +4 021 8900745 www.cnsc.ro În
CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleus nr.6 Sector 3,... România,CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642, +4 021 8900745 www.cnsc.ro În
Anexa II Concluzii ştiinţifice şi motivele concluziilor 8
 Anexa II Concluzii ştiinţifice şi motivele concluziilor 8 Concluzii ştiinţifice şi motivele concluziilor După analiza recomandării PRAC din data de 5 septembrie 2013 cu privire la Numeta G13%E şi Numeta
Anexa II Concluzii ştiinţifice şi motivele concluziilor 8 Concluzii ştiinţifice şi motivele concluziilor După analiza recomandării PRAC din data de 5 septembrie 2013 cu privire la Numeta G13%E şi Numeta
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE Bine ați venit pe site-ul sondajului online Dedicated
 Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Ordin ANRE nr.164 din
 ORDIN nr. 164 din 7 decembrie 2015 privind aprobarea certificării Companiei Naţionale de Transport al Energiei Electrice "Transelectrica" - S.A. ca operator de transport şi de sistem al sistemului electroenergetic
ORDIN nr. 164 din 7 decembrie 2015 privind aprobarea certificării Companiei Naţionale de Transport al Energiei Electrice "Transelectrica" - S.A. ca operator de transport şi de sistem al sistemului electroenergetic
Cuprins Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac
 Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Vokanamet, INN-canagliflozin-metformin
 ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DOXIUM 500 mg capsule 2.
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DOXIUM 500 mg capsule 2.
Instanţa de fond: Judecătoria Economică de Circumscripţie Dosarul nr
 Dosarul nr. 3ra-1288/16 Instanţa de fond: Judecătoria Rîşcani mun. Chişinău V. Jomiru-Niculiţă Instanţa de apel: CA Chişinău M. Ciugureanu, Gr. Daşchevici, Iu. Cotruţă Î N C H E I E R E 28 septembrie 2016
Dosarul nr. 3ra-1288/16 Instanţa de fond: Judecătoria Rîşcani mun. Chişinău V. Jomiru-Niculiţă Instanţa de apel: CA Chişinău M. Ciugureanu, Gr. Daşchevici, Iu. Cotruţă Î N C H E I E R E 28 septembrie 2016
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1
 Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
RCP_870_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 870/2008/01 Anexa 2` Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mucosolvan Junior 15 mg/5
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 870/2008/01 Anexa 2` Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mucosolvan Junior 15 mg/5
Microsoft Word - RPMC de publicat.docx
 REGULAMENTUL PRIVIND PROCEDURILE DE MONITORIZARE FINANCIARĂ ȘI DE LUARE A DECIZIILOR DE SANCŢIONARE A CLUBURILOR LICENŢIATE DE LIGA I București 2018 P 1 P 2 CAPITOLUL 1 DISPOZIŢII GENERALE Articolul 1
REGULAMENTUL PRIVIND PROCEDURILE DE MONITORIZARE FINANCIARĂ ȘI DE LUARE A DECIZIILOR DE SANCŢIONARE A CLUBURILOR LICENŢIATE DE LIGA I București 2018 P 1 P 2 CAPITOLUL 1 DISPOZIŢII GENERALE Articolul 1
AUTORIZATIE DE PUNERE PE PIATA NR. 6906/2006/01-02 Anexa 1 Prospect FUROSEMID LPH 40 mg, comprimate Furosemidă Compoziţie Un comprimat conţine furosem
 AUTORIZATIE DE PUNERE PE PIATA NR. 6906/2006/01-02 Anexa 1 Prospect FUROSEMID LPH 40 mg, comprimate Furosemidă Compoziţie Un comprimat conţine furosemidă 40 mg şi excipienţi: lactoză monohidrat 100 mesh,
AUTORIZATIE DE PUNERE PE PIATA NR. 6906/2006/01-02 Anexa 1 Prospect FUROSEMID LPH 40 mg, comprimate Furosemidă Compoziţie Un comprimat conţine furosemidă 40 mg şi excipienţi: lactoză monohidrat 100 mesh,
Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LE
 Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LEGISLATIVE ACTS AND OTHER INSTRUMENTS: CORRIGENDUM/RECTIFICATIF
Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LEGISLATIVE ACTS AND OTHER INSTRUMENTS: CORRIGENDUM/RECTIFICATIF
PROCEDURĂ GENERALĂ COD: PGONFR - 04 TRATAREA RECLAMAȚIILOR ȘI APELURILOR REVIZIE: 2 Pagina: 1 / 7 Exemplar nr. : APROBAT DIRECTOR ONFR, Vasile STĂNESC
 Pagina: 1 / 7 APROBAT DIRECTOR ONFR, Vasile STĂNESCU AVIZAT ŞEF DEPARTAMENT SUBSISTEME STRUCTURALE ŞI VEHICULE, Constantin ANDRONACHE Data intrării în vigoare a: Reviziei zero: 01.03.2014 Reviziei actuale:
Pagina: 1 / 7 APROBAT DIRECTOR ONFR, Vasile STĂNESCU AVIZAT ŞEF DEPARTAMENT SUBSISTEME STRUCTURALE ŞI VEHICULE, Constantin ANDRONACHE Data intrării în vigoare a: Reviziei zero: 01.03.2014 Reviziei actuale:
AM_Ple_LegReport
 7.3.2016 A8-0046/295 295 Considerentul 65 (65) Verificarea conformității cu cerințele juridice prin controale are o importanță fundamentală pentru a se asigura că obiectivele regulamentului sunt realizate
7.3.2016 A8-0046/295 295 Considerentul 65 (65) Verificarea conformității cu cerințele juridice prin controale are o importanță fundamentală pentru a se asigura că obiectivele regulamentului sunt realizate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COM
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
Consiliul Uniunii Europene Bruxelles, 17 decembrie 2018 (OR. en) 14991/18 ADD 1 LIMITE PV CONS 65 COMPET 834 IND 381 MI 913 RECH 513 ESPACE 72 PROIECT
 Consiliul Uniunii Europene Bruxelles, 17 decembrie 2018 (OR. en) 14991/18 ADD 1 LIMITE PV CONS 65 COMPET 834 IND 381 MI 913 RECH 513 ESPACE 72 PROIECT DE PROCES-VERBAL CONSILIUL UNIUNII EUROPENE (Competitivitate
Consiliul Uniunii Europene Bruxelles, 17 decembrie 2018 (OR. en) 14991/18 ADD 1 LIMITE PV CONS 65 COMPET 834 IND 381 MI 913 RECH 513 ESPACE 72 PROIECT DE PROCES-VERBAL CONSILIUL UNIUNII EUROPENE (Competitivitate
Jurnalul Oficial al Uniunii Europene C 144 I Ediția în limba română Comunicări și informări 25 aprilie 2019 Anul 62 Cuprins II Comunicări COMUNICĂRI P
 Jurnalul Oficial al Uniunii Europene C 144 I Ediția în limba română Comunicări și informări 25 aprilie 2019 Anul 62 Cuprins II Comunicări COMUNICĂRI PVENIND DE LA INSTITUȚIILE, ORGANELE ȘI ORGANISMELE
Jurnalul Oficial al Uniunii Europene C 144 I Ediția în limba română Comunicări și informări 25 aprilie 2019 Anul 62 Cuprins II Comunicări COMUNICĂRI PVENIND DE LA INSTITUȚIILE, ORGANELE ȘI ORGANISMELE
RCP_4611_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4611/2012/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI RILUZOL
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4611/2012/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI RILUZOL
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
st00TSCG26.ro12
 Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3213/2011/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3213/2011/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS
Microsoft Word - decizie_164_a.doc
 CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleus nr.6 Sector 3,... România,CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642, +4 021 8900745 www.cnsc.ro În
CONSILIUL NAŢIONAL DE SOLUŢIONARE A CONTESTAŢIILOR C. N. S. C. Str. Stavropoleus nr.6 Sector 3,... România,CP 030084, CIF 20329980 Tel. +4 021 3104641 Fax. +4 021 3104642, +4 021 8900745 www.cnsc.ro În
Republica Moldova CURTEA CONSTITUŢIONALĂ AVIZ privind constatarea circumstanțelor care justifică interimatul funcției de Președinte al Republicii Mold
 Republica Moldova CURTEA CONSTITUŢIONALĂ AVIZ privind constatarea circumstanțelor care justifică interimatul funcției de Președinte al Republicii Moldova pentru exercitarea obligației constituționale de
Republica Moldova CURTEA CONSTITUŢIONALĂ AVIZ privind constatarea circumstanțelor care justifică interimatul funcției de Președinte al Republicii Moldova pentru exercitarea obligației constituționale de
Act LexBrowser
 MINISTERUL SĂNĂTĂŢII Nr. 10 din 8 ianuarie 2010 MINISTERUL MEDIULUI ŞI PĂDURILOR Nr. 368 din 17 martie 2010 AUTORITATEA NAŢIONALĂ SANITARĂ VETERINARĂ ŞI PENTRU SIGURANŢA ALIMENTELOR Nr. 11 din 4 martie
MINISTERUL SĂNĂTĂŢII Nr. 10 din 8 ianuarie 2010 MINISTERUL MEDIULUI ŞI PĂDURILOR Nr. 368 din 17 martie 2010 AUTORITATEA NAŢIONALĂ SANITARĂ VETERINARĂ ŞI PENTRU SIGURANŢA ALIMENTELOR Nr. 11 din 4 martie
simva leaflet
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
31996L0059.doc
 31996L0059 DIRECTIVA 96/59/CE A CONSILIULUI din 16 septembrie 1996 privind eliminarea bifenililor policloruraţi şi a terfenilior policloruraţi (PCB/TPC) CONSILIUL UNIUNII EUROPENE, având în vedere Tratatul
31996L0059 DIRECTIVA 96/59/CE A CONSILIULUI din 16 septembrie 1996 privind eliminarea bifenililor policloruraţi şi a terfenilior policloruraţi (PCB/TPC) CONSILIUL UNIUNII EUROPENE, având în vedere Tratatul
Jurnalul Oficial al Uniunii Europene L 92 Ediția în limba română Legislație Anul 62 1 aprilie 2019 Cuprins II Acte fără caracter legislativ DECIZII De
 Jurnalul Oficial al Uniunii Europene L 92 Ediția în limba română Legislație Anul 62 1 aprilie 2019 Cuprins II Acte fără caracter legislativ DECIZII Decizia (PESC) 2019/535 a Consiliului din 29 martie 2019
Jurnalul Oficial al Uniunii Europene L 92 Ediția în limba română Legislație Anul 62 1 aprilie 2019 Cuprins II Acte fără caracter legislativ DECIZII Decizia (PESC) 2019/535 a Consiliului din 29 martie 2019
HOTARÂRE nr
 HOTĂRÂRE nr. 1.876 din 22 decembrie 2005 privind cerinţele minime de securitate şi sănătate referitoare la expunerea lucrătorilor la riscurile generate de vibratii EMITENT: GUVERNUL PUBLICAT ÎN: MONITORUL
HOTĂRÂRE nr. 1.876 din 22 decembrie 2005 privind cerinţele minime de securitate şi sănătate referitoare la expunerea lucrătorilor la riscurile generate de vibratii EMITENT: GUVERNUL PUBLICAT ÎN: MONITORUL
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/ Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
3 Aprobate prin Hotărîrea Guvernului nr. din 2016 CERINŢE MINIME de securitate şi sănătate în muncă pentru protecţia salariatelor gravide, care au năs
 3 Aprobate prin Hotărîrea Guvernului nr. din 2016 CERINŢE MINIME de securitate şi sănătate în muncă pentru protecţia salariatelor gravide, care au născut de curînd sau care alăptează I. DISPOZIŢII GENERALE
3 Aprobate prin Hotărîrea Guvernului nr. din 2016 CERINŢE MINIME de securitate şi sănătate în muncă pentru protecţia salariatelor gravide, care au născut de curînd sau care alăptează I. DISPOZIŢII GENERALE
RCP
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2177/2009/01-02 Anexa 2 NR.2178/2009/01-02 NR.2179/2009/01-02 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2177/2009/01-02 Anexa 2 NR.2178/2009/01-02 NR.2179/2009/01-02 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A
Lege Nr. 97 din pentru modificarea şi completarea Legii nr. 66-XVI din 27 martie 2008 privind protecţia indicaţiilor geografice, denumirilo
 Republica Moldova PARLAMENTUL LEGE Nr. 97 din 13.05.2016 pentru modificarea şi completarea Legii nr. 66-XVI din 27 martie 2008 privind protecţia indicaţiilor geografice, denumirilor de origine şi specialităţilor
Republica Moldova PARLAMENTUL LEGE Nr. 97 din 13.05.2016 pentru modificarea şi completarea Legii nr. 66-XVI din 27 martie 2008 privind protecţia indicaţiilor geografice, denumirilor de origine şi specialităţilor
CONSILIUL CONCURENŢEI СОВЕТ ПО КОНКУРЕНЦИИ PLENUL CONSILIULUI CONCURENŢEI DECIZIE Nr. ASO-42 din mun. Chişinău Plenul Consiliului Concurenţ
 CONSILIUL CONCURENŢEI СОВЕТ ПО КОНКУРЕНЦИИ PLENUL CONSILIULUI CONCURENŢEI DECIZIE Nr. ASO-42 din 06.06.2019 mun. Chişinău Plenul Consiliului Concurenţei, acționând în temeiul art. 41 al Legii concurenţei
CONSILIUL CONCURENŢEI СОВЕТ ПО КОНКУРЕНЦИИ PLENUL CONSILIULUI CONCURENŢEI DECIZIE Nr. ASO-42 din 06.06.2019 mun. Chişinău Plenul Consiliului Concurenţei, acționând în temeiul art. 41 al Legii concurenţei
FISA CU DATE DE SECURITATE BREEZE LEMON Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substan
 Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substantei/amestecului si a societatii/întreprinderii 1.1. Element de identificare a produsului Nume
Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substantei/amestecului si a societatii/întreprinderii 1.1. Element de identificare a produsului Nume
Regulamentul de punere în aplicare (UE) nr. 29/2012 al Comisiei din 13 ianuarie 2012 privind standardele de comercializare a uleiului de măsline
 L 12/14 Jurnalul Oficial al Uniunii Europene 14.1.2012 REGULAMENTUL DE PUNERE ÎN APLICARE (UE) NR. 29/2012 AL COMISIEI din 13 ianuarie 2012 privind standardele de comercializare a uleiului de măsline (text
L 12/14 Jurnalul Oficial al Uniunii Europene 14.1.2012 REGULAMENTUL DE PUNERE ÎN APLICARE (UE) NR. 29/2012 AL COMISIEI din 13 ianuarie 2012 privind standardele de comercializare a uleiului de măsline (text
untitled
 ROMÂNIA MINISTERUL AGRICULTURII ŞI DEZVOLTĂRII RURALE Regulament de organizare şi funcţionare a Comitetului Naţional de Coordonare a Reţelei Naţionale de Dezvoltare Rurală 2007-2013 Articolul 1 Dispoziţii
ROMÂNIA MINISTERUL AGRICULTURII ŞI DEZVOLTĂRII RURALE Regulament de organizare şi funcţionare a Comitetului Naţional de Coordonare a Reţelei Naţionale de Dezvoltare Rurală 2007-2013 Articolul 1 Dispoziţii
Avamys, INN-fluticasone furoate
 REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI AVAMYS 27,5 micrograme/puf, spray nazal suspensie 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare puf eliberează furoat de
REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI AVAMYS 27,5 micrograme/puf, spray nazal suspensie 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare puf eliberează furoat de
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura d
 ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
EN
 COMISIA EUROPEANĂ Bruxelles, 6.8.2010 COM(2010)420 final 2010/0228 (NLE) C7-0400/10 Propunere de DECIZIE A CONSILIULUI privind încheierea Acordului între Uniunea Europeană și Republica Federativă a Braziliei
COMISIA EUROPEANĂ Bruxelles, 6.8.2010 COM(2010)420 final 2010/0228 (NLE) C7-0400/10 Propunere de DECIZIE A CONSILIULUI privind încheierea Acordului între Uniunea Europeană și Republica Federativă a Braziliei
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
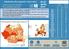 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Microsoft Word - anunt prealabil selectie 2018.doc
 INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
Utilizare curentă EIOPA EIOPA-BoS-19/040 RO 19 februarie 2019 Recomandări pentru sectorul asigurărilor în contextul retragerii Regatului Unit din Uniu
 Utilizare curentă EIOPA EIOPA-BoS-19/040 RO 19 februarie 2019 Recomandări pentru sectorul asigurărilor în contextul retragerii Regatului Unit din Uniunea Europeană Recomandări Introducere 1. Conform articolului
Utilizare curentă EIOPA EIOPA-BoS-19/040 RO 19 februarie 2019 Recomandări pentru sectorul asigurărilor în contextul retragerii Regatului Unit din Uniunea Europeană Recomandări Introducere 1. Conform articolului
eb76_3_parlemeter_report_ro
 Eurobarometru 76.3 Parlametru Realizat de TNS Opinion & Social la cererea Parlamentului European Sondaj coordonat de Direcţia Generală Comunicare CUPRINS INTRODUCERE...3 REZUMAT...5 I. INFORMAŢII PRIVIND
Eurobarometru 76.3 Parlametru Realizat de TNS Opinion & Social la cererea Parlamentului European Sondaj coordonat de Direcţia Generală Comunicare CUPRINS INTRODUCERE...3 REZUMAT...5 I. INFORMAŢII PRIVIND
32006D0770
 32006D0770 Jurnalul Oficial L 312, 11/11/2006 p. 0059-0065 Decizia Comisiei din 9 noiembrie 2006 de modificare a anexei la Regulamentul (CE) nr. 1228/2003 privind condiţiile de acces la reţea pentru schimburile
32006D0770 Jurnalul Oficial L 312, 11/11/2006 p. 0059-0065 Decizia Comisiei din 9 noiembrie 2006 de modificare a anexei la Regulamentul (CE) nr. 1228/2003 privind condiţiile de acces la reţea pentru schimburile
