COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
|
|
|
- Romeo Stancu
- 4 ani în urmă
- Vzualizari:
Transcriere
1 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului (European Medicines Agency = EMA) referitor la suspendarea autorizaţiei de punere pe piaţă pentru medicamentul Numeta G13%E şi la introducerea unor noi măsuri de reducere la minimum a riscului pentru medicamentul Numeta G16%E. EMA, 20 septembrie 2013 Comunicat de presă EMA referitor la suspendarea autorizaţiei de punere pe piaţă pentru medicamentul Numeta G13%E şi la introducerea unor noi măsuri de reducere la minimum a riscului pentru medicamentul Numeta G16%E Grupul de Coordonare pentru Procedurile de Recunoaştere Mutuală şi Descentralizată uman (Co-ordination Group for Mutual Recognition and Decentralised Procedures Human = CMDh), organism de reglementare în domeniul medicamentului, care reprezintă statele membre ale Uniunii Europene, a adoptat prin consens recomandarea de suspendare a autorizaţiei de punere pe piaţă pentru medicamentul Numeta G13%E, din cauza riscului de apariţie a hipermagneziemiei (concentraţii sanguine crescute de magneziu). Autorizaţia de punere pe piaţă pentru medicamentul Numeta G13%E care este administrat intravenos la nou-născuţii prematur pentru asigurarea suportului nutriţional (nutriţie intravenoasă sau parenterală), va fi suspendată până la apariţia unui preparat reformulat. Referitor la un alt preparat pentru nutriţie intravenoasă, Numeta G16%E, utilizat la nou-născuţii la termen şi la copiii cu vârsta de până la doi ani, CMDh a considerat că raportul beneficiu-risc rămâne pozitiv, cu condiţia monitorizării de către profesioniştii din domeniul sănătăţii a concentraţiilor sanguine de magneziu ale pacienţilor înaintea administrării tratamentului şi la intervale de timp adecvate în timpul acestuia, în concordanţă cu practica clinică de rutină şi cu 1/7
2 particularităţile clinice individuale. În cazul pacienţilor care prezintă concentraţii sanguine crescute de magneziu sau semne de hipermagneziemie, tratamentul cu medicamentul Numeta G16%E trebuie oprit sau trebuie redusă rata de perfuzare. Soluţiile Numeta se administrează în vederea asigurării suportului nutriţional la copiii care nu pot fi alimentaţi pe cale orală sau cu ajutorul unei sonde de alimentare. Aceste perfuzii conţin substanţe nutritive precum: glucoză (zahăr), lipide (grăsimi), aminoacizi şi alţi constituenţi importanţi, printre care şi magneziu. Hipermagneziemia este o afecţiune gravă, printre simptomele căreia se pot enumera slăbiciune, senzaţie de greaţă şi vărsături, dificultăţi de respiraţie, hipotensiune (presiune sanguină scăzută) şi aritmii (bătăi neregulate ale inimii). Reevaluarea medicamentelor Numeta G13%E şi Numeta G16%E a fost efectuată de către Comitetul de farmacovigilenţă pentru evaluarea riscului (Pharmacovigilance Risk Assessment Committee = PRAC) al EMA, ca urmare a mai multor raportări de apariţie a unor reacţii adverse de hipermagneziemie (fără manifestări clinice) la nou-născuţi prematur. Ca măsură de precauţie, deţinătorul autorizaţiei de punere pe piaţă a decis, din proprie iniţiativă, să retragă medicamentul Numeta G13%E de pe piaţa întregii Uniuni Europene (UE). PRAC a evaluat datele referitoare la riscul de hipermagneziemie asociat cu soluţiile Numeta G13%E şi Numeta G16%E, reieşite din studiile clinice, reacţiile raportate după punerea pe piaţă şi din literatura de specialitate, având în vedere ghidurile de tratament disponibile. Părţile interesate au fost şi acestea invitate să transmită date relevante în vederea susţinerii acestei evaluări, consultându-se totodată şi Comitetul pentru medicamente de uz pediatric (Paediatric Committee = PDCO) al EMA. După analiza ghidurilor disponibile şi a literaturii de specialitate şi ţinând cont de conţinutul de magneziu al medicamentului Numeta, PRAC a concluzionat că administrarea soluţiei Numeta G13%E poate determina creşterea riscului de apariţie a hipermagneziemiei. În plus, PRAC a observat că nou-născuţii prematur prezintă un risc şi mai accentuat, deoarece rinichii acestora sunt imaturi, având o capacitate mai redusă de eliminare a magneziului din organism. Totodată, PRAC a mai observat şi că, în cazul nou-născuţilor prematur, identificarea simptomelor de hipermagneziemie este mai dificilă, hipermagneziemia rămânând neobservată până în momentul în care determină apariţia de complicaţii grave. 2/7
3 În cazul medicamentului Numeta G16%E, PRAC a concluzionat că, deşi conţinutul de magneziu poate duce la un aport de magneziu uşor mai mare decât cel prevăzut în anumite ghiduri, măsurile propuse, inclusiv actualizarea informaţiilor despre medicament şi realizarea altui studiu, sunt suficiente pentru a asigura utilizarea acestuia în condiţii de siguranţă. Informaţiile despre medicament trebuie revizuite în mod corespunzător, iar profesioniştii din domeniul sănătăţii trebuie informaţi cu privire la riscul posibil de apariţie a hipermagneziemiei şi la măsurile care trebuie luate pentru reducerea la minimum a acestui risc, care este crescut la pacienţii cu insuficienţă renală şi la acei pacienţi ale căror mame au primit magneziu suplimentar înainte de naştere. În plus, PRAC a recomandat realizarea unui studiu în vederea evaluării în continuare a concentraţiei sanguine a magneziului, în urma administrării medicamentului Numeta G16%E la nou-născuţii la termen şi copiii cu vârsta mai mică de doi ani. Deoarece recomandările PRAC au fost adoptate prin consens de către CMDh, acestea vor fi implementate direct în toate statele membre, în concordanţă cu un calendar stabilit. Informaţii pentru părinţi şi îngrijitori: Autorizaţia de punere pe piaţă pentru preparatul pentru nutriţie parenterală Numeta G13%E a fost suspendată din cauza riscului de apariţie a hipermagneziemiei (niveluri crescute ale magneziului în sânge), până la apariţia unui preparat reformulat. Numeta G13%E este administrat intravenos, pentru a asigura suportul nutriţional la nou-născuţii prematur care nu pot fi alimentaţi pe cale orală sau cu ajutorul unei sonde de alimentare. Preparatul pentru nutriţie parenterală Numeta G16%E poate fi administrat în continuare nou-născuţilor la termen şi copiilor cu vârsta sub 2 ani, cu condiţia monitorizării de către medic a concentraţiilor sanguine ale magneziului înainte de administrarea preparatului şi la intervale adecvate după iniţierea tratamentului. Dacă nivelul sanguin al magneziului este crescut, medicul va opri administrarea preparatului Numeta G16%E sau va reduce rata de perfuzie. Apariţia hipermagneziemiei severe este rară însă poate avea efecte clinice adverse. Medicii vor monitoriza nou-născuţii şi copiii aflaţi în tratament cu Numeta G16%E pentru a observa apariţia unor simptome de 3/7
4 hipermagneziemie precum slăbiciune, greaţă şi vărsături, dificultăţi de respiraţie, hipotensiune (presiune sanguină scăzută) şi aritmii (bătăi neregulate ale inimii). Părinţii care au întrebări sau îngrijorări trebuie să discute cu medicul curant sau cu alt profesionist din domeniul sănătăţii. Informaţii pentru profesioniştii din domeniul sănătăţii: Referitor la medicamentul Numeta G13%E: Ca urmare a unor raportări de apariţie a hipermagneziemiei la nou-născuţii prematuri, autorizaţia de punere pe piaţă pentru preparatul nutriţional Numeta G13%E a fost suspendată până la apariţia unui preparat reformulat. Pe durata perioadei de suspendare a autorizaţiei de punere pe piaţă pentru medicamentul Numeta G13%E, profesioniştii din domeniul sănătăţii trebuie să utilizeze soluţii alternative de nutriţie, printre care medicamente preparate standardizat, autorizate, sau preparate individual. Referitor la medicamentul Numeta G16%E: Raportul beneficiu-risc pentru preparatul nutriţional Numeta G16%E, utilizat la nou-născuţii la termen şi la copiii cu vârsta de până la doi ani, rămâne pozitiv. Cu toate acestea, profesioniştii din domeniul sănătăţii trebuie să aibă în vedere riscul potenţial de apariţie a hipermagneziemiei. Ricul este crescut în cazul pacienţilor cu disfuncţie renală şi la nounăscuţii ale căror mame au primit magneziu suplimentar înainte de naştere. În cazul tratamentului cu Numeta G16%E, medicii trebuie să monitorizeze concentraţiile serice ale magneziului şi altor electroliţi, atât la momentul iniţial cât şi ulterior, la intervale adecvate. Monitorizarea trebuie efectuată în concordanţă cu practica clinică de rutină şi cu particularităţile clinice individuale. Totodată, medicii trebuie să monitorizeze pacienţii pentru depistarea apariţiei semnelor şi simptomelor de hipermagneziemie precum greaţă, vărsături şi eritem facial, slăbiciune generalizată, insuficienţă respiratorie, 4/7
5 hipotensiune şi aritmii. Semnele clinice pot rămâne neidentificate dacă hipermagneziemia nu este severă. În cazul apariţiei hipermagneziemiei tratamentul cu Numeta G16%E se opreşte sau se reduce rata de perfuzare şi se prescriu fluide alternative, nutriţie şi electroliţi după cum se consideră clinic adecvat. Informaţii suplimentare cu privire la evaluarea siguranţei pe întreg teritoriul UE: Deţinătorul autorizaţiei de punere pe piaţă pentru medicamentul Numeta a identificat 14 raportări de cazuri de apariţie a hipermagneziemiei în asociere cu medicamentul Numeta G13%E. Concentraţiile serice ale magneziului au variat între 1,025mmol/l şi 1,5 mmol/l, fără raportare de semne clinice sau simptome în niciunul dintre cazuri. Aportul adecvat de magneziu administrat parenteral pentru nou-născuţii prematur nu este cunoscut. Cu toate acestea, ghiduri recunoscute pe scară largă 1,2 recomandă un aport de magneziu pe cale parenterală de 0,15-0,25mmol/kg/zi. Cantitatea totală autorizată de magneziu care se poate furniza nou-născuţilor prematur în timpul tratamentului cu Numeta G13%E este 0,55mmol/kg/zi, cantitate care depăşeşte doza recomandată. Compania deţinătoare a autorizaţiei a identificat un caz de hipermagneziemie apărută în asociere cu administrarea medicamentului Numeta G16%E. Această raportare a fost neclară, existând posibilitatea administrării de magneziu suplimentar. Conform informaţiilor despre medicament, cantitatea totală de magneziu care se poate furniza nou-născuţilor la termen în timpul tratamentului cu Numeta G16%E este de 0,3mmol/kg/zi. Deşi, în mare, această doză se încadrează în recomandările raportate din literatură, aceasta este totuşi uşor crescută faţă de doza sugerată de unele ghiduri recunoscute de tratament 1,2,3 (0,15-0,25 mmol/kg/zi şi 0,2mmol/kg/zi pentru nou-născuţii la termen până la vârsta de un an, 0,15-0,25 mmol/kg/zi şi 0,1mmol/kg/zi pentru copiii cu vârsta cuprinsă între 1 şi 2 ani). Referinţe: 1. Canada T, Crill C, Guenter P. A.S.P.E.N. Parenteral Nutrition Handbook. Silver Spring,Maryland: American Society for Parenteral and Enteral Nutrition. 2009; 167 5/7
6 2. Mirtallo et al. Safe Practices for Parenteral Nutrition JPEN 2004; 28: S 39 S Koletzko B, Goulet O, Hunt J, Krohn K, Shamir R. Guidelines on Paediatric Parenteral Nutrition of the European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN), and the European Society for Clinical Nutrition and Metabolism (ESPEN), Supported by the European Society of Paediatric Research (ESPR). J Pediatric Gastroenterology Nutrition 2005; 41:S1-S87. Informaţii suplimentare despre medicament: Medicamentele Numeta G13%E şi Numeta G16%E (glucoză, lipide, aminoacizi şi electroliţi) sunt soluţii pentru nutriţie parenterală. Nutriţia parenterală constă în furnizarea de substanţe nutritive şi lichide pe cale intravenoasă pacienţilor la care administrarea pe cale orală sau enterală (cu ajutorul unei sonde care ajunge direct în stomac) nu se poate utiliza. Nutriţia parenterală este necesară la nou-născuţii prematur şi, în unele cazuri, la copiii născuţi la termen, în scopul prevenirii unor complicaţii precum întârzieri de creştere şi complicaţii respiratorii şi pentru favorizarea dezvoltării normale a creierului. Medicamentele Numeta G13% E şi Numeta G16 E% sunt autorizate din 2011 prin procedură naţională, în următoarele state membre ale UE: Austria, Belgia, Republica Cehă, Danemarca, Finlanda, Franţa, Germania, Grecia, Irlanda, Italia, Luxemburg, Malta, Olanda, Norvegia, Polonia, Portugalia, Spania, Suedia, Marea Britanie. Informaţii suplimentare cu privire la procedura de evaluare: Reevaluarea medicamentelor Numeta G13%E şi Numeta G16%E a fost declanşată în data 13 iunie 2013, la cererea autorităţii competente în domeniul medicamentului din Suedia, conform prevederilor Articolului 107i al Directivei 2001/83/CE, cunoscut sub denumirea de Procedură de urgenţă la nivelul Uniunii. Reevaluarea a fost realizată de către Comitetul de farmacovigilenţă pentru evaluarea riscului (Pharmacovigilance Risk Assessment Committee = PRAC). 6/7
7 Deoarece evaluarea implică numai medicamente autorizate prin procedură naţională, recomandarea formulată de PRAC a fost înaintată Grupului de Coordonare pentru Procedurile de Recunoaştere Mutuală şi Descentralizată uman (Co-ordination Group for Mutual Recognition and Decentralised Procedures Human = CMDh), care a adoptat o decizie finală. CMDh este un organism de reglementare care reprezintă autorităţile naţionale de reglementare în domeniul medicamentului din statele membre ale Uniunii Europene. Deoarece opinia CMDh a fost adoptată prin consens, aceasta va fi implementată direct de către statele membre în care sunt autorizate medicamentele respective. Contactaţi ofiţerii de presă Monika Benstetter sau Martin Harvey Tel. +44 (0) press@ema.europa.eu 7/7
Anexa II Concluzii ştiinţifice şi motivele concluziilor 8
 Anexa II Concluzii ştiinţifice şi motivele concluziilor 8 Concluzii ştiinţifice şi motivele concluziilor După analiza recomandării PRAC din data de 5 septembrie 2013 cu privire la Numeta G13%E şi Numeta
Anexa II Concluzii ştiinţifice şi motivele concluziilor 8 Concluzii ştiinţifice şi motivele concluziilor După analiza recomandării PRAC din data de 5 septembrie 2013 cu privire la Numeta G13%E şi Numeta
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
Vokanamet, INN-canagliflozin-metformin
 ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
PRO_4804_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă d
 Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
Enurace Annexes I-II-III
 ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
FAQs as published on the web - EN version
 13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
Furosemide Vitabalans Annex I_II_ro
 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
COMISIA EUROPEANĂ Bruxelles, COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea
 COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
1
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2339/2010/04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Prismasol 2 mmol/l potasiu soluţie pentru hemofiltrare/hemodializă Clorură de calciu dihidrat/ Clorură
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2339/2010/04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Prismasol 2 mmol/l potasiu soluţie pentru hemofiltrare/hemodializă Clorură de calciu dihidrat/ Clorură
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
New product information wording - Dec RO
 17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6475/2014/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Aminoplasmal 100 g/l cu electroliţi solu
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6475/2014/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Aminoplasmal 100 g/l cu electroliţi soluţie perfuzabilă Aminoacizi şi electroliţi Citiţi cu
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6475/2014/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Aminoplasmal 100 g/l cu electroliţi soluţie perfuzabilă Aminoacizi şi electroliţi Citiţi cu
Furosemide Vitabalans Annex I_II_ro
 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui Rom
 ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui României Voturi valabil exprimate 156 66 64 169 16 noiembrie
ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui României Voturi valabil exprimate 156 66 64 169 16 noiembrie
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
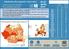 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a înc
 Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
EMA ENRO
 Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacog
 August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacogen (decitabină) 50 mg pulbere pentru concentrat pentru
August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacogen (decitabină) 50 mg pulbere pentru concentrat pentru
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI!
 Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
Anexe PO concurs
 B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1
 Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progeste
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
Microsoft Word - 1st year leaflet_ROM
 Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
Microsoft Word _Perfalgan 100ml_UK PIL_II-44+ UT.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
Cuprins Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac
 Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
C(2015)6507/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
PowerPoint-Präsentation
 Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
ETICHETAREA ENERGIEI ELECTRICE FURNIZATE CONSUMATORILOR
 DATE STATISTICE AFERENTE ENERGIEI ELECTRICE PRODUSE ÎN ANUL 2005 Pe baza declaraţiilor transmise de producătorii de energie electrică în luna ianuarie 2006, ANRE a elaborat o situaţie centralizată la nivelul
DATE STATISTICE AFERENTE ENERGIEI ELECTRICE PRODUSE ÎN ANUL 2005 Pe baza declaraţiilor transmise de producătorii de energie electrică în luna ianuarie 2006, ANRE a elaborat o situaţie centralizată la nivelul
LISTA angajaţilor ANMDM desemnaţi ca titulari sau înlocuitori în Consiliul de administraţie, comitetele ştiinţifice şi grupurile de lucru ale Agenţiei
 LISTA angajaţilor ANMDM desemnaţi ca titulari sau înlocuitori în Consiliul de administraţie, comitetele ştiinţifice şi grupurile de lucru ale Agenţiei Europene a Medicamentului (EMA), ale Şefilor Agenţiilor
LISTA angajaţilor ANMDM desemnaţi ca titulari sau înlocuitori în Consiliul de administraţie, comitetele ştiinţifice şi grupurile de lucru ale Agenţiei Europene a Medicamentului (EMA), ale Şefilor Agenţiilor
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara
 Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la
 Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea CE ESTE DMK 1.1
 https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
SPC in English
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1
 Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Проспект: Информация для пациента, потребителя
 Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Harmonised DHPC letter_BCR-ABLTKIs_HepBreactivation_19Feb2016_PRAC version
 Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
CUPRINS CHELTUIELILE TURISTICE ALE NEREZIDENŢILOR, ÎN ANUL A. Tabele referitoare la cheltuielile turistice ale nerezidenţilor cazaţi în structu
 CUPRINS CHELTUIELILE TURISTICE ALE NEREZIDENŢILOR, ÎN ANUL 2018 5 A. Tabele referitoare la cheltuielile turistice ale nerezidenţilor cazaţi în structurile de cazare turistică colective 1. Numărul nerezidenţilor,
CUPRINS CHELTUIELILE TURISTICE ALE NEREZIDENŢILOR, ÎN ANUL 2018 5 A. Tabele referitoare la cheltuielile turistice ale nerezidenţilor cazaţi în structurile de cazare turistică colective 1. Numărul nerezidenţilor,
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologie
 MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE Bine ați venit pe site-ul sondajului online Dedicated
 Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
PROSPECT: INFORMAŢII PENTRU UTILIZATOR
 PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu I. Contul cure
 Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu 15.07.2019 I. Contul curent standard A. SERVICII DE CONT CURENT CONTURI CURENTE
Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu 15.07.2019 I. Contul curent standard A. SERVICII DE CONT CURENT CONTURI CURENTE
Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LE
 Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LEGISLATIVE ACTS AND OTHER INSTRUMENTS: CORRIGENDUM/RECTIFICATIF
Council of the European Union Brussels, 9 September 2019 Interinstitutional File: 2005/0227 (COD) 10633/19 JUR 372 MI 538 ECO 72 SAN 317 CODEC 1263 LEGISLATIVE ACTS AND OTHER INSTRUMENTS: CORRIGENDUM/RECTIFICATIF
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR
 Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
Microsoft Word - pag3.doc
 ISSN-L: 2066-625x ISSN: 2065-8443 ROMÂNIA Institutul Naţional de Statistică Cheltuielile turistice ale nerezidenţilor în perioada 1.I 30.IX.2012 - Decembrie 2012 - CUPRINS Pag. CHELTUIELILE TURISTICE ALE
ISSN-L: 2066-625x ISSN: 2065-8443 ROMÂNIA Institutul Naţional de Statistică Cheltuielile turistice ale nerezidenţilor în perioada 1.I 30.IX.2012 - Decembrie 2012 - CUPRINS Pag. CHELTUIELILE TURISTICE ALE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
Protocol clinic naţional Diabetul zaharat, Chişinău 2017 Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evolu
 Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evoluţie cronică apărută prin alterarea secreţiei de insulină, care determină modificări majore în metabolismul glucozei
Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evoluţie cronică apărută prin alterarea secreţiei de insulină, care determină modificări majore în metabolismul glucozei
Lectia de economie. Derapaje fiscal bugetare majore in
 Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
Anexa nr
 Expunere de motive Secţiunea 1 Titlul proiectului de act normativ Lege privind aprobarea contribuției financiare anuale a României la bugetul Centrului European de Excelență pentru Combaterea Amenințărilor
Expunere de motive Secţiunea 1 Titlul proiectului de act normativ Lege privind aprobarea contribuției financiare anuale a României la bugetul Centrului European de Excelență pentru Combaterea Amenințărilor
Microsoft Word - anunt prealabil selectie 2018.doc
 INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
ANEXA nr
 ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunarea de Jos din Galati 1.2 Facultatea / Departamentul Medicina si Farmacie / Stiinte
ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunarea de Jos din Galati 1.2 Facultatea / Departamentul Medicina si Farmacie / Stiinte
Introducing high blood pressure RO.qxp:BPA
 Despre hipertensiunea arterială BLOOD PRESSURE UK Hipertensiunea arterială este cauza cea mai cunoscută ce provoacă invaliditate şi moarte prematură în Marea Britanie prin atac cerebral, infarct şi boli
Despre hipertensiunea arterială BLOOD PRESSURE UK Hipertensiunea arterială este cauza cea mai cunoscută ce provoacă invaliditate şi moarte prematură în Marea Britanie prin atac cerebral, infarct şi boli
CNAS
 FIŞĂ DE INIŢIERE A TRATAMENTULUI CU ORLISTATUM (XENICAL) PENTRU PACIENTUL CU TULBURĂRI DE NUTRIŢIE ŞI METABOLISM I. Date de identificare a. Numele şi prenumele pacientului Data naşterii (zi, luna, an)
FIŞĂ DE INIŢIERE A TRATAMENTULUI CU ORLISTATUM (XENICAL) PENTRU PACIENTUL CU TULBURĂRI DE NUTRIŢIE ŞI METABOLISM I. Date de identificare a. Numele şi prenumele pacientului Data naşterii (zi, luna, an)
PROSPECT: INFORMAŢII PENTRU UTILIZATOR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4037/2011/01-05 Anexa 1' 4038/2011/01-05 Prospect Prospect: Informaţii pentru utilizator rizatriptan Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4037/2011/01-05 Anexa 1' 4038/2011/01-05 Prospect Prospect: Informaţii pentru utilizator rizatriptan Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
Microsoft Word - Lansoprazole_Annex_I-III_ro
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/ Anexa /2012/ /2012/ Prospect Prospect: Informaţii pe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
Microsoft Word - aa00015-re02.ro05.doc
 NEGOCIERILE PENTRU ADERAREA BULGARIEI ŞI A ROMÂNIEI LA UNIUNEA EUROPEANĂ Bruxelles, 31 martie 2005 AA 15/2/05 REV 2 TRATATUL DE ADERARE: ACTUL DE ADERARE, ANEXA II PROIECTE DE ACTE LEGISLATIVE ŞI DE ALTE
NEGOCIERILE PENTRU ADERAREA BULGARIEI ŞI A ROMÂNIEI LA UNIUNEA EUROPEANĂ Bruxelles, 31 martie 2005 AA 15/2/05 REV 2 TRATATUL DE ADERARE: ACTUL DE ADERARE, ANEXA II PROIECTE DE ACTE LEGISLATIVE ŞI DE ALTE
Milnacipran Pierre Fabre Medicament, INN: milnacipran
 ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
ANEXA CONCLUZII ŞTIINŢIFICE ŞI MOTIVE ALE REFUZULUI PREZENTATE DE EMEA REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU MILNACIPRAN PIERRE FABRE MEDICAMENT Milnacipran Pierre Fabre Medicament conţine milnacipran,
31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de as
 31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de COMISIA COMUNITĂŢILOR EUROPENE având în vedere Tratatul
31999R1228 REGULAMENTUL COMISIEI (CE) nr. 1228/1999 din 28 mai 1999 privind seriile de date care trebuie furnizate pentru statistica serviciilor de COMISIA COMUNITĂŢILOR EUROPENE având în vedere Tratatul
REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate
 REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate CE SUNT REȚELELE EUROPENE DE REFERINȚĂ? Rețelele europene de referință (ERN) [European
REȚELELE EUROPENE DE REFERINȚĂ AJUTORAREA PACIENȚILOR CARE SUFERĂ DE BOLI RARE SAU COMPLEXE Share. Care. Cure. Sănătate CE SUNT REȚELELE EUROPENE DE REFERINȚĂ? Rețelele europene de referință (ERN) [European
EMA ENRO
 Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
PRO_4755_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
Microsoft Word - comunicat_ nr 126 turism_aprilie_2014.doc
 ROMÂNIA Biroul de presă B-dul Libertăţii nr.16, sector 5, Bucureşti Tel/Fax: 318 18 69; Fax 312 48 75 e-mail: romstat@insse.ro; biroupresa@insse.ro COMUNICAT DE PRESĂ Nr. 126 din 2 iunie Embargo ora 10.00
ROMÂNIA Biroul de presă B-dul Libertăţii nr.16, sector 5, Bucureşti Tel/Fax: 318 18 69; Fax 312 48 75 e-mail: romstat@insse.ro; biroupresa@insse.ro COMUNICAT DE PRESĂ Nr. 126 din 2 iunie Embargo ora 10.00
COM(2009)225/F1 - RO
 RO RO RO COMISIA COMUNITĂŢILOR EUROPENE Bruxelles, 15.5.2009 COM(2009) 225 final RAPORT AL COMISIEI de analizare a sancțiunilor prevăzute în legislația statelor membre pentru încălcările grave ale normelor
RO RO RO COMISIA COMUNITĂŢILOR EUROPENE Bruxelles, 15.5.2009 COM(2009) 225 final RAPORT AL COMISIEI de analizare a sancțiunilor prevăzute în legislația statelor membre pentru încălcările grave ale normelor
Microsoft Word - societatea informationala.doc
 I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2017/01-19 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Volulyte 6% soluţie perfuzabilă Hidroxieti
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10443/2017/01-19 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Volulyte 6% soluţie perfuzabilă Hidroxietil amidon (HES 130/0,4) în soluţie electrolitică izotonă
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10443/2017/01-19 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Volulyte 6% soluţie perfuzabilă Hidroxietil amidon (HES 130/0,4) în soluţie electrolitică izotonă
Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea CE
 https://www.printo.it/pediatric-rheumatology/ro/intro Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea 2016 1. CE ESTE PFAPA 1.1 Ce este această boală? Acronimul PFAPA
https://www.printo.it/pediatric-rheumatology/ro/intro Febra Periodică Asociată cu Stomatită Aftoasă, Faringită şi Adenită (PFAPA) Versiunea 2016 1. CE ESTE PFAPA 1.1 Ce este această boală? Acronimul PFAPA
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
eb76_3_parlemeter_report_ro
 Eurobarometru 76.3 Parlametru Realizat de TNS Opinion & Social la cererea Parlamentului European Sondaj coordonat de Direcţia Generală Comunicare CUPRINS INTRODUCERE...3 REZUMAT...5 I. INFORMAŢII PRIVIND
Eurobarometru 76.3 Parlametru Realizat de TNS Opinion & Social la cererea Parlamentului European Sondaj coordonat de Direcţia Generală Comunicare CUPRINS INTRODUCERE...3 REZUMAT...5 I. INFORMAŢII PRIVIND
INSMC ALESSANDRESCU RUSESCU organizează cu sprijinul NestleHealth Science cursul Monitorizarea în pediatrie între teorie și practică ediția a IIa Invi
 INSMC ALESSANDRESCU RUSESCU organizează cu sprijinul NestleHealth Science cursul Monitorizarea în pediatrie între teorie și practică ediția a IIa Invitație Stimați colegi, Vă invităm să participați la
INSMC ALESSANDRESCU RUSESCU organizează cu sprijinul NestleHealth Science cursul Monitorizarea în pediatrie între teorie și practică ediția a IIa Invitație Stimați colegi, Vă invităm să participați la
PRO_3712_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg co
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
ROMÂNIA Institutul Naţional de Statistică Frecventarea structurilor de primire turistică cu funcţiuni de cazare în trimestrul l mai 2019-
 ROMÂNIA Institutul Naţional de Statistică Frecventarea structurilor de primire turistică cu funcţiuni de cazare în trimestrul l 2019 - mai 2019- C U P R I N S Pagina Frecventarea structurilor de primire
ROMÂNIA Institutul Naţional de Statistică Frecventarea structurilor de primire turistică cu funcţiuni de cazare în trimestrul l 2019 - mai 2019- C U P R I N S Pagina Frecventarea structurilor de primire
Fişa de date Imprimantă HP Sprocket 200 Imprimi imediat fotografii de 5 x 7,6 cm (2 x 3 inchi) de la smartphone. Haide să imprimăm această petrecere.
 Fişa de date Imprimantă HP Sprocket 00 Imprimi imediat fotografii de 5 x 7,6 cm ( x 3 inchi) de la smartphone. Haide să imprimăm această petrecere. Partajează prezentul cu fotografii instantanee de 5 x
Fişa de date Imprimantă HP Sprocket 00 Imprimi imediat fotografii de 5 x 7,6 cm ( x 3 inchi) de la smartphone. Haide să imprimăm această petrecere. Partajează prezentul cu fotografii instantanee de 5 x
AUTORIZATIE DE PUNERE PE PIATA NR
 AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SE
 Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Academy of European Law PROCEDURILE DE SOLUŢIONARE A LITIGIILOR TRANSFRONTALIERE ÎN PRACTICĂ CREANŢELE AVÂND CA OBIECT PLATA UNEI SUME DE BANI ŞI E-JU
 Academy of European Law PROCEDURILE DE SOLUŢIONARE A LITIGIILOR TRANSFRONTALIERE ÎN PRACTICĂ CREANŢELE AVÂND CA OBIECT PLATA UNEI SUME DE BANI ŞI E-JUSTIŢIE LA NIVEL EUROPEAN 14-15 noiembrie 2013, Bucureşti
Academy of European Law PROCEDURILE DE SOLUŢIONARE A LITIGIILOR TRANSFRONTALIERE ÎN PRACTICĂ CREANŢELE AVÂND CA OBIECT PLATA UNEI SUME DE BANI ŞI E-JUSTIŢIE LA NIVEL EUROPEAN 14-15 noiembrie 2013, Bucureşti
ROMÂNIA Institutul Naţional de Statistică Cheltuielile turistice ale nerezidenţilor în trimestrul I Iunie
 ROMÂNIA Institutul Naţional de Statistică Celtuielile turistice ale nerezidenţilor în trimestrul I 2019 - Iunie 2019 - i CUPRINS CHELTUIELILE TURISTICE ALE NEREZIDENŢILOR ÎN TRIMESTRUL I 2019 5 A. Tabele
ROMÂNIA Institutul Naţional de Statistică Celtuielile turistice ale nerezidenţilor în trimestrul I 2019 - Iunie 2019 - i CUPRINS CHELTUIELILE TURISTICE ALE NEREZIDENŢILOR ÎN TRIMESTRUL I 2019 5 A. Tabele
Arterita Takayasu Arterita Takayasu Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 Arterita Takayasu
 Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin n
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
EllaOne,INN-ulipristal acetate
 Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZATIE DE PUNERE PE PIATA NR.3163/2003/01-02; 3164/2003/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALA A PRODUSULUI MEDICAMENTOS
AUTORIZATIE DE PUNERE PE PIATA NR.3163/2003/01-02; 3164/2003/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALA A PRODUSULUI MEDICAMENTOS
COM(2019)113/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 28.2.2019 COM(2019) 113 final RAPORT AL COMISIEI CĂTRE PARLAMENTUL EUROPEAN ȘI CONSILIU privind punerea în aplicare a Regulamentului (CE) nr. 450/2003 al Parlamentului European
COMISIA EUROPEANĂ Bruxelles, 28.2.2019 COM(2019) 113 final RAPORT AL COMISIEI CĂTRE PARLAMENTUL EUROPEAN ȘI CONSILIU privind punerea în aplicare a Regulamentului (CE) nr. 450/2003 al Parlamentului European
Microsoft Word - decizia docx
 1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pen
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pentru soluţie perfuzabilă Clorhidrat de irinotecan trihidrat
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pentru soluţie perfuzabilă Clorhidrat de irinotecan trihidrat
ACTIVITATEA DE TURISM ÎN ANUL 2000
 Nr. 4 2018 ACTIVITATEA DE TURISM ÎN ANUL 2018 ¾ ¾ În anul 2018 faġă de anul 2017, frecventarea structurilor de primire turistică cu funcġiuni de cazare se caracterizează prin creúterea capacităġii de cazare
Nr. 4 2018 ACTIVITATEA DE TURISM ÎN ANUL 2018 ¾ ¾ În anul 2018 faġă de anul 2017, frecventarea structurilor de primire turistică cu funcġiuni de cazare se caracterizează prin creúterea capacităġii de cazare
CASA DE ASIGURARI DE SANATATE NEAMT Anexa nr. 7 Cap. 7 : INGRIJIRI MEDICALELA DOMICILIU/ÎNGRIJIRI PALIATIVE LA DOMICILIU 7.1. SITUATIA CONTRACTELOR IN
 CASA DE ASIGURARI DE SANATATE NEAMT Anexa nr. 7 Cap. 7 : INGRIJIRI MEDICALELA DOMICILIU/ÎNGRIJIRI PALIATIVE LA DOMICILIU 7.1. SITUATIA CONTRACTELOR INCHEIATE INTRE CAS SI FURNIZORII DE SERVICII DE INGRIJIRI
CASA DE ASIGURARI DE SANATATE NEAMT Anexa nr. 7 Cap. 7 : INGRIJIRI MEDICALELA DOMICILIU/ÎNGRIJIRI PALIATIVE LA DOMICILIU 7.1. SITUATIA CONTRACTELOR INCHEIATE INTRE CAS SI FURNIZORII DE SERVICII DE INGRIJIRI
