Denumirea atribuită farmaceutică
|
|
|
- Victoria Ene
- 2 ani în urmă
- Vzualizari:
Transcriere
1 ANEXA I LISTA DENUMIRILOR, FORMELOR FARMACEUTICE, CONCENTRAŢIILOR PRODUSELOR MEDICINALE VETERINARE, SPECIILOR DE ANIMALE, CĂII DE ADMINISTRARE, TITULARILOR AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ DIN STATELE MEMBRE 1/55
2 Statul membru Deţinătorul autorizaţiei de comercializare Denumirea atribuită Forma farmaceutică Concentraţia Speciile de animale Calea de administrare Austria Novartis Animal Health GmbH., Biochemiestrasse 10, A-6250 Kundl Denagard Novartis 100 g/kg Arzneimittelvormischung zur Herstellung von Fütterungsarzneimitteln für Schweine Premix 100 g/kg Orală Belgia VMD nv Leo Aerden Hoge Mauw 900, 2370 Arendonk Denagard Novartis 20 g/kg Arzneimittelvormischung zur Herstellung von Fütterungsarzneimitteln für Schweine Tiamutin 20 g/kg Arzneimittelvormischung zur Herstellung von Fütterungsarzneimitteln für Schweine Tiamutin 10% gemedicineerd voormengsel 20 g/kg 20 g/kg Premix 100 mg/g Orală Cipru Republica Cehă Franţa Germania Novartis Animal Health Inc., Basel, Elveţia Novartis Animal Health d.o.o., Verovškova 57, Ljubljana, Slovenia Novartis Sante Animale 14 Boulevard Richelieu Rueil Malmaison Novartis Tiergesundheit GmbH Zielstattstr. 40, D München Denagard 10% Premix 100 mg/g Orală Tiamutin 10% ad us.vet. Tiamutin 2% ad us.vet. Denagard prémélange tiamuline 16.2 pneumonie volaille - porc Premix Premix 100 mg/1 g 20 mg/1 g 16,2 mg/g Pui Curcani Curcani Găini Denagard prémélange tiamuline 6.5 6,5 mg/g enterite porc enterocolite lapin Denagard 10% AMV Premix 100 g/kg Orală Orală Orală 2/55
3 Grecia Ungaria Irlanda Italia Letonia Lituania Portugalia Premier Shukuroglu Hellas SA Mesogion Av Holargos Grecia Novartis Animal Health d.o.o. Verovškova 57, 1000 Ljubljana, Slovenia Novartis Animal Health Ireland Ltd., Industrial park, Cork Road, Waterford Ireland Novartis Animal Health S.P.A Largo Umberto Boccioni, Origlio (Varese) Novartis Animal Health d.o.o. Verovškova 57, SI-1000 Ljubljana, Slovenia Novartis Animal Health d.o.o. Verovškova 57, SI-1000 Ljubljana, Slovenia Novartis Farma Produtos Farmacęuticos S.A Rua do Centro Empresarial Edifício 8 Quinta da Beloura Sintra Denagard 2% Denagard 10% Denagard 10 % gyógy A.U.V. Tiamutin 2% Tiamutin 80% Premix 20 mg/g 100 mg/g Orală Premix 100 mg/g Orală Premix 20 mg/g 800 mg/g Denagard 10% Premix Denagard 10% Premix Plus Premix 100 mg/g 100 mg/g ne Păsări de curte Orală ne Tiamutin 10% Premix 100 mg/g Orală Tiamutin 10% vaistinis premiksas kiaulėms Denagard 20 g/kg Denagard 100 g/kg Dynamutilin 100 g/kg Orală Premix 100 mg/g Orală Premix 20 g/kg 100 g/kg 100 g/kg ne Păsări de curte Orală Polonia Novartis Animal Health d.o.o. Verovškova 57, SI-1000 Ljubljana, Slovenia Tiamutin 10% premiks leczniczy dla świń Tiamutin 2% 20 mg/g premiks do Premix 100 mg/g Orală 3/55
4 sporządzania paszy leczniczej dla świń 20 mg/g România Novartis Animal Health d.o.o. Verovškova 57, SI-1000 Ljubljana, Slovenia Tiamutin 10% Premix pentru furaje medicamentate pentru porci Premix 100 mg/g Pui de carne Orală Slovacia Novartis Animal Health d.o.o. Verovškova 57, SI-1000 Ljubljana, Slovenia Tiamutin 80% coated Tiamutin 10% prm. ad us. vet. Tiamutin 2% prm. ad us. vet. Premix 800 g/100 kg 100 mg/g 20 mg/g Pui de găină Curcani Orală Spania Novartis Sanidad Animal SL c/de la Marina, Barcelona Spania Denagard 100g/kg Premezcla medicamentosa Premix 100g/kg Pui Curcani Orală Denagard 20g/kg Premezcla medicamentosa 20g/kg Suedia Olanda Novartis Healthcare A/S Animal Health Lyngbyvej 172 DK-2100 Köpenhamn Ö Danemarca Novartis Consumer health Claudius Prinsenlaan CP Breda, Olanda Dynamutilin 10% 100g/kg Pui Curcani Denagard vet. Premix 20 mg/g Orală Tiamutin 10% Denagard 2% Premix pentru furaje medicamentate 100 g/kg 20 g/kg Orală 4/55
5 Regatul Unit al Marii Britanii Novartis Animal Health UK Ltd. Frimley Business Park Frimely Camberley Surrey GU16 7SR Marea Britanie Denagard 2% w/w Denagard 80% w/w Denagard 10% w/w Premix 2 mg/g 800mg/g 100 mg/g Orală 5/55
6 ANEXA II CONCLUZII ŞTIINŢIFICE ŞI MOTIVE PENTRU MODIFICAREA REZUMATULUI CARACTERISTICILOR PRODUSULUI ŞI ETICHETĂRII 6/55
7 REZUMAT GENERAL AL EVALUĂRII ŞTIINŢIFICE PENTRU TIAMUTIN PREMIX ŞI DENUMIRILE ASOCIATE (a se vedea anexa I) 1. Introducere Premixurile cu tiamulină sunt comercializate în 20 de state membre ale Uniunii Europene sub o varietate de denumiri inventate (a se vedea anexa I). Formulele autorizate sunt pe bază de hidrogen fumarat de tiamulină într-o concentraţie de: 0,8%, 2%, 10% şi 80%. În Franţa, ul înregistrat de 0,65% se referă la tiamulină bază echivalentă cu un ce conţine 0,8% hidrogen fumarat de tiamulină, iar ul înregistrat de 1,62% se referă la tiamulină bază care este echivalentă cu un ce conţine 2,0% hidrogen fumarat de tiamulină. Animalele-ţintă sunt: porci pui de găină curci iepuri Anumite concentraţii ale acestor formule nu sunt în prezent autorizate în statele membre respective la anumite specii, de exemplu, concentraţia de 0,8% nu este autorizată la pui de găină şi curci, iar concentraţia de 80% nu este autorizată la iepuri. Având în vedere deciziile naţionale divergente luate de statele membre cu privire la autorizarea acestor produse, a fost sesizat în acest sens CVMP în temeiul articolului 34 alineatul (1) din Directiva 2001/82/CE, pentru a soluţiona divergenţele dintre Rezumatele caracteristicilor produsului (RCP) autorizate la nivel naţional în întreaga Uniune Europeană. Principalele secţiuni de dezacord din RCP-urile existente au fost: 1. indicaţii de utilizare; 2. cantităţi de administrat şi calea de administrare; 3. timp de aşteptare. 2. Dezbatere Deţinătorii autorizaţiilor de punere pe piaţă au fost invitaţi: 1. să furnizeze o listă exhaustivă a diferenţelor dintre RCP-urile produselor autorizate în statele membre; 2. să reexamineze toate secţiunile din RCP-uri şi să sugereze modificări corespunzătoare ale textului acolo unde există divergenţe, precum şi să propună Informaţii despre produs armonizate (RCP şi etichetarea), ţinând cont de cele mai recente ghiduri; 3. să prezinte date relevante disponibile, în special în sprijinul acestor Informaţii despre produs armonizate propuse, în legătură cu discrepanţele identificate mai sus. În ceea ce priveşte armonizarea indicaţiilor şi pe baza datelor de eficacitate prezentate, s-a convenit armonizarea indicaţiilor după cum urmează: : A fost acceptată utilizarea tiamutin şi denumirile asociate în tratamentul şi profilaxia dizenteriei porcine, tratamentul spirochetozei de colon porcine (colită) cauzate de Brachyspira pilosicoli, tratamentul enteropatiei proliferative porcine (ileită) cauzate de L. intracellularis şi tratamentul pneumoniei enzootice cauzate de M. hyopneumoniae. Nu a fost acceptată indicaţia la porci cu privire la utilizarea tiamutin şi denumirile asociate pentru profilaxia pneumoniei enzootice cauzate de M. hyopneumoniae. Pe baza datelor prezentate, nu se justifică posibilitatea utilizării tiamulinei în profilaxia pneumoniei enzootice. Nu ar fi conform cu recomandările de utilizare responsabilă (a se vedea, de asemenea, Codexul Cod de practică pentru reducerea la minimum şi limitarea rezistenţei antimicrobiene (CAC/RCP ), Orientările OIE pentru utilizarea responsabilă şi prudentă a agenţilor antimicrobieni în medicina 7/55
8 veterinară şi Federaţia Veterinarilor din Europa: Rezistenţa la antibiotice şi utilizarea prudentă a antibioticelor în medicina veterinară) să se utilizeze preventiv un antimicrobian doar dacă există un beneficiu direct în ceea ce priveşte un nivel redus de infecţie clinică şi/sau reducerea răspândirii infecţiei în cadrul turmei. De reţinut că deşi emergenţa rezistenţei antimicrobiene împotriva M. hyopneumoniae nu pare să fie de interes imediat, este necesar să se analizeze rezistenţa şi împotriva altor microbi prezenţi în turmele de porci precum B. hyodysenteriae. Pui (broileri, puicuţe de înlocuire, găini ouătoare şi de reproducţie): A fost acceptată utilizarea tiamutin şi denumirile asociate în tratamentul şi profilaxia bolii respiratorii cronice (BRC) cauzate de M. gallisepticum şi a saculitei aeriene şi sinovitei infecţioase cauzate de M. synoviae. Curci (pui tineri, curci de reproducţie): A fost acceptată utilizarea tiamutin şi denumirile asociate în tratamentul şi profilaxia sinuzitei infecţioase şi saculitei aeriene cauzate de M. gallisepticum, M. synoviae şi M. meleagridis. : A fost acceptată utilizarea tiamutin şi denumirile asociate în tratamentul enterocolitei epizootice la iepuri (ERE) şi profilaxia ERE în ferme cu semne clinice de ERE în ciclul de îngrăşare anterior ca parte a unui program ce include măsuri vizând eradicarea sau controlul infecţiei în cadrul fermei. Datorită variaţiei de posologie între Rezumatele caracteristicilor produsului (RCP) autorizate la nivel naţional, şi această problemă trebuia soluţionată în cadrul acestei proceduri de sesizare. Pentru fiecare indicaţie aprobată şi pe baza datelor prezentate, s-a convenit armonizarea cantităţilor de administrat pentru fiecare indicaţie aşa cum se arată în tabelele de mai jos. Referitor la timpul de aşteptare, a fost remarcată variaţia foarte mare a timpului de aşteptare aprobat în prezent (de exemplu, între 1 zi şi 20 de zile la porci, între 3 şi 8 zile la pui de găină şi curci, 0 zile la iepuri). În mod excepţional, în acest caz, CVMP a fost de acord cu timpii de aşteptare diferiţi propuşi la porci pentru indicaţiile de profilaxie şi tratament datorită dozajelor separate propuse şi pe baza datelor prezentate de deţinătorii autorizaţiilor de punere pe piaţă. Concluzie: După ce a analizat motivele sesizării şi răspunsurile prezentate de deţinătorii autorizaţiilor de punere pe piaţă, CVMP a ajuns la următoarea concluzie: Indicaţii de utilizare şi cantităţi de administrat şi calea de administrare Tratamentul dizenteriei porcine cauzate de B. hyodysenteriae, tratamentul spirochetozei de colon porcine (colită) cauzate de B. pilosicoli Dozaj: 5-10 mg hidrogen fumarat de tiamulină/kg de greutate corporală zilnic administrat timp de 7-10 zile consecutive. Dozajul se va obţine în mod normal printr-un nivel de includere de ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 8,0 12,5 25,0 kg 20,0 5,0 10,0 kg 100,0 1,0 2,0 kg 800,0 0,125 0,25 kg Profilaxia dizenteriei porcine cauzate de B. hyodysenteriae Dozaj: 2,0 mg hidrogen fumarat de tiamulină/kg de greutate corporală zilnic. Dozajul se va obţine în mod normal printr-un nivel de includere de 40 ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. Trebuie să se administreze tratament profilactic cu tiamulină timp de 2-4 săptămâni. 8/55
9 Tratamentul profilactic cu tiamulină trebuie iniţiat doar după confirmarea infecţiei cu B. hyodysenteriae şi apoi ca parte a unui program ce include măsuri vizând eradicarea sau controlul infecţiei în cadrul turmei. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 8,0 5,0 kg 20,0 2,0 kg 100,0 0,4 kg 800,0 0,05 kg Tratamentul enteropatiei proliferative porcine (ileită) cauzate de L. intracellularis Dozaj: 7,5 mg hidrogen fumarat de tiamulină/kg de greutate corporală zilnic administrat timp de zile consecutive. Dozajul se va obţine în mod normal printr-un nivel de includere de 150 ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 8,0 18,75 kg 20,0 7,5 kg 100,0 1,5 kg 800,0 0,188 kg Tratamentul pneumoniei enzootice cauzate de M. hyopneumoniae Dozaj: 5,0-10,0 mg hidrogen fumarat de tiamulină/kg de greutate corporală zilnic administrat timp de 7-10 zile consecutive. Dozajul se va obţine în mod normal printr-un nivel de includere de ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. Infecţia secundară cauzată de organisme precum Pasteurella multocida şi Actinobacillus pleuropneumoniae poate complica pneumonia enzootică şi poate necesita medicaţie specifică. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 8,0 12,5 25,0 kg 20,0 5,0 10,0 kg 100,0 1,0 2,0 kg 800,0 0,125 0,25 kg Pui (broileri, puicuţe de înlocuire, găini ouătoare şi de reproducţie) Tratamentul şi profilaxia bolii respiratorii cronice (BRC) cauzate de M. gallisepticum şi a saculitei aeriene şi sinovitei infecţioase cauzate de M. synoviae. Dozaj tratament şi profilaxie: 25 mg hidrogen fumarat de tiamulină/kg de greutate corporală administrat zilnic pe o perioadă de 3-5 zile consecutive. Acest dozaj se obţine în mod normal printrun nivel de includere de ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. În majoritatea cazurilor, vor fi necesare niveluri de includere din partea superioară a intervalului pentru a evita dozarea insuficientă. La păsările care cresc rapid, de exemplu, pui broiler, în primele 2-4 săptămâni de viaţă, nivelurile de includere din partea inferioară a intervalului pot fi suficiente. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 20,0 12,5 25,0 kg 100,0 2,5 5,0 kg 800,0 0,313 0,625 kg Curci (pui tineri, curci de reproducţie) Tratamentul şi profilaxia sinuzitei infecţioase şi saculitei aeriene cauzate de M. gallisepticum, M. synoviae şi M. meleagridis. Dozaj tratament şi profilaxie: 40 mg hidrogen fumarat de tiamulină/kg de greutate corporală administrat zilnic pe o perioadă de 3-5 zile consecutive. Acest dozaj se obţine în mod normal printrun nivel de includere de ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia 9/55
10 ca raţia de furaj să nu fie afectată. În majoritatea cazurilor, vor fi necesare niveluri de includere din partea superioară a intervalului pentru a evita dozarea insuficientă. La păsările care cresc rapid, de exemplu, puii de curcă, în primele 2-4 săptămâni de viaţă, nivelurile de includere din partea inferioară a intervalului pot fi suficiente. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 20,0 12,5 25,0 kg 100,0 2,5 5,0 kg 800,0 0,313 0,625 kg Tratamentul profilactic cu tiamulină trebuie iniţiat doar după confirmarea infecţiei cu M. gallisepticum, M. synoviae sau M. meleagridis şi apoi ca adjuvant în strategia profilactică pentru a reduce semnele clinice şi mortalitatea asociată bolii respiratorii la efectivele de păsări, unde infecţia in ovum este probabilă deoarece se cunoaşte existenţa bolii la generaţia părinte. Strategia profilactică trebuie să includă eforturi de eliminare a infecţiei în rândul generaţiei părinte. Tratamentul enterocolitei epizootice la iepuri (ERE) şi profilaxia ERE în ferme cu semne clinice de ERE în ciclul de îngrăşare anterior ca parte a unui program ce include măsuri vizând eradicarea sau controlul infecţiei în cadrul fermei. Dozaj: 3 mg hidrogen fumarat de tiamulină/kg de greutate corporală zilnic. Dozajul se va obţine în mod normal printr-un nivel de includere de 40 ppm hidrogen fumarat de tiamulină în furajele finite cu condiţia ca raţia de furaj să nu fie afectată. Tratamentul trebuie administrat până la 2-3 zile după dispariţia semnelor clinice. Tratamentul profilactic trebuie administrat timp de 3-4 săptămâni după prima săptămână post-înţărcare. Cantitate de hidrogen fumarat de Cantitate de formulă per tonă de furaj tiamulină (mg/g) per formulă 8,0 12,5 25,0 kg 20,0 5,0 10,0 kg 100,0 1,0 2,0 kg Timp de aşteptare Profilaxie (la 2,0 mg/kg greutate corporală): carne şi organe: 1 zi Tratament (la 5-10 mg/kg greutate corporală): carne şi organe: 6 zile Pui de găină Carne şi organe: 1 zi Ouă: 0 zile Curci Carne şi organe: 4 zile Carne şi organe: 0 zile În mod excepţional, în acest caz, CVMP a fost de acord cu timpii de aşteptare diferiţi propuşi la porci pentru indicaţiile de profilaxie şi tratament datorită dozajelor separate propuse şi pe baza datelor prezentate de deţinătorii autorizaţiilor de punere pe piaţă. 10/55
11 MOTIVE PENTRU MODIFICAREA REZUMATULUI CARACTERISTICILOR PRODUSULUI ŞI ETICHETĂRII Întrucât - CVMP a considerat că indicaţiile de utilizare trebuie armonizate pentru fiecare specie, dar că indicaţia ca tiamulina să fie utilizată în profilaxia pneumoniei enzootice nu poate fi acceptată pe baza datelor prezentate; - CVMP a considerat că pentru fiecare specie cantităţile de administrat şi calea de administrare trebuie armonizate; - CVMP a considerat că timpii de aşteptare trebuie armonizaţi pentru fiecare specie, după cum urmează: Profilaxie (la 2,0 mg/kg greutate corporală); carne şi organe: 1 zi Tratament (la 5-10 mg/kg greutate corporală); carne şi organe: 6 zile Pui de găină Carne şi organe: 1 zi Ouă: 0 zile Curci Carne şi organe: 4 zile Carne şi organe: 0 zile. În mod excepţional, în acest caz, CVMP a fost de acord cu timpii de aşteptare diferiţi propuşi la porci pentru indicaţiile de profilaxie şi tratament datorită dozajelor separate propuse şi pe baza datelor prezentate de deţinătorii autorizaţiilor de punere pe piaţă; - CVMP a considerat că RCP-ul trebuie armonizat în cadrul acestei proceduri de sesizare, remarcând totodată că anumite concentraţii ale formulelor nu sunt în prezent autorizate în statele membre la anumite specii, de exemplu, concentraţia de 0,8% nu este autorizată la pui de găină şi curci, iar concentraţia de 80% nu este autorizată la iepuri; CVMP a recomandat modificarea autorizaţiilor de punere pe piaţă pentru care Rezumatul caracteristicilor produsului şi etichetarea sunt prezentate în anexa III pentru Tiamutin şi denumirile asociate (a se vedea anexa I). Trebuie menţionate următoarele: concentraţia de 0,65% autorizată în prezent în Franţa este inclusă în RCP-ul/etichetarea pentru Premix 0,8% (0,65% tiamulină bază echivalează cu 0,8% hidrogen fumarat de tiamulină), iar concentraţia de 1,62% autorizată în prezent în Franţa este inclusă în RCP-ul/etichetarea pentru Premix 2% (1,62% tiamulină bază echivalează cu 2% hidrogen fumarat de tiamulină). 11/55
12 ANEXA III REZUMATUL CARACTERISTICILOR PRODUSULUI 12/55
13 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Premix pentru furaje medicamentate pentru porci şi iepuri 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Substanţa activă: Tiamulin hidrogen fumarat 8 mg/g În cazul ului 0,65% autorizat în Franța, acesta se refera la tiamulin baza echivalent cu ul conținând 0,8% tiamulin hidrogen fumarat, fiind acoperit de RCP/eticheta pentru ul 0,8%. Excipienţi: Pentru lista completă a excipienţilor, vezi secţiunea FORMA FARMACEUTICĂ Premix pentru furaje medicamentate 4. PARTICULARITĂŢI CLINICE 4.1 Specii ţintă 4.2 Indicaţii pentru utilizare, cu specificarea speciilor ţintă Pentru tratarea şi prevenirea dizenteriei porcine produse de Brachyspira hyodysenteriae Pentru tratarea colitei produse de Brachyspira pilosicoli Pentru tratarea ileitei produse de Lawsonia intracellularis Pentru tratarea pneumoniei enzootice produse de Mycoplasma hyopneumoniae Pentru tratarea şi prevenirea enterocolitei epizootice la iepuri (EEI) 4.3 Contraindicaţii Animalele nu trebuie să primească produse care conţin ionofori (monensin, narasin sau salinomicin) în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea Atenţionări speciale pentru fiecare specie ţintă În cazul unui consum redus de furaje, poate fi necesară creşterea nivelurilor de includere în furaje pentru a se obţine dozajul ţintă. Cazurile acute şi animalele grav bolnave, cu un consum redus de furaje, trebuie tratate cu un produs având o formulă potrivită, cum ar fi o soluţie injectabilă sau pe soluţie apoasă. 4.5 Precauţii speciale pentru utilizare Precauţii speciale pentru utilizare la animale Este foarte bine ca tratamentul să se bazeze în practică pe testarea sensibilităţii bacteriilor izolate de la animal. Dacă nu este posibil, tratamentul se va baza pe informaţiile epidemiologice locale (regionale, la nivel de fermă) despre sensibilitatea bacteriei ţintă. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea /55
14 Precauţii speciale care trebuie luate de persoana care administrează produsul medicinal veterinar la animale În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat, trebuie evitat contactul direct cu ochii, pielea şi mucoasele. În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat se va purta echipament personal de protecţie: salopete, mănuşi impermeabile şi fie o mască de unică folosinţă pentru respiraţie conform standardului european EN 149, fie un aparat respirator conform standardului european EN 140 cu filtru conform standardului european EN 143. Pielea contaminată se va spăla. În cazul unei ingerări accidentale, consultaţi imediat un medic şi arătaţi-i acestuia ambalajul sau eticheta. Persoanele cu hipersensibilitate cunoscută la tiamulin trebuie să administreze produsul cu precauţie. 4.6 Reacţii adverse (frecvenţă şi gravitate) Rareori pot să apară la porci eriteme sau edeme uşoare ale pielii, ca urmare a utilizării de tiamulin. 4.7 Utilizare în perioada de gestaţie, lactaţie sau în perioada de ouat Poate fi utilizat la porci în perioada de gestaţie şi lactaţie. Poate fi utilizat la iepuri în perioada de gestaţie şi lactaţie. 4.8 Interacţiune cu alte produse medicinale sau alte forme de interacţiune Tiamulin interacţionează cu ionofori ca monensin, salinomicin şi narasin şi pot apare semne nesesizabile de intoxicaţie cu ionofori. Animalele nu trebuie să primească produse care conţin monensin, narasin sau salinomicin în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Dacă apar semne de interacţiune, se va opri imediat administrarea furajelor contaminate. Acestea vor fi îndepărtate şi înlocuite cât mai curând posibil cu furaje proaspete, care nu conţin anticoccidienele monensin, salinomicin sau narasin. 4.9 Cantităţi de administrat şi calea de administrare Calculele pentru obţinerea dozei corecte şi a ratei de includere corecte trebuie efectuate conform formulei: - Rata de includere (ppm) = doză (mg/kg greutate corporală) x greutatea corporală (kg) / cantitatea de furaje consumată zilnic (kg) În vederea asigurării unui dozaj corect, greutatea corporală trebuie stabilită cât mai exact cu putinţă, pentru a se evita subdozajul. Consumul de furaje medicamentate depinde de starea clinică a animalelor. Pentru a obţine dozajul corect, concentraţia de tiamulin hidrogen fumarat trebuie ajustată corespunzător. Tratarea dizenteriei porcine produse de B. hyodysenteriae, tratarea spirochetozei de colon porcine (colită) produse de B. pilosicoli Dozaj: 5-10 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 8,0 12,5-25,0 kg Prevenirea dizenteriei porcine produse de B. hyodysenteriae Dozaj: 2,0 mg de tiamulin hidrogen fumarat /kg greutate corporală zilnic. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 40 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Medicaţia preventivă cu tiamulin trebuie administrată timp de 2-4 săptămâni. 14/55
15 Tratamentul preventiv cu tiamulin trebuie iniţiat doar după confirmarea infecţiei cu B. Hyodysenteriae şi apoi ca parte a unui program care include măsuri pentru eradicarea sau controlul infecţiei la nivelul turmei. 8,0 5,0 kg Tratarea enteropatiei proliferative porcine (ileită) produse de L. intracellularis Dozaj: 7,5 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 150 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 8,0 18,75 kg Tratarea pneumoniei enzootice produse de M. hyopneumoniae Dozaj: 5,0-10,0 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Infecţiile secundare cu microorganisme cum ar fi Pasteurella multocida şi Actinobacillus pleuropneumoniae pot complica pneumonia enzootică şi va fi necesară o medicaţie specifică. 8,0 12,5-25,0 kg Tratarea enterocolitei epizootice la iepuri (EEI) şi prevenirea EEI în fermele cu semne de EEI în ciclurile anterioare de îngrăşare ca parte a programului de măsuri pentru eradicarea sau controlul infecţiei în fermă. Dozaj: 3 mg de tiamulin hidrogen fumarat /kg greutate corporală. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 40 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Tratamentul va fi administrat încă 2-3 zile după dispariţia semnelor clinice. Tratamentul preventiv va fi administrat timp de 3-4 săptămâni din prima săptămână de la înţărcare. 8,0 5,0 kg 4.10 Supradozare (simptome, proceduri de urgenţă, antidoturi), după caz : Doze orale unice de 100 mg/kg greutate corporală la porci au cauzat hiperpnee şi disconfort abdominal. La 150 mg/kg nu s-au remarcat efecte SNC, cu excepţia sedării. La 55 mg/kg administrate timp de 14 zile, au apărut o salivare temporară şi o uşoară iritaţie gastrică. Nu a fost stabilită o doză minimă letală la porci. Dacă apar semne de intoxicaţie, opriţi imediat administrarea furajelor medicamentate, înlocuiţi-le cu furaje proaspete nemedicamentate şi aplicaţi tratament simptomatic, de susţinere Timp de aşteptare Prevenire (la 2,0 mg/kg greutate corporală): 1 (o) zi Tratament (la 5-10 mg/kg greutate corporală): 6 zile Carne şi organe: 0 zile 15/55
16 5. PROPRIETĂŢI FARMACOLOGICE Grupa farmacoterapeutică: antibacterian pentru uz sistemic Codul veterinar ATC: QJ 01 XQ Proprietăţi farmacodinamice Tiamulin este un antibiotic bacteriostatic semisintetic, care aparţine grupei pleuromutilinelor şi acţionează la nivel ribozomal pentru a inhiba sinteza proteică bacteriană. Tiamulin a demonstrat o activitate in vitro împotriva unui spectru larg de bacterii, inclusiv Brachyspira hyodysenteriae, Brachyspira pilosicoli, Lawsonia intracellularis şi Mycoplasma spp. Tiamulin este bacteriostatic în concentraţii terapeutice şi s-a demonstrat că acţionează la nivelul ribozomilor 70 S şi se leagă în principal de subunitatea 50 S şi posibil în subsidiar de locul în care subunităţile 50 S şi 30 S se unesc. Pare să inhibe producerea de proteine microbiene prin producerea de complexe de iniţiere inactive biochimic, care împiedică elongarea lanţului polipeptidic. Se consideră că mecanismele responsabile pentru dezvoltarea rezistenţei la clasa de antibiotice a pleuromutilinelor la Brachyspira spp. se bazează pe mutaţii la nivelul ribozomal ţintă. Rezistenţa relevantă clinic la tiamulin presupune combinaţii de mutaţii în jurul locului de legare a acestuia. Rezistenţa la tiamulin poate fi asociată cu sensibilitatea scăzută la alte pleuromutiline. 5.2 Particularităţi farmacocinetice Tiamulin este bine absorbit la porci (peste 90%) în urma administrării orale şi larg răspândit în corp. Ca urmare a administrării unei singure doze orale de 10 mg şi 25 mg de tiamulin/kg greutate corporală, C max a fost de 1,03 µg/ml şi respectiv 1,82 µg/ml la analiza microbiologică, iar T max a fost 2 ore pentru amândouă. S-a demonstrat că tiamulin se concentrează în plămân, un ţesut ţintă şi în ficat, unde este metabolizat şi excretat (70-85%) în bilă, restul fiind excretat prin rinichi (15-30%). Cantitatea de tiamulin care nu a fost absorbită sau metabolizată trece prin intestine în colon şi se concentrează acolo. Nu sunt disponibile date farmacocinetice la iepuri. 6. PARTICULARITĂŢI FARMACEUTICE 6.1 Lista excipienţilor Se va completa national 6.2 Incompatibilităţi Nu se cunosc 6.3 Perioadă de valabilitate Se va completa national 6.4 Precauţii speciale pentru depozitare Se va completa national 6.5 Natura şi compoziţia ambalajului primar Se va completa national 6.6 Precauţii speciale pentru eliminarea produselor medicinale veterinare neutilizate sau a deşeurilor provenite din utilizarea unor astfel de produse Orice produs neutilizat sau deşeu trebuie eliminat în conformitate cu cerinţele naţionale. 16/55
17 7. DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE Se va completa national 8. NUMĂRUL (NUMERELE) AUTORIZAŢIEI DE COMERCIALIZARE Se va completa national 9. DATA PRIMEI AUTORIZĂRI/REÎNNOIRII AUTORIZAŢIEI Se va completa national 10. DATA REVIZUIRII TEXTULUI Se va completa national Interdicţii pentru vânzare, eliberare şi/sau utilizare Nu este cazul. 17/55
18 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Se va completa national Premix pentru furaje medicamentate pentru porci, păsări de curte şi iepuri 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Substanţa activă: Tiamulin hidrogen fumarat 20,0 mg/g În cazul ului 1,62% autorizat în Franța, acesta se refera la tiamulin baza echivalent cu ul conținând 2% tiamulin hidrogen fumarat, fiind acoperit de RCP/eticheta pentru ul 2%. Excipienţi: Pentru lista completă a excipienţilor, vezi secţiunea FORMA FARMACEUTICĂ Premix pentru furaje medicamentate 4. PARTICULARITĂŢI CLINICE 4.1 Specii ţintă Păsări de curte - Pui (pui de carne, puicuţe de înlocuire, găini ouătoare/de prăsilă) - Curcani (pui (producători) şi de prăsilă) 4.2 Indicaţii pentru utilizare, cu specificarea speciilor ţintă Pentru tratarea şi prevenirea dizenteriei porcine produse de Brachyspira hyodysenteriae Pentru tratarea colitei produse de Brachyspira pilosicoli Pentru tratarea ileitei produse de Lawsonia intracellularis Pentru tratarea pneumoniei enzootice produse de Mycoplasma hyopneumoniae Pui Pentru tratarea şi prevenirea bolii respiratorii cronice (BRC) şi a aerosaculitei produse de Mycoplasma gallisepticum şi de Mycoplasma synoviae Curcani Pentru tratarea şi prevenirea sinuzitei infecţioase şi a aerosaculitei produse de Mycoplasma gallisepticum, de Mycoplasma meleagridis şi de Mycoplasma synoviae Pentru tratarea şi prevenirea enterocolitei epizootice la iepuri (EEI). 4.3 Contraindicaţii Animalele nu trebuie să primească produse care conţin ionofori (monensin, narasin sau salinomicin) în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea Atenţionări speciale pentru fiecare specie ţintă În cazul unui consum redus de furaje, poate fi necesară creşterea nivelurilor de includere în furaje pentru a se obţine dozajul ţintă. Cazurile acute şi animalele grav bolnave, cu un consum redus de 18/55
19 furaje, trebuie tratate cu un produs având o formulă potrivită, cum ar fi o soluţie injectabilă sau pe soluţie apoasă. 4.5 Precauţii speciale pentru utilizare Precauţii speciale pentru utilizare la animale Este foarte bine ca tratamentul să se bazeze în practică pe testarea sensibilităţii bacteriilor izolate de la animal. Dacă nu este posibil, tratamentul se va baza pe informaţiile epideimologice locale (regionale, la nivel de fermă) despre sensibilitatea bacteriei ţintă. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea 4.8 Precauţii speciale care trebuie luate de persoana care administrează produsul medicinal veterinar la animale În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat, trebuie evitat contactul direct cu ochii, pielea şi mucoasele. În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat se va purta echipament personal de protecţie: salopete, mănuşi impermeabile şi fie o mască de unică folosinţă pentru respiraţie conform standardului european EN 149, fie un aparat respirator conform standardului european EN 140 cu filtru conform standardului european EN 143. Pielea contaminată se va spăla. În cazul unei ingerări accidentale, consultaţi imediat un medic şi arătaţi-i acestuia ambalajul sau eticheta. Persoanele cu hipersensibilitate cunoscută la tiamulin trebuie să administreze produsul cu precauţie. 4.6 Reacţii adverse (frecvenţă şi gravitate) Rareori pot să apară la porci eriteme sau edeme uşoare ale pielii, ca urmare a utilizării de tiamulin. 4.7 Utilizare în perioada de gestaţie, lactaţie sau în perioada de ouat Poate fi utilizat la porci în perioada de gestaţie şi lactaţie. Poate fi utilizat la pui şi curcani în perioada de ouat. Poate fi utilizat la iepuri în perioada de gestaţie şi lactaţie. 4.8 Interacţiune cu alte produse medicinale sau alte forme de interacţiune Tiamulin interacţionează cu ionofori ca monensin, salinomicin şi narasin şi pot apare semne nesesizabile de intoxicaţie cu ionofori. Animalele nu trebuie să primească produse care conţin monensin, narasin sau salinomicin în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Dacă apar semne de interacţiune, se va opri imediat administrarea furajelor contaminate. Acestea vor fi îndepărtate şi înlocuite ât mai curând posibil cu furaje proaspete, care nu conţin anticoccidienele monensin, salinomicin sau narasin. 4.9 Cantităţi de administrat şi calea de administrare Calculele pentru obţinerea dozei corecte şi a ratei de includere corecte trebuie efectuate conform formulei: - Rata de includere (ppm) = doză (mg/kg greutate corporală) x greutatea corporală (kg) / cantitatea de furaje consumată zilnic (kg) În vederea asigurării unui dozaj corect, greutatea corporală trebuie stabilită cât mai exact cu putinţă, pentru a se evita subdozajul. Consumul de furaje medicamentate depinde de starea clinică a animalelor. Pentru a obţine dozajul corect, concentraţia de tiamulin hidrogen fumarat trebuie ajustată corespunzător. Tratarea dizenteriei porcine produse de B. hyodysenteriae, tratarea spirochetozei de colon porcine (colită) produse de B. pilosicoli 19/55
20 Dozaj: 5-10 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 20,0 5,0-10,0 kg Prevenirea dizenteriei porcine produse de B. hyodysenteriae Dozaj: 2,0 mg de tiamulin hidrogen fumarat /kg greutate corporală zilnic. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 40 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Medicaţia preventivă cu tiamulin trebuie administrată timp de 2-4 săptămâni. Tratamentul preventiv cu tiamulin trebuie iniţiat doar după confirmarea infecţiei cu B. hyodysenteriae şi apoi ca parte a unui program care include măsuri pentru eradicarea sau controlul infecţiei la nivelul turmei. 20,0 2,0 kg Tratarea enteropatiei proliferative porcine (ileită) produse de L. intracellularis Dozaj: 7,5 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 150 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 20,0 7,5 kg Tratarea pneumoniei enzootice produse de M. hyopneumoniae Dozaj: 5,0-10,0 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Infecţiile secundare cu microorganisme cum ar fi Pasteurella multocida şi Actinobacillus pleuropneumoniae pot complica pneumonia enzootică şi va fi necesară o medicaţie specifică. 20,0 5,0-10,0 kg Pui (pui de carne, puicuţe de înlocuire, găini ouătoare şi de prăsilă) Tratarea şi prevenirea bolii respiratorii cronice (BRC) produse de M. gallisepticum şi a aerosaculitei şi sinovitei infecţioase produse de M. synoviae. Dozaj Tratare şi prevenire: 25 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 3-5 zile consecutive. Acesta este obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de hrană. Nivelele ridicate de includere sunt necesare în majoritatea cazurilor pentru a evita subdozarea. La păsările cu creştere rapidă, de ex. puii de carne în primele 2-4 săptămâni de viaşă, pot fi suficiente nivelele joase de includere. 20,0 12,5-25,0 kg Curcani (pui tineri, curcani de prăsilă) Tratarea şi prevenirea sinuzitei infecţioase şi a aerosaculitei produse de M. gallisepticum, M. synoviae şi M. meleagridis. Dozaj Tratare şi prevenire: 40 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 3-5 zile consecutive. Acesta este obţinut în mod normal printr-un nivel 20/55
21 de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Nivelele ridicate de includere sunt necesare în majoritatea cazurilor pentru a evita subdozarea. La păsările cu creltere rapidă, de ex. puii în primele 2-4 săptămâni de viaţă, pot fi suficiente nivelele joase de includere. 20,0 12,5 25,0 kg Tratamentul preventiv cu tiamulin ar trebui iniţiat doar după confirmarea infecţiei cu M. gallisepticum, M. synoviae sau M. meleagridis şi apoi ca susţinere a strategiei de prevenire pentru reducerea semnelor clinice şi mortalităţii din cauze respiratorii în efectiv, unde infecţia in ovum este de aşteptat deoarece boala există la generaţia parentală. Strategia de prevenire trebuie să includă măsuri pentru eliminarea infecţiei la generaţia parentală. Tratarea şi prevenirea enterocolitei epizootice la iepuri (EEI) şi prevenirea EEI în fermele cu semne de EEI în ciclurile anterioare de îngrăşare ca parte a programului de măsuri pentru eradicarea sau controlul infecţiei în fermă. Dozaj: 3 mg de tiamulin hidrogen fumarat /kg greutate corporală. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 40 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Tratamentul va fi administrat încă 2-3 zile după dispariţia semnelor clinice. Tratamentul preventiv va fi administrat timp de 3-4 săptămâni din prima săptămână de la înţărcare. 20,0 2,0 kg 4.10 Supradozare (simptome, proceduri de urgenţă, antidoturi), după caz : Doze orale unice de 100 mg/kg greutate corporală la porci au cauzat hiperpnee şi disconfort abdominal. La 150 mg/kg nu s-au remarcat efecte SNC, cu excepţia sedării. La 55 mg/kg administrate timp de 14 zile, au apărut o salivare temporară şi o uşoară iritaţie gastrică. Nu a fost stabilită o doză minimă letală la porci. Păsări de curte: LD 5 pentru pui de găină este 1290 mg/kg, iar pentru curcani 840 mg/kg greutate corporală. Semnele clinice ale toxicităţii acute la puii de găină sunt vocalizarea, crampele clonice şi poziţia culcată laterală. La curcani, semnele de toxicitate acută includ crampe clonice, poziţia culcată laterală sau dorsală, salivare şi ptoză. Dacă apar semne de intoxicaţie, opriţi imediat administrarea furajelor medicamentate, înlocuiţi-le cu furaje proaspete nemedicamentate şi aplicaţi tratament simptomatic, de susţinere Timp de aşteptare Prevenire (la 2,0 mg/kg greutate corporală): 1 (o) zi Tratament (la 5-10 mg/kg greutate corporală): 6 zile Pui Carne şi organe: 1 (o) zi Ouă: 0 zile Curcani Carne şi organe: 4 zile Carne şi organe: 0 zile 5. PROPRIETĂŢI FARMACOLOGICE Grupa farmacoterapeutică: antibacterian pentru uz sistemic Codul veterinar ATC: QJ 01 XQ 01 21/55
22 5.1 Proprietăţi farmacodinamice Tiamulin este un antibiotic bacteriostatic semisintetic, care aparţine grupei pleuromutilinelor şi acţionează la nivel ribozomal pentru a inhiba sinteza proteică bacteriană. Tiamulin a demonstrat o activitate in vitro împotriva unui spectru larg de bacterii, inclusiv Brachyspira hyodysenteriae, Brachyspira pilosicoli, Lawsonia intracellularis şi Mycoplasma spp. Tiamulin este bacteriostatic în concentraţii terapeutice şi s-a demonstrat că acţionează la nivelul ribozomilor 70 S şi se leagă în principal de subunitatea 50 S şi posibil în subsidiar de locul în care subunităţile 50 S şi 30 S se unesc. Pare să inhibe producerea de proteine microbiene prin producerea de complexe de iniţiere inactive biochimic, care împiedică elongarea lanţului polipeptidic. Se consideră că mecanismele responsabile pentru dezvoltarea rezistenţei Brachyspira spp. la clasa de antibiotice a pleuromutilinelor se bazează pe mutaţii la nivelul ribozomal ţintă. Rezistenţa relevantă clinic la tiamulin presupune combinaţii de mutaţii în jurul locului de legare a acestuia. Rezistenţa la tiamulin poate fi asociată cu o sensibilitate scăzută la alte pluromutiline. 5.2 Particularităţi farmacocinetice Tiamulin este bine absorbit la porci (peste 90%) în urma administrării orale şi larg răspândit în corp. Ca urmare a administrării unei singure doze orale de 10 mg şi 25 mg de tiamulin/kg greutate corporală, C max a fost de 1,03 µg/ml şi respectiv 1,82 µg/ml la analiza microbiologică, iar T max a fost 2 ore pentru amândouă. S-a demonstrat că tiamulin se concentrează în plămân, un ţesut ţintă şi în ficat, unde este metabolizat şi excretat (70-85%) în bilă, restul fiind excretat prin rinichi (15-30%). Cantitatea de tiamulin care nu a fost absorbită sau metabolizată trece prin intestine în colon şi se concentrează acolo. Pui Tiamulin este bine absorbit la puii de găină (70-95%) după administrare orală Tiamulin are o răspândire largă în corp şi s-a demonstrat că acesta se concentrează în ficat şi rinichi (locurile de excreţie) şi în plămân (de 30 de ori mai mult decât nivelul seric). Excreţia are loc în principal prin bilă (55-65%) şi rinichi (15-30%) mai ales sub formă de metaboliţi inactivi din punct de vedere microbiologic şi este destul de rapidă, 99% din doză în 48 de ore. Curcani La curcani, nivelurile serice de tiamulin sunt similare cu cele de la pui. La cei de prăsilă la 0,025% tiamulin nivelul seric mediu a fost de 0,36 µg/ml (interval 0,22-0,5 µg/ml). Nu sunt disponibile date farmacocinetice la iepuri. 6. PARTICULARITĂŢI FARMACEUTICE 6.1 Lista excipienţilor 6.2 Incompatibilităţi Nu se cunosc 6.3 Perioadă de valabilitate 6.4 Precauţii speciale pentru depozitare 6.5 Natura şi compoziţia ambalajului primar 22/55
23 6.6 Precauţii speciale pentru eliminarea produselor medicinale veterinare neutilizate sau a deşeurilor provenite din utilizarea unor astfel de produse Orice produs neutilizat sau deşeu trebuie eliminat în conformitate cu cerinţele naţionale. 7. DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 8. NUMĂRUL (NUMERELE) AUTORIZAŢIEI DE COMERCIALIZARE 9. DATA PRIMEI AUTORIZĂRI/REÎNNOIRII AUTORIZAŢIEI 10. DATA REVIZUIRII TEXTULUI Interdicţii pentru vânzare, eliberare şi/sau utilizare Nu este cazul. 23/55
24 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Premix pentru furaje medicamentate pentru porci, păsări de curte şi iepuri 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Substanţa activă: Tiamulin hidrogen fumarat mg/g Excipienţi: Pentru lista completă a excipienţilor, vezi secţiunea FORMA FARMACEUTICĂ Premix pentru furaje medicamentate 4. PARTICULARITĂŢI CLINICE 4.1 Specii ţintă Păsări de curte - Pui (pui de carne, puicuţe de înlocuire, găini ouătoare/de prăsilă) - Curcani (pui (producători) şi de prăsilă) 4.2 Indicaţii pentru utilizare, cu specificarea speciilor ţintă Pentru tratarea şi prevenirea dizenteriei porcine produse de Brachyspira hyodysenteriae Pentru tratarea colitei produse de Brachyspira pilosicoli Pentru tratarea ileitei produse de Lawsonia intracellularis Pentru tratarea pneumoniei enzootice produse de Mycoplasma hyopneumoniae Pui Pentru tratarea şi prevenirea bolii respiratorii cronice (BRC) şi a aerosaculitei produse de Mycoplasma gallisepticum şi de Mycoplasma synoviae Curcani Pentru tratarea şi prevenirea sinuzitei infecţioase şi a aerosaculitei produse de Mycoplasma gallisepticum, de Mycoplasma meleagridis şi de Mycoplasma synoviae Pentru tratarea şi prevenirea enterocolitei epizootice la iepuri (EEI) 4.3 Contraindicaţii Animalele nu trebuie să primească produse care conţin ionofori (monensin, narasin sau salinomicin) în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea Atenţionări speciale pentru fiecare specie ţintă În cazul unui consum redus de furaje, poate fi necesară creşterea nivelurilor de includere în furaje pentru a se obţine dozajul ţintă. Cazurile acute şi animalele grav bolnave, cu un consum redus de furaje, trebuie tratate cu un produs având o formulă potrivită, cum ar fi o soluţie injectabilă sau pe soluţie apoasă. 24/55
25 4.5 Precauţii speciale pentru utilizare Precauţii speciale pentru utilizare la animale Este foarte bine ca tratamentul să se bazeze în practică pe testarea sensibilităţii bacteriilor izolate de la animal. Dacă nu este posibil, tratamentul se va baza pe informaţiile epidemiologice locale (regionale, la nivel de fermă) despre sensibilitatea bacteriei ţintă. Pentru informaţii privind interacţiunea dintre tiamulin şi ionofori, consultaţi secţiunea 4.8 Precauţii speciale care trebuie luate de persoana care administrează produsul medicinal veterinar la animale În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat trebuie evitat contactul direct cu ochii, pielea şi mucoasele. În timpul mixării produsului medicinal veterinar şi manipulării furajului medicamentat se va purta echipament personal de protecţie: salopete, mănuşi impermeabile şi fie o mască de unică folosinţă pentru respiraţie conform standardului european EN 149, fie un aparat respirator conform standardului european EN 140 cu filtru conform standardului european EN 143. Pielea contaminată se va spăla. În cazul unei ingerări accidentale, consultaţi imediat un medic şi arătaţi-i acestuia ambalajul sau eticheta. Persoanele cu hipersensibilitate cunoscută la tiamulin trebuie să administreze produsul cu precauţie. 4.6 Reacţii adverse (frecvenţă şi gravitate) Rareori pot să apară la porci eriteme sau edeme uşoare ale pielii, ca urmare a utilizării de tiamulin. 4.7 Utilizare în perioada de gestaţie, lactaţie sau în perioada de ouat Poate fi utilizat la porci în perioada de gestaţie şi lactaţie. Poate fi utilizat la pui şi curcani în perioada de ouat. Poate fi utilizat la iepuri în perioada de gestaţie şi lactaţie. 4.8 Interacţiune cu alte produse medicinale sau alte forme de interacţiune Tiamulin interacţionează cu ionofori ca monensin, salinomicin şi narasin şi pot apare semne nesesizabile de intoxicaţie cu ionofori. Animalele nu trebuie să primească produse care conţin monensin, narasin sau salinomicin în timpul tratamentului cu tiamulin sau timp de cel puţin şapte zile înainte sau după tratamentul cu tiamulin. Pot interveni încetinirea semnificativă a creşterii sau moartea. Dacă apar semne de interacţiune, se va opri imediat administrarea furajelor contaminate.acestea vor fi îndepărtate şi înlocuite cât mai curând posibil cu furaje proaspete, care nu conţin anticoccidienele monensin, salinomicin sau narasin. 4.9 Cantităţi de administrat şi calea de administrare Calculele pentru obţinerea dozei corecte şi a ratei de includere corecte trebuie efectuate conform formulei: - Rata de includere (ppm) = doză (mg/kg greutate corporală) x greutatea corporală (kg) / cantitatea de furaje consumată zilnic (kg) În vederea asigurării unui dozaj corect, greutatea corporală trebuie stabilită cât mai exact cu putinţă, pentru a se evita subdozajul. Consumul de furaje medicamentate depinde de starea clinică a animalelor. Pentru a obţine dozajul corect, concentraţia de tiamulin hidrogen fumarat trebuie ajustată corespunzător. Tratarea dizenteriei porcine produse de B. hyodysenteriae, tratarea spirochetozei de colon porcine (colită) produse de B. pilosicoli Dozaj: 5-10 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de /55
26 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 100,0 1,0-2,0 kg Prevenirea dizenteriei porcine produse de B. hyodysenteriae Dozaj: 2,0 mg de tiamulin hidrogen fumarat /kg greutate corporală zilnic. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 40 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Medicaţia preventivă cu tiamulin trebuie administrată timp de 2-4 săptămâni. Tratamentul preventiv cu tiamulin trebuie iniţiat doar după confirmarea infecţiei cu B. hyodysenteriae şi apoi ca parte a unui program care include măsuri pentru eradicarea sau controlul infecţiei la nivelul turmei. 100,0 0,4 kg Tratarea enteropatiei proliferative porcine (ileită) produse de L. intracellularis Dozaj: 7,5 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de 150 ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. 100,0 1,5 kg Tratarea pneumoniei enzootice produse de M. hyopneumoniae Dozaj: 5,0-10,0 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 7-10 zile consecutive. Dozajul va fi obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Infecţiile secundare cu microorganisme cum ar fi Pasteurella multocida şi Actinobacillus pleuropneumoniae pot complica pneumonia enzootică şi va fi necesară o medicaţie specifică. 100,0 1,0-2,0 kg Pui (pui de carne, puicuţe de înlocuire, găini ouătoare şi de prăsilă) Tratarea şi prevenirea bolii respiratorii cronice (BRC) produse de M. gallisepticum şi a aerosaculitei şi sinovitei infecţioase produse de M. synoviae. Dozaj Tratare şi prevenire: 25 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 3-5 zile consecutive. Acesta este obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de hrană. Nivelele ridicate de includere sunt necesare în majoritatea cazurilor pentru a evita subdozarea. La păsările cu creştere rapidă, de ex. puii de carne în primele 2-4 săptămâni de viaţă, pot fi suficiente nivelele joase de includere. 100,0 2,5-5,0 kg Curcani (pui tineri, curcani de prăsilă) Tratarea şi prevenirea sinuzitei infecţioase şi a aerosaculitei produse de M. gallisepticum, M. synoviae şi M. meleagridis. Dozaj Tratare şi prevenire: 40 mg de tiamulin hidrogen fumarat /kg greutate corporală administrat zilnic timp de 3-5 zile consecutive. Acesta este obţinut în mod normal printr-un nivel de includere de ppm de tiamulin hidrogen fumarat în furajele în stare finită, cu condiţia de a nu fi afectat consumul de furaje. Nivelele ridicate de includere sunt necesare în majoritatea 26/55
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
RESPIPORC FLUpan H1N1, INN: porcine influenza vaccine (inactivated)
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR RESPIPORC FLUpan H1N1, suspensie injectabilă, pentru porci 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare doză
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR RESPIPORC FLUpan H1N1, suspensie injectabilă, pentru porci 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare doză
Cytopoint, INN-lokivetmab
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR CYTOPOINT 10 mg soluție injectabilă pentru câini CYTOPOINT 20 mg soluție injectabilă pentru câini CYTOPOINT
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR CYTOPOINT 10 mg soluție injectabilă pentru câini CYTOPOINT 20 mg soluție injectabilă pentru câini CYTOPOINT
Furosemide Vitabalans Annex I_II_ro
 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Fevaxyn Pentofel
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Fevaxyn Pentofel, suspensie injectabilă pentru pisici 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ O doză de 1 ml
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Fevaxyn Pentofel, suspensie injectabilă pentru pisici 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ O doză de 1 ml
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
Enurace Annexes I-II-III
 ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
EMA ENRO
 Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Versican Plus L4, INN-Inactivated leptospira interrogans serovar bratislava,strain mslb1088/inactivated leptospira interrogans serovar canicola,strain
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Versican Plus L4, suspensie injectabilă, pentru câini 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare doză de
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Versican Plus L4, suspensie injectabilă, pentru câini 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare doză de
EMA ENRO
 Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COM
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI LOMEXIN 20 mg/g cremă 2. COMPOZIŢIA
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9429/2016/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI LOMEXIN 20 mg/g cremă 2. COMPOZIŢIA
Metacam, meloxicam
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Metacam 5 mg/ml, soluţie injectabilă pentru bovine şi porcine 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Un ml
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Metacam 5 mg/ml, soluţie injectabilă pentru bovine şi porcine 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Un ml
Furosemide Vitabalans Annex I_II_ro
 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
SPC in English
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COM
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Quality Review of Documents human product information template version 8 clean
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10459/2017/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI ACEVIREX 50 mg/g cremă
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10459/2017/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI ACEVIREX 50 mg/g cremă
Posatex, INN-Posaconazole, Orbifloxacin, Mometasone furoate
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Posatex picaturi auriculare pentru câini. 2. COMPOZITIA CALITATIVA ŞI CANTITATIVĂ Substanţe active Orbifloxacin
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Posatex picaturi auriculare pentru câini. 2. COMPOZITIA CALITATIVA ŞI CANTITATIVĂ Substanţe active Orbifloxacin
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
Purevax RCPCh FeLV, INN-FHV F2 strain+FCV 431 and G1 strains+905 strain+PLI IV+vCP97
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Purevax RCPCh FeLV liofilizat şi solvent pentru suspensie injectabilă. 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Purevax RCPCh FeLV liofilizat şi solvent pentru suspensie injectabilă. 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
Microsoft Word - Lansoprazole_Annex_I-III_ro
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologie
 MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
Equilis StrepE
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Equilis StrepE, liofilizat și solvent pentru suspensie injectabilă, la cai 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Equilis StrepE, liofilizat și solvent pentru suspensie injectabilă, la cai 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
Data revizuirii: Revizuire: 4 Înlocuieşte data: FIŞA CU DATE DE SECURITATE INSULCAST RTVS Part B SECŢIUNEA 1: Identificar
 FIŞA CU DATE DE SECURITATE SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului Numele produsului 1.2. Utilizări relevante identificate
FIŞA CU DATE DE SECURITATE SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului Numele produsului 1.2. Utilizări relevante identificate
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă d
 Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
FISA CU DATE DE SECURITATE BREEZE LEMON Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substan
 Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substantei/amestecului si a societatii/întreprinderii 1.1. Element de identificare a produsului Nume
Pagina: 1 Data completarii: 01/08/2008 Revizuire: 08/02/2012 Nr. revizie: 3 Sectiunea 1: Identificarea substantei/amestecului si a societatii/întreprinderii 1.1. Element de identificare a produsului Nume
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
AM_Ple_LegReport
 7.3.2016 A8-0046/313 313 Merja Kyllönen, Stefan Eck, Miguel Viegas, João Ferreira, João Pimenta Lopes, Marina Albiol Guzmán, Kostas Chrysogonos, Tania González Peñas, Miguel Urbán Crespo, Lola Sánchez
7.3.2016 A8-0046/313 313 Merja Kyllönen, Stefan Eck, Miguel Viegas, João Ferreira, João Pimenta Lopes, Marina Albiol Guzmán, Kostas Chrysogonos, Tania González Peñas, Miguel Urbán Crespo, Lola Sánchez
RCP_4839_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DOXIUM 500 mg capsule 2.
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7409/2006/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DOXIUM 500 mg capsule 2.
EllaOne,INN-ulipristal acetate
 Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Bravecto, INN-Fluralaner
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Bravecto 112.5 mg tablete masticabile pentru câini de talie foarte mică (2-4.5 kg) Bravecto 250 mg tablete masticabile
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Bravecto 112.5 mg tablete masticabile pentru câini de talie foarte mică (2-4.5 kg) Bravecto 250 mg tablete masticabile
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZATIE DE PUNERE PE PIATĂ NR. 5830/2005/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS IMODIUM 2. COMPOZITIA
AUTORIZATIE DE PUNERE PE PIATĂ NR. 5830/2005/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS IMODIUM 2. COMPOZITIA
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
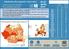 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Microsoft Word _iul_Marti_Radu_ro.doc
 UNIVERSITATEA DE ŞTIINŢE AGRICOLE ŞI MEDICINĂ VETERINARĂ ION IONESCU DE LA BRAD - IAŞI FACULTATEA DE ZOOTEHNIE DOMENIUL: ZOOTEHNIE SPECIALIZAREA: TEHNOLOGIA EXPLOATĂRII PĂSĂRILOR ŞI ANIMALELOR DE BLANĂ
UNIVERSITATEA DE ŞTIINŢE AGRICOLE ŞI MEDICINĂ VETERINARĂ ION IONESCU DE LA BRAD - IAŞI FACULTATEA DE ZOOTEHNIE DOMENIUL: ZOOTEHNIE SPECIALIZAREA: TEHNOLOGIA EXPLOATĂRII PĂSĂRILOR ŞI ANIMALELOR DE BLANĂ
Innovax-ND-IBD
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Innovax-ND-IBD suspensie şi solvent pentru suspensie injectabila pentru pui 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Innovax-ND-IBD suspensie şi solvent pentru suspensie injectabila pentru pui 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
Microsoft Word _Perfalgan 100ml_UK PIL_II-44+ UT.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
FISA CU DATE DE SECURITATE conf Regulament CE nr 1907/2006 COMPO Granule contra cartitelor Reg.. Nr.: N Cod art Ver. 1 0 Rev:
 FISA CU DATE DE SECURITATE conf Regulament CE nr 1907/2006 COMPO Granule contra cartitelor Reg.. Nr. N-18429 Cod art. 16707 Ver. 1 0 Rev 11.08.2011 Identificarea substantei/preparatului si a producatorului
FISA CU DATE DE SECURITATE conf Regulament CE nr 1907/2006 COMPO Granule contra cartitelor Reg.. Nr. N-18429 Cod art. 16707 Ver. 1 0 Rev 11.08.2011 Identificarea substantei/preparatului si a producatorului
Suprelorin; INN: deslorelin (as deslorelin acetate)
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Suprelorin 4,7 mg implant pentru câini 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Substanţă activă: 4,7 mg deslorelin
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Suprelorin 4,7 mg implant pentru câini 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Substanţă activă: 4,7 mg deslorelin
FISE TEHNICE DE SECURITATE LTP MATTSTONE H20 Capitol 1: Identificare 1.1. Identificare produs Nume: LTP MATTSTONE H Recomandari si restrictii l
 Capitol 1: Identificare 1.1. Identificare produs Nume: 1.2. Recomandari si restrictii la utilizare Utilizare: industriala si profesionala. Impermeabilizant pentru piatra naturala si alte tipuri de suprafete.
Capitol 1: Identificare 1.1. Identificare produs Nume: 1.2. Recomandari si restrictii la utilizare Utilizare: industriala si profesionala. Impermeabilizant pentru piatra naturala si alte tipuri de suprafete.
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3213/2011/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3213/2011/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS
Microsoft Word - societatea informationala.doc
 I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
Cuprins Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac
 Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Microsoft Word - Brodibleu_ro
 Fişa de siguranţă (rev. 2.0 30 septembrie 2007) 1. 1. PRODUSUL CHIMIC ŞI IDENTIFICAREA COMPANIEI 1.1 Identificarea produsului Denumirea comerciala: BRODIBLEU Nr. de înregistrare la Ministerul Sănătăţii
Fişa de siguranţă (rev. 2.0 30 septembrie 2007) 1. 1. PRODUSUL CHIMIC ŞI IDENTIFICAREA COMPANIEI 1.1 Identificarea produsului Denumirea comerciala: BRODIBLEU Nr. de înregistrare la Ministerul Sănătăţii
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
BROILER Obiective de performanţă An Aviagen Brand
 BROILER Obiective de performanţă 08 An Aviagen Brand BROILER ROSS 308: Obiective de performanţă Introducere Această broșură conține Obiective de Performanță pentru broiler Ross 308 și trebuie folosit împreună
BROILER Obiective de performanţă 08 An Aviagen Brand BROILER ROSS 308: Obiective de performanţă Introducere Această broșură conține Obiective de Performanță pentru broiler Ross 308 și trebuie folosit împreună
RO Jurnalul Oficial al Uniunii Europene L 280/5 REGULAMENTUL (CE) NR. 1237/2007 AL COMISIEI din 23 octombrie 2007 de modificare a Regulamen
 24.10.2007 Jurnalul Oficial al Uniunii Europene L 280/5 REGULAMENTUL (CE) NR. 1237/2007 AL COMISIEI din 23 octombrie 2007 de modificare a Regulamentului (CE) nr. 2160/2003 al Parlamentului European și
24.10.2007 Jurnalul Oficial al Uniunii Europene L 280/5 REGULAMENTUL (CE) NR. 1237/2007 AL COMISIEI din 23 octombrie 2007 de modificare a Regulamentului (CE) nr. 2160/2003 al Parlamentului European și
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la
 Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1
 Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Harmonised DHPC letter_BCR-ABLTKIs_HepBreactivation_19Feb2016_PRAC version
 Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
RCP_5701_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5701/2013/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Nitroxolin-MIP 250 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5701/2013/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Nitroxolin-MIP 250 mg
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
Microsoft Word - RO_EMEA
 ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
C(2015)6507/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
PRO_4804_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
COMISIA EUROPEANĂ Bruxelles, COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea
 COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1604/2009/01 Anexa 2 Rezumatul Caracteristicilor Produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Haemocomplettan P 1 g pulbere
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1604/2009/01 Anexa 2 Rezumatul Caracteristicilor Produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Haemocomplettan P 1 g pulbere
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a înc
 Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara
 Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Studiu privind dezvoltarea unei mici afaceri de crestere a prepelitelor 1
 Studiu privind dezvoltarea unei mici afaceri de crestere a prepelitelor http://proability.md/ro/ 1 Desfasurarea afacerii - efectivului initial 500 capete. Investitia initiala 15 350 lei Creşterea prepeliţelor
Studiu privind dezvoltarea unei mici afaceri de crestere a prepelitelor http://proability.md/ro/ 1 Desfasurarea afacerii - efectivului initial 500 capete. Investitia initiala 15 350 lei Creşterea prepeliţelor
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
Data revizuirii: Revizuire: 8 Înlocuieşte data: FIŞA CU DATE DE SECURITATE MA420/920/1020 EU ACTIVATOR Regulamentul Comisiei (UE
 FIŞA CU DATE DE SECURITATE Regulamentul Comisiei (UE) Nr. 2015/830 din 28 mai 2015. SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului
FIŞA CU DATE DE SECURITATE Regulamentul Comisiei (UE) Nr. 2015/830 din 28 mai 2015. SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului
Act LexBrowser
 MINISTERUL SĂNĂTĂŢII Nr. 10 din 8 ianuarie 2010 MINISTERUL MEDIULUI ŞI PĂDURILOR Nr. 368 din 17 martie 2010 AUTORITATEA NAŢIONALĂ SANITARĂ VETERINARĂ ŞI PENTRU SIGURANŢA ALIMENTELOR Nr. 11 din 4 martie
MINISTERUL SĂNĂTĂŢII Nr. 10 din 8 ianuarie 2010 MINISTERUL MEDIULUI ŞI PĂDURILOR Nr. 368 din 17 martie 2010 AUTORITATEA NAŢIONALĂ SANITARĂ VETERINARĂ ŞI PENTRU SIGURANŢA ALIMENTELOR Nr. 11 din 4 martie
PowerPoint-Präsentation
 Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
Creditarea companiilor evoluţii şi provocări Cristian Sporis, Vicepreşedinte Raiffeisen Bank Iulie 19 1 Reducere amplă a intermedierii financiare bancare în ţările membre UE 3 4 18 Soldul creditelor acordate
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacog
 August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacogen (decitabină) 50 mg pulbere pentru concentrat pentru
August 2017 COMUNICARE DIRECTĂ CĂTRE PROFESIONIȘTII DIN DOMENIUL SĂNĂTĂȚII Modificarea recomandărilor privind diluarea soluției reconstituite de Dacogen (decitabină) 50 mg pulbere pentru concentrat pentru
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progeste
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
ANEXA nr
 ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galaţi 1.2 Facultatea / Departamentul Medicină şi Farmacie / Ştiinţe
ANEXA nr. 3 la metodologie FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galaţi 1.2 Facultatea / Departamentul Medicină şi Farmacie / Ştiinţe
Apoquel, INN-oclacitinib maleate
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Apoquel 3,6 mg, comprimate filmate pentru câini Apoquel 5,4 mg, comprimate filmate pentru câini Apoquel 16 mg,
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA PRODUSULUI MEDICINAL VETERINAR Apoquel 3,6 mg, comprimate filmate pentru câini Apoquel 5,4 mg, comprimate filmate pentru câini Apoquel 16 mg,
SANTE/12376/2015-EN
 Consiliul Uniunii Europene Bruxelles, 24 aprilie 2017 (OR. en) 8318/17 AGRILEG 82 NOTĂ DE ÎNSOȚIRE Sursă: Comisia Europeană Data primirii: 19 aprilie 2017 Destinatar: Nr. doc. Csie: D046260/03 Subiect:
Consiliul Uniunii Europene Bruxelles, 24 aprilie 2017 (OR. en) 8318/17 AGRILEG 82 NOTĂ DE ÎNSOȚIRE Sursă: Comisia Europeană Data primirii: 19 aprilie 2017 Destinatar: Nr. doc. Csie: D046260/03 Subiect:
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZATIE DE PUNERE PE PIATA NR.3163/2003/01-02; 3164/2003/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALA A PRODUSULUI MEDICAMENTOS
AUTORIZATIE DE PUNERE PE PIATA NR.3163/2003/01-02; 3164/2003/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALA A PRODUSULUI MEDICAMENTOS
RCP_5988_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5988/2013/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Cicatrol 10 mg/g pastă
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5988/2013/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Cicatrol 10 mg/g pastă
PRO_3425_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
Studiu privind dezvoltarea unei mici afaceri de crestere a iepurilor 1
 Studiu privind dezvoltarea unei mici afaceri de crestere a iepurilor http://proability.md/ro/ 1 Desfasurarea afacerii - efectivului initial 15 femele si 1 mascul. Investitia initiala- 28 250 lei In urma
Studiu privind dezvoltarea unei mici afaceri de crestere a iepurilor http://proability.md/ro/ 1 Desfasurarea afacerii - efectivului initial 15 femele si 1 mascul. Investitia initiala- 28 250 lei In urma
PRO_671_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
R4BP 3 Print out
 Rezumatul caracteristicilor produsului pentru un produs biocid Denumirea produsului: Ratimor granule Tipul (tipurile) de produs (produse): TP - Rodenticide Numărul curent: RO0007MRA UK-0-0658 Numărul curent
Rezumatul caracteristicilor produsului pentru un produs biocid Denumirea produsului: Ratimor granule Tipul (tipurile) de produs (produse): TP - Rodenticide Numărul curent: RO0007MRA UK-0-0658 Numărul curent
Data revizuirii: Revizuire: 2 Înlocuieşte data: FIŞA CU DATE DE SECURITATE MA320 White/MA550 EU Activator Regulamentul Comisiei
 FIŞA CU DATE DE SECURITATE Regulamentul Comisiei (UE) Nr. 2015/830 din 28 mai 2015. SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului
FIŞA CU DATE DE SECURITATE Regulamentul Comisiei (UE) Nr. 2015/830 din 28 mai 2015. SECŢIUNEA 1: Identificarea substanţei/amestecului şi a societăţii/întreprinderii 1.1. Element de identificare a produsului
UNIVERSITATEA DE ŞTIINŢE AGRONOMICE Şl MEDICINĂ VETERINARĂ BUCUREŞTI FACULTATEA DE AGRICULTURĂ TEZĂ DE DOCTORAT CERCETĂRI PRIVIND UTILIZAREA DE TEHNIC
 UNIVERSITATEA DE ŞTIINŢE AGRONOMICE Şl MEDICINĂ VETERINARĂ BUCUREŞTI FACULTATEA DE AGRICULTURĂ TEZĂ DE DOCTORAT CERCETĂRI PRIVIND UTILIZAREA DE TEHNICI ECOLOGICE ÎN VEDEREA CREŞTERII CONSERVABILITĂŢII
UNIVERSITATEA DE ŞTIINŢE AGRONOMICE Şl MEDICINĂ VETERINARĂ BUCUREŞTI FACULTATEA DE AGRICULTURĂ TEZĂ DE DOCTORAT CERCETĂRI PRIVIND UTILIZAREA DE TEHNICI ECOLOGICE ÎN VEDEREA CREŞTERII CONSERVABILITĂŢII
FIȘĂ CU DATE DE SIGURANȚĂ pagina 1/5 SHOFU BLOCK HC SHOFU DISK HC Dată imprimare: 5 ianuarie 2017 SECȚIUNEA 1. Identificarea substanței/amestecului și
 pagina 1/5 SECȚIUNEA 1. Identificarea substanței/amestecului și a companiei/întreprinderii (Cont. de la pagina0) 1.1 Identificator produs Denumire comercială: / 1.2 Utilizări relevante identificate ale
pagina 1/5 SECȚIUNEA 1. Identificarea substanței/amestecului și a companiei/întreprinderii (Cont. de la pagina0) 1.1 Identificator produs Denumire comercială: / 1.2 Utilizări relevante identificate ale
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2018/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10957/2018/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DUAC 10 mg/g + 30 mg/g
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10957/2018/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI DUAC 10 mg/g + 30 mg/g
RCP_870_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 870/2008/01 Anexa 2` Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mucosolvan Junior 15 mg/5
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 870/2008/01 Anexa 2` Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mucosolvan Junior 15 mg/5
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui Rom
 ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui României Voturi valabil exprimate 156 66 64 169 16 noiembrie
ROMÂNIA BIROUL ELECTORAL CENTRAL Afganistan Africa de Sud Albania Algeria Arabia Saudita Argentina Ţara A TOTAL STRĂINĂTATE Alegerea Preşedintelui României Voturi valabil exprimate 156 66 64 169 16 noiembrie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2018/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefixim
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
Microsoft Word - 663E5DA5.doc
 Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
st00TSCG26.ro12
 Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
ANEXA II
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7319/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI SALOFALK, 4 g/60 ml, suspensie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7319/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI SALOFALK, 4 g/60 ml, suspensie
Anexa 2 ANALIZA DE HAZARD ÎN DOMENIUL SANITAR VETERINAR ȘI PENTRU SIGURANȚA ALIMENTELOR 1. DEFINIŢIE Conform IEC/ISO Ghid 73 Managementul Riscului Voc
 Anexa 2 ANALIZA DE HAZARD ÎN DOMENIUL SANITAR VETERINAR ȘI PENTRU SIGURANȚA ALIMENTELOR 1. DEFINIŢIE Conform IEC/ISO Ghid 73 Managementul Riscului Vocabular, 2009 hazard = sursă potenţială de daună/vătămare,
Anexa 2 ANALIZA DE HAZARD ÎN DOMENIUL SANITAR VETERINAR ȘI PENTRU SIGURANȚA ALIMENTELOR 1. DEFINIŢIE Conform IEC/ISO Ghid 73 Managementul Riscului Vocabular, 2009 hazard = sursă potenţială de daună/vătămare,
PRO_3712_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
Lectia de economie. Derapaje fiscal bugetare majore in
 Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
