PRO_7051_ doc
|
|
|
- Emanuil Stoica
- 4 ani în urmă
- Vzualizari:
Transcriere
1 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7051/2014/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere de inhalat Budesonidă/Fumarat de formoterol dihidrat Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament deoarece conţine informaţii importante pentru dumneavoastră. - Păstraţi acest prospect. S-ar putea să fie necesar să-l recitiţi. - Dacă aveţi orice întrebări suplimentare, adresaţi-vă medicului dumneavoastră sau farmacistului. - Acest medicament a fost prescris numai pentru dumneavoastră. Nu trebuie să-l daţi altor persoane. Le poate face rău, chiar dacă au aceleaşi semne de boală ca dumneavoastră. - Dacă manifestaţi orice reacţii adverse, adresaţi-vă medicului dumneavoastră sau farmacistului. Acestea includ orice posibile reacţii adverse nemenţionate în acest prospect. Vezi pct. 4. Ce găsiţi în acest prospect: 1. Ce este Symbicort Turbuhaler şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Symbicort Turbuhaler 3. Cum să utilizaţi Symbicort Turbuhaler 4. Reacţii adverse posibile 5. Cum se păstrează Symbicort Turbuhaler 6. Conţinutul ambalajului şi alte informaţii 1. Ce este Symbicort Turbuhaler şi pentru ce se utilizează Symbicort Turbuhaler este un inhalator care este utilizează pentru tratarea astmului la adulți și adolescenți cu vârsta cuprinsă între ani. De asemenea, este folosit pentru tratarea simptomelor bolii pulmonare obstructive cronice (BPOC) la adulți cu vârsta de 18 ani și peste. Symbicort Turbuhaler conţine două substanţe active: budesonidă şi fumarat de formoterol dihidrat. Budesonida aparţine unui grup de medicamente denumite corticosteroizi. Acţionează prin reducerea şi prevenirea inflamaţiei din plămânii dumneavoastră. Fumaratul de formoterol dihidrat aparţine grupului de medicamente denumite beta 2-agonişti cu durată lungă de acţiune sau bronhodilatatoare. Acţionează prin relaxarea musculaturii din căile respiratorii. Acesta vă ajută să respiraţi mult mai uşor. Astm bronşic Symbicort Turbuhaler poate fi prescris pentru astm bronşic în 2 moduri diferite. a) Pentru unele persoane sunt prescrise două inhalatoare pentru astmul bronşic: Symbicort Turbuhaler şi un alt inhalator de salvare Aceste persoane vor utiliza un inhalator Symbicort Turbuhaler în fiecare zi. Aceasta ajută la prevenirea apariţiei simptomelor de astm bronşic. Vor utiliza inhalatorul de salvare când au nevoie să trateze crizele de astm bronşic, pentru a putea respira din nou mai uşor. b) Pentru unele persoane este prescris un singur inhalator pentru astmul bronşic: Symbicort Turbuhaler Aceste persoane vor utiliza Symbicort Turbuhaler în fiecare zi. Aceasta ajută la prevenirea apariţiei simptomelor de astm bronşic. 1
2 Aceste persoane, de asemenea, vor utiliza Symbicort Turbuhaler când au nevoie să trateze crizele de astm bronşic, pentru a putea respira din nou mai uşor. Aceste persoane nu au nevoie de un inhalator separat pentru aceasta. Boală pulmonară obstructivă cronică (BPOC) Symbicort Turbuhaler poate fi utilizat şi în tratarea simptomelor pacienţilor adulţi cu boală pulmonară obstructivă cronică (BPOC). BPOC este o boală cu durată lungă, a căilor respiratorii de la nivelul plămânilor, care adesea este provocată de fumul de ţigară. 2. Ce trebuie să ştiţi înainte să utilizaţi Symbicort Turbuhaler Nu utilizaţi Symbicort Turbuhaler dacă: - sunteţi alergic la budesonidă, formoterol sau altă componentă a acestui medicament (enumerată la pct. 6), care este lactoza (care conţine mici cantităţi de proteine din lapte). Atenţionări şi precauţii Înainte de utilizarea Symbicort Turbuhaler, spuneţi medicului dumneavoastră sau farmacistului dacă: Sunteţi diabetic Aveţi o infecţie la nivelul plămânilor Aveţi tensiune arterială mare sau aţi avut în antecedente o problemă la nivelul inimii (inclusiv bătăi neregulate ale inimii, puls foarte rapid, îngustare a unor artere sau insuficienţă cardiacă) Aveţi probleme cu glanda tiroidă sau suprarenală Aveţi o valoare mică de potasiu în sânge Aveţi probleme severe la nivelul ficatului Adresați-vă medicului dumneavoastră dacă aveți vederea încețoșată sau alte tulburări de vedere. Symbicort Turbuhaler împreună cu alte medicamente Spuneţi medicului dumneavoastră sau farmacistului dacă utilizați sau aţi utilizat recent sau s-ar putea să utilizaţi orice alte medicamente. În mod special, spuneţi medicului dumneavoastră sau farmacistului utilizaţi oricare din următoarele medicamente: Medicamente beta blocante (cum este atenololul sau propranololul pentru tratarea tensiunii arteriale mari) incluzând picăturile pentru ochi (cum este timololul pentru glaucom) Medicamente pentru bătăi de inimă rapide sau neregulate (cum este chinidina) Medicamente ca digoxina utilizate frecvent pentru insuficienţa cardiacă Diuretice sau medicamente pentru a elimina apa (cum este furosemida). Acestea sunt utilizate pentru tratamentul tensiunii arteriale mari. Corticosteroizi administraţi pe cale orală (cum este prednisolonul) Derivaţi xantinici (cum este teofilina sau aminofilina). Aceştia sunt utilizaţi frecvent în tratamentul astmului bronşic. Alte bronhodilatatoare (cum este salbutamolul). Antidepresive triciclice (cum este amitriptilina) şi antidepresivul nefazodonă. Fenotiazine (cum sunt clorpromazina şi proclorperazina). Medicamente numite Inhibitori de protează HIV (cum este ritonavirul) pentru tratamentul infecţiei cu HIV. Medicamente pentru tratarea infecţiilor (de exemplu, ketoconazol, itraconazol, voriconazol, posaconazol, claritromicină, telitromicină). Medicamente pentru boala Parkinson (cum este levo-dopa). Medicamente pentru problemele tiroidiene (cum este levo-tiroxina). Dacă oricare din cele de mai sus vă sunt familiare sau dacă nu sunteţi sigur, discutaţi acest lucru cu medicul dumneavoastră sau farmacistul înainte să utilizaţi Symbicort Turbuhaler. 2
3 De asemenea, spuneţi medicului dumneavoastră sau farmacistului dacă urmează să fiţi supus unei anestezii generale pentru o intervenţie chirurgicală sau stomatologică. Sarcina, alăptarea şi fertilitatea Dacă sunteţi gravidă sau intenţionaţi să rămâneţi gravidă, discutaţi cu medicul dumneavoastră înainte de a utiliza Symbicort Turbuhaler nu utilizaţi Symbicort Turbuhaler fără acordul medicului dumneavoastră. Dacă rămâneţi gravidă în timpul utilizării Symbicort Turbuhaler, nu întrerupeţi utilizarea acestuia, dar discutaţi imediat cu medicul dumneavoastră. Dacă alăptaţi, discutaţi cu medicul dumneavoastră înainte de a utiliza Symbicort Turbuhaler. Conducerea vehiculelor şi folosirea utilajelor Symbicort Turbuhaler nu are sau are o influenţă neglijabilă asupra capacităţii capacitatea de a conduce sau de a folosi utilaje. Symbicort Turbuhaler conţine lactoză Symbicort Turbuhaler conţine lactoză, care este un tip de zahăr. Dacă medicul dumneavoastră v-a atenţionat că aveţi intoleranţă la unele categorii de glucide, vă rugăm să-l întrebaţi înainte de a lua acest medicament. Cantitatea de lactoză din acest medicament nu determină în mod normal probleme în cazul persoanelor care au intoleranţă la lactoză. Lactoza conţine mici cantităţi de proteine din lapte, care pot provoca reacţii alergice. 3. Cum să utilizaţi Symbicort Turbuhaler Utilizaţi întotdeauna acest medicament exact aşa cum v-a spus medicul dumneavoastră sau farmacistul. Discutaţi cu medicul dumneavoastră sau cu farmacistul dacă nu sunteţi sigur. Este important să utilizaţi Symbicort Turbuhaler zilnic, chiar dacă nu aveţi simptome de astm bronşic sau BPOC. Dacă utilizaţi Symbicort Turbuhaler pentru astm bronşic, medicul dumneavoastră vă va monitoriza periodic simptomele. Dacă aţi luat comprimate care conţin corticosteroizi pentru astmul dumneavoastră sau boala pulmonară obstructivă cronică (BPOC), medicul dumneavoastră vă poate reduce numărul comprimatelor odată ce aţi început tratamentul cu Symbicort Turbuhaler. Dacă aţi luat comprimate care conţin corticosteroizi pentru o perioadă lungă de timp, medicul dumneavoastră poate dori să efectuaţi analizele de sânge din când în când. În cazul reducerii administrării orale a numărului comprimatelor care conţin corticosteroizi, vă puteţi simţi rău chiar dacă simptomele respiratorii pot fi îmbunătăţite. Puteţi prezenta simptome, cum sunt nas înfundat sau secreţii nazale, slăbiciune sau durere musculară sau articulară şi erupţie trecătoare pe piele (eczemă). Dacă oricare din aceste simptome vă deranjează sau apar alte simptome, cum sunt durerea de cap, oboseala, senzaţia de rău (greaţă), starea de rău (vărsături), vă rugăm să vă adresaţi imediat medicului dumneavoastră. Dacă dezvoltaţi simptome alergice sau artritice, poate fi necesar să luaţi alte medicamente. Trebuie să discutaţi cu medicul dumneavoastră dacă sunteţi îngrijorat privind continuarea sau nu a administrării Symbicort Turbuhaler. Medicul dumneavoastră vă poate recomanda administrarea suplimentară a comprimatelor cu corticosteroizi la tratamentul uzual, în decursul perioadelor de stres (de exemplu, în cazul unei infecţii toracice sau înainte de o intervenţie chirurgicală). Informaţii importante despre simptomele dumneavoastră de astm bronşic sau BPOC Dacă simţiţi că nu mai puteţi respira sau aveţi respiraţie şuierătoare în timpul utilizării Symbicort Turbuhaler, trebuie să continuaţi să utilizaţi Symbicort Turbuhaler şi să vă adresaţi medicului dumneavoastră cât mai repede, deoarece este posibil să aveţi nevoie de un tratament suplimentar. Contactaţi imediat medicul dumneavoastră dacă: 3
4 Respiraţi mai greu sau vă treziţi frecvent în timpul nopţii având tulburări respiratorii Simţiţi dimineaţa o senzaţie de constricţie în piept sau constricţia durează mai mult decât în mod normal. Aceste semne pot însemna că astmul bronşic sau BPOC-ul dumneavoastră nu este controlat corespunzător şi probabil aveţi nevoie imediat de un alt tratament sau de un tratament suplimentar. Astm bronşic Symbicort Turbuhaler poate fi recomandat în astmul bronşic în două moduri. Cantitatea de Symbicort Turbuhaler şi modul de utilizare depind de modul de prescriere. a) Vi se poate prescrie Symbicort Turbuhaler şi un alt inhalator de salvare. În acest caz citiţi pct. a) Utilizarea Symbicort Turbuhaler şi un alt inhalator de salvare. b) Symbicort Turbuhaler vă poate fi prescris în monoterapie, ca unic inhalator. În acest caz citiţi pct. b) Utilizarea Symbicort Turbuhaler ca unic inhalator. a) Utilizarea Symbicort Turbuhaler şi un alt inhalator de salvare Utilizaţi Symbicort Turbuhaler zilnic. Aceasta vă ajută la prevenirea apariţiei simptomelor de astm bronşic Adulţi (cu vârsta de 18 ani şi peste) Doza uzuală este de 1-2 inhalaţii, de două ori pe zi Medicul dumneavoastră poate creşte doza la 4 inhalaţii, de două ori pe zi Dacă simptomele dumneavoastră sunt bine controlate, medicul dumneavoastră vă poate recomanda utilizarea medicamentului, o dată pe zi Adolescenţi (cu vârsta cuprinsă între 12 şi 17 ani) Doza uzuală este de 1-2 inhalaţii, de două ori pe zi Dacă simptomele dumneavoastră sunt bine controlate, medicul dumneavoastră vă poate recomanda utilizarea medicamentului, o dată pe zi O concentraţie mai mică de Symbicort Turbuhaler este disponibilă pentru copiii cu vârsta cuprinsă între 6 şi 11 ani. Symbicort Turbuhaler nu este recomandat copiilor cu vârsta mai mică de 6 ani. Medicul dumneavoastră (sau asistenta medicală) vă va ajuta să controlaţi simptomele de astm bronşic. Medicul vă poate ajusta doza de medicament la cea mai mică doză care controlează simptomele de astm bronşic. Cu toate acestea, nu ajustaţi doza, fără să discutaţi în prealabil cu medicul dumneavoastră (sau asistenta medicală). Utilizarea inhalatorului de salvare pentru a trata apariţia simptomelor de astm bronşic. Purtaţi mereu cu dumneavoastră inhalatorul de salvare, pentru a putea fi utilizat la nevoie. Nu utilizaţi Symbicort Turbuhaler pentru tratamentul simptomelor de astm bronşic utilizaţi inhalatorul de salvare. b) Utilizarea Symbicort Turbuhaler ca unic inhalator Utilizaţi Symbicort Turbuhaler în acest mod numai dacă medicul dumneavoastră vă recomandă şi dacă aveţi vârsta peste 12 ani. Utilizaţi Symbicort Turbuhaler zilnic. Aceasta vă ajută la prevenirea apariţiei simptomelor de astm bronşic. Puteţi administra: 1 inhalație dimineaţa şi 1 inhalație dată seara sau administra 2 inhalaţii dimineaţa sau 4
5 administra 2 inhalaţii seara. Medicul vă poate creşte doza la 2 inhalaţii, de două ori pe zi. De asemenea, puteţi utiliza Symbicort Turbuhaler şi ca tratament de salvare în crizele de astm bronşic la apariţia simptomelor, inhalaţi o dată şi aşteptaţi câteva minute dacă nu vă simţiţi mai bine, mai inhalaţi o dată nu administraţi mai mult de 6 inhalaţii pentru o criză Purtaţi întotdeauna inhalatorul Symbicort Turbuhaler cu dumneavoastră, pentru a-l putea utiliza la nevoie. În mod normal o doză totală zilnică de mai mult de 8 inhalaţii nu este necesară. Cu toate acestea, medicul dumneavoastră vă poate permite să utilizaţi până la 12 inhalaţii pe zi, pentru o perioadă limitată de timp. Dacă în mod normal aveţi nevoie de 8 sau mai multe inhalaţii pe zi, este recomandabil să faceţi o programare la medicul dumneavoastră, care ar putea să vă schimbe tratamentul. Nu administraţi mai mult de 12 inhalaţii în 24 de ore. Dacă simptomele de astm bronşic apar în timpul efortului fizic, utilizaţi Symbicort Turbuhaler aşa cum a fost descris mai sus. Nu utilizaţi Symbicort Turbuhaler înainte de începerea efortului fizic pentru a preveni apariţia simptomelor de astm bronşic. Boala pulmonară obstructivă cronică (BPOC) Se va utiliza numai de adulţi (în vârstă de 18 ani şi peste) Doza uzuală este de 2 inhalaţii, de două ori pe zi Medicul dumneavoastră vă poate prescrie, de asemenea, alte medicamente bronhodilatatoare, de exemplu anticolinergice (ca tiotropium sau ipratropium brumură) pentru BPOC. Pregătirea inhalatorului Symbicort Turbuhaler pentru prima sa utilizare Înainte de utilizarea unui inhalator Symbicort Turbuhaler nou, pentru prima dată, trebuie să-l pregătiţi astfel: Deşurubaţi şi ridicaţi capacul. Puteţi să auziţi un zgomot. Ţineţi inhalatorul Symbicort Turbuhaler în sus cu discul roşu în jos Răsuciţi discul roşu cât de mult se poate într-o direcţie. Apoi, răsuciţi în direcţia opusă (nu contează direcţia în care rotiţi prima dată). Veţi auzi un click. Repetaţi manevra, răsucind discul roşu în ambele direcţii Acum inhalatorul Symbicort Turbuhaler este gata de utilizare Cum se administrează o doză De fiecare dată când aveţi nevoie să administraţi o doză, urmaţi instrucţiunile de mai jos. 1. Deşurubaţi şi ridicaţi capacul. Puteţi să auziţi un zgomot. 2. Ţineţi inhalatorul Symbicort Turbuhaler în sus cu discul roşu în jos 5
6 3. Nu ţineţi de piesa bucală când încărcaţi inhalatorul Symbicort Turbuhaler. Pentru a încărca inhalatorul Symbicort Turbuhaler cu o doză, răsuciţi discul roşu cât de mult se poate într-o direcţie. Apoi, răsuciţi în direcţia opusă (nu contează direcţia în care rotiţi prima dată). Veţi auzi un click. Acum inhalatorul Symbicort Turbuhaler este gata de utilizare. Încărcaţi dispozitivul doar înainte de utilizare. 4. Ţineţi inhalatorul Symbicort Turbuhaler departe de gură. Expiraţi uşor (atât cât vă este confortabil). Nu expiraţi prin piesa bucală a inhalatorul Symbicort Turbuhaler. 5. Aşezaţi piesa bucală uşor între dinţi. Strângeţi buzele. Inspiraţi pe gură cât de profund puteţi. Nu mestecaţi sau muşcaţi piesa bucală. 6. Scoateţi inhalatorul Symbicort Turbuhaler din gură. Apoi expiraţi uşor. Cantitatea de medicament inhalată este foarte mică. Aceasta înseamnă că nu-i veţi simţi gustul după inhalare. Dacă aţi urmat instrucţiunile, puteţi să fiţi sigur că aţi inhalat doza şi medicamentul a ajuns în plămânii dumneavoastră. 7. Dacă v-a fost prescrisă mai mult de o inhalaţie, repetaţi paşii Puneţi capacul la loc. 9. Clătiţi gura cu apă după doza zilnică de dimineaţă şi/sau de seară (nu înghiţiţi). Nu încercaţi să îndepărtaţi piesa bucală sau să o răsuciţi în mod inutil; este ataşată de inhalatorul Symbicort Turbuhaler şi nu trebuie scoasă. Nu utilizaţi inhalatorul Symbicort Turbuhaler dacă este stricat sau dacă piesa bucală nu este ataşată la dispozitiv. Ca în cazul tuturor inhalatoarelor, pentru copiii cărora li s-a prescris Symbicort Turbuhaler, persoanele care îi au în grijă trebuie să se asigure că aceştia folosesc corect tehnica de inhalare, aşa cum este descrisă mai sus. Curăţarea inhalatorului Symbicort Turbuhaler Ştergeţi o dată pe săptămână piesa bucală utilizand o cârpă uscată. Nu utilizaţi apă sau lichide când curăţaţi piesa bucală. Când se începe utilizarea unui nou inhalator Indicatorul de doze vă arată câte doze (inhalaţii) au mai rămas în inhalatorul dumneavoastră începând cu 30, 60 sau 120 doze atunci când este plin. Indicatorul de doze este marcat la intervale de 10 doze (pentru inhalatoarele cu 60 și 120 doze) și la intervale de 15 doze (pentru inhalatorul cu 30 doze). Prin urmare, indicatorul de doză nu arată fiecare doză. 6
7 Cand vedeţi pentru prima dată semnul roşu la marginea ferestrei indicatorului, au mai rămas aproximativ 20 doze. Pentru ultimele 10 doze, fondul indicatorului de doze este roşu. Când 0 pe fond roşu a ajuns la jumătatea ferestrei, trebuie să începeţi să utilizaţi un nou inhalator Symbicort Turbuhaler. Notă: Discul se va roti şi veţi auzi click chiar dacă inhalatorul Symbicort Turbuhaler este gol Sunetul pe care îl auziţi când scuturaţi inhalatorul este produs de un agent sicativ şi nu de către medicament. Prin urmare, sunetul nu vă poate spune cât de mult medicament a rămas în inhalatorul Symbicort Turbuhaler Dacă din greşeală, încărcaţi în dispozitiv mai mult de o doză, veţi inhala numai o singură doză, în timp ce indicatorul va înregistra toate dozele încărcate. Dacă utilizaţi Symbicort Turbuhaler mai mult decât trebuie Este important să luaţi doza aşa cum este stabilit pe eticheta medicamentului la farmacie sau cum v-a recomandat medicul dumneavoastră. Nu trebuie să creşteţi sau să scădeţi doza fără să vă sfătuiţi cu medicul. Cele mai frecvente simptome care pot apărea după administrarea mai multor doze de Symbicort Turbuhaler decât trebuie sunt tremurăturile, durerea de cap sau bătăile rapide ale inimii. Dacă uitaţi să utilizaţi Symbicort Turbuhaler Dacă aţi uitat să luaţi o doză, luaţi-o cât de repede vă amintiţi. Cu toate acestea, dacă este aproape ora de administrare a dozei următoare, nu luaţi doza uitată, luaţi următoarea doză, la ora obişnuită. Nu luaţi o doză dublă pentru a înlocui doza uitată. Dacă aveţi orice întrebări suplimentare cu privire la acest medicament, adresaţi-vă medicului dumneavoastră sau farmacistului. 4. Reacţii adverse posibile Ca toate medicamentele, acest medicament poate provoca uneori reacţii adverse, cu toate că nu apar la toate persoanele. Dacă apar oricare din următoarele, opriţi utilizarea Symbicort Turbuhaler şi adresaţi-vă imediat medicului dumneavoastră: Umflare a feţei, în special în jurul gurii (limbă şi/sau gât şi/sau dificultăţi la înghiţire) sau urticarie cu dificultăţi în respiraţie (angioedem) şi/sau senzaţie bruscă de leşin. Acestea pot însemna că aveţi o reacţie alergică. Aceasta se întâmplă rar, afectând mai puţin de 1 din 1000 de persoane. Respiraţie şuierătoare cu debut brusc sau scurtarea respiraţiei imediat după inhalarea medicamentului. Dacă apar oricare din aceste simptome, opriţi imediat administrarea Symbicort Turbuhaler şi utilizaţi inhalatorul de salvare. Adresaţi-vă medicului dumneavoastră imediat pentru că puteţi avea nevoie de o schimbare a tratamentului. Aceasta se întâmplă foarte rar, afectând mai puţin de 1 din de persoane. Alte posibile reacţii adverse: Frecvente (afectează până la 1 din 10 persoane) Palpitaţii (conştientizarea bătăilor inimii), tremor localizat sau generalizat. Dacă apar aceste reacţii adverse, ele sunt, de regulă, uşoare şi dispar, în mod normal, la continuarea tratamentului cu Symbicort Turbuhaler. Stomatită (infecţie fungică la nivelul gurii). Aceasta e puţin probabil să apară dacă vă clătiţi gura după ce utilizaţi inhalatorul Symbicort Turbuhaler Dureri uşoare în gât, tuse şi voce răguşită 7
8 Durere de cap Pneumonie (infecție la nivelul plămânilor) la pacienții cu BPOC Spuneți medicului dumneavoastră dacă manifestați oricare dintre următoarele simptome în timp ce luați Symbicort Turbuhaler, deoarece acestea pot indica o infecție la nivelul plămânilor: Febră sau frisoane Eliminare crescută de mucus, modificare a culorii mucusului Agravare a tusei sau a dificultăților de respirație Mai puţin frecvente (afectează până la 1 din 100 de persoane) Senzaţie de nelinişte, nervozitate sau agitaţie Tulburări de somn Ameţeli Greaţă (senzaţie de rău) Bătăi rapide ale inimii Vânătăi Crampe musculare Vedere încețoșată Rare (afectează până la 1 din 1000 de persoane) Erupţie trecătoare pe piele, mâncărime Bronhospasm (constricţia muşchilor căilor respiratorii având drept urmare respiraţia şuierătoare). Dacă respiraţia şuierătoare apare brusc după utilizarea Symbicort Turbuhaler, opriţi utilizarea Symbicort Turbuhaler şi adresaţi-vă imediat medicului dumneavoastră Valori mici de potasiu în sânge Bătăi neregulate ale inimii Foarte rare (afectează până la 1 din de persoane) Depresie Tulburări de comportament, în special la copii Durere în piept sau senzaţie de apăsare (angina pectorală) O creştere a glucozei (zahărului) din sânge Modificări ale gustului, cum ar fi un gust neplăcut în gură Modificări ale tensiunii arteriale Corticosteroizii utilizaţi pe cale inhalatorie pot afecta producerea de hormoni steroidieni din organismul dumneavoastră, în special dacă sunt utilizaţi în doze mari şi pe perioadă îndelungată. Aceste efecte pot include: modificări ale densităţii minerale osoase (subţierea oaselor) cataractă (înceţoşarea lentilelor ochiului) glaucomul (tensiune mărită la nivelul ochiului) o încetinire a ritmului de creştere la copii şi adolescenţi un efect asupra glandei suprarenale (o glandă mică situată lângă rinichi). Aceste reacţii adverse sunt mai puţin probabil să apară la utilizarea corticosteroizilor administraţi pe cale inhalatorie comparativ cu utilizarea corticosteroizilor pe cale orală. Raportarea reacţiiloradverse Dacă manifestaţi orice reacţii adverse, adresaţi-vă medicului dumneavoastră, farmacistului sau asistentei medicale. Acestea includ orice reacţii adverse nemenţionate în acest prospect. De asemenea, puteţi raporta reacţiile adverse direct prin intermediul sistemului naţional de raportare, ale cărui detalii sunt publicate pe web-site-ul Agenţiei Naţionale a Medicamentului şi a Dispozitivelor Medicale Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale Str. Aviator Sănătescu nr. 48, sector 1 8
9 Bucuresti RO Tel: Fax: adr@anm.ro. Raportând reacţiile adverse, puteţi contribui la furnizarea de informaţii suplimentare privind siguranţa acestui medicament. 5. Cum se păstreaza Symbicort Turbuhaler Nu lăsaţi acest medicament la vederea şi îndemâna copiilor. Nu utilizaţi acest medicament după data de expirare înscrisă pe cutie sau eticheta dispozitivului de inhalare, după EXP. Data expirării se referă la ultima zi a lunii respective. Acest medicament nu necesită condiții speciale de păstrare. Nu aruncaţi niciun medicament pe calea apei sau a reziduurilor menajere. Întrebaţi farmacistul cum să aruncaţi medicamentele pe care nu le mai folosiţi. Aceste măsuri vor ajuta la protejarea mediului. 6. Conţinutul ambalajului şi alte informaţii Ce conţine Symbicort Turbuhaler160 micrograme/4,5 micrograme/inhalaţie, pulbere de inhalat Substanţele active sunt budesonida şi fumarat de formoterol dihidrat. Fiecare doză inhalată conţine budesonidă 160 micrograme şi fumarat de formoterol dihidrat 4,5 micrograme. Alt component este lactoza monohidrat (care conţine proteine din lapte). Cum arată Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere de inhalat şi conţinutul ambalajului Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere de inhalat este un inhalator care conţine medicamentul dumneavoastră. Pulberea de inhalat este de culoare albă. Fiecare inhalator Turbuhaler conţine 30, 60 sau 120 de doze, având un corp de culoare albă şi un disc roşu care se roteşte. Discul conţine un cod Braille, numărul 6, pentru identificare pentru diferenţierea de alte medicamente inhalatorii AstraZeneca. Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere de inhalat este disponibil în cutii cu 1 inhalator conţinând 30 de doze sau cu 1, 2, 3, 10 sau 18 inhalatoare conţinând 60 sau 120 de doze. Este posibil ca nu toate mărimile de ambalaj să fie comercializate. Deţinătorul autorizaţiei de punere pe piaţă şi fabricantul Deţinătorul autorizaţiei de punere pe piaţă AstraZeneca AB Forskargatan 18, SE-15185, Södertälje Suedia Fabricanţi AstraZeneca AB Kvarnbergagatan 12, SE-15185, Södertälje Suedia AstraZeneca GmbH Tinsdaler Weg 183, D Wedel Germania 9
10 AstraZeneca UK Limited Silk Road Business Park Macclesfield Cheshire SK10 2NA Marea Britanie Acest medicament este autorizat în Statele Membre ale Spaţiului Economic European sub următoarele denumiri comerciale: Statul Membru Austria Belgia Bulgaria Cipru Croatia Republica Cehă Danemarca Estonia Finlanda Franţa Germania Grecia Ungaria Islanda Irlanda Italia Letonia Lituania Luxemburg Malta Olanda Norvegia Polonia Portugalia România Republica Slovacia Slovenia Spania Suedia Marea Britanie Denumirea comercială şi concentraţia Symbicort Turbohaler 160μg/4.5μg/inhalation Symbicort Turbohaler 160μg/4.5μg/inhalation Symbicort Turbuhaler 160 μg/4.5 μg/inhalation Symbicort Turbuhaler 200μg/6μg/inhalation Symbicort Turbuhaler 200μg/6μg/inhalation Symbicort Turbohaler 160μg/4.5μg/inhalation Symbicort Turbuhaler160μg/4.5μg/inhalation Symbicort Turbohaler 200μg/6μg/inhalation Symbicort 160μg/4.5μg/inhalation Symbicort Turbohaler 160μg/4.5μg/inhalation Symbicort Turbohaler 200μg/6μg/inhalation Symbicort Turbuhaler 200μg/6μg/inhalation Symbicort Turbohaler160μg/4.5μg/inhalation Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie Symbicort Turbuhaler 200μg/6μg/inhalation Symbicort Turbuhaler160μg/4.5μg/inhalation Symbicort Turbohaler 200μg/6μg/inhalation Acest prospect a fost aprobat în Mai 2018 Informații detaliate și actualizate referitoare la acest medicament sunt disponibile prin scanarea codului QR care apare în prospect și pe cutie, folosind un smartphone. Aceleași informații sunt disponibile urmând link-ul: {cod QR} 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin n
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
PRO_671_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
PRO_886_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 885/2008/01 Anexa 1' 886/2008/01 887/2008/01 Prospect Prospect: Informaţii pentru utilizator Seretide Inhaler CFC-Free 25 micrograme/50 micrograme suspensie de inhalat
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 885/2008/01 Anexa 1' 886/2008/01 887/2008/01 Prospect Prospect: Informaţii pentru utilizator Seretide Inhaler CFC-Free 25 micrograme/50 micrograme suspensie de inhalat
PRO_3712_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/ Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
VISINE®
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6026/2013/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Osetron 4 mg comprimate filmate Ondansetron Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6026/2013/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Osetron 4 mg comprimate filmate Ondansetron Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progeste
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg co
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
PRO_4755_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
PRO_4804_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
PRO_1053_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1053/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator NEBIVOLOL TERAPIA 5 mg comprimate Nebivolol Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1053/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator NEBIVOLOL TERAPIA 5 mg comprimate Nebivolol Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/ Anexa /2012/ /2012/ Prospect Prospect: Informaţii pe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a înc
 Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule
 AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule pentru suspensie orală Keflex 250 mg/5 ml granule
AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule pentru suspensie orală Keflex 250 mg/5 ml granule
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabil
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabile Montelukast Pentru copii cu vârsta cuprinsă între
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabile Montelukast Pentru copii cu vârsta cuprinsă între
PRO_837_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 837/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator Diclac 50 mg/g gel Diclofenac sodic Citiţi cu atenţie şi în întregime acest prospect înainte de
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 837/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator Diclac 50 mg/g gel Diclofenac sodic Citiţi cu atenţie şi în întregime acest prospect înainte de
Проспект: Информация для пациента, потребителя
 Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
ANEXA II
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7270/2014/01-02-03-04-05-06-07-08-09 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Voltaren Forte 23,2 mg/g gel Diclofenac dietilamină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7270/2014/01-02-03-04-05-06-07-08-09 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Voltaren Forte 23,2 mg/g gel Diclofenac dietilamină Citiţi cu atenţie şi
Microsoft Word _Perfalgan 100ml_UK PIL_II-44+ UT.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu aten
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
PROSPECT: INFORMAŢII PENTRU UTILIZATOR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4037/2011/01-05 Anexa 1' 4038/2011/01-05 Prospect Prospect: Informaţii pentru utilizator rizatriptan Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4037/2011/01-05 Anexa 1' 4038/2011/01-05 Prospect Prospect: Informaţii pentru utilizator rizatriptan Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
B
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3872/2011/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru pacient 25 mg comprimate filmate Sildenafil Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3872/2011/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru pacient 25 mg comprimate filmate Sildenafil Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofi
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
PRO_900_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 900 /2008/01-02-03 Anexa 1 Prospect PROSPECT: Informaţii pentru utilizator Brival 125 mg comprimate Brivudină Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 900 /2008/01-02-03 Anexa 1 Prospect PROSPECT: Informaţii pentru utilizator Brival 125 mg comprimate Brivudină Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6637/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DIAZEPAM 10 mg comprimate Diazepam Citiţi cu atenţie şi în întregime acest prospect înainte de a
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6637/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DIAZEPAM 10 mg comprimate Diazepam Citiţi cu atenţie şi în întregime acest prospect înainte de a
simva leaflet
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el con
 PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el conţine informaţii importante pentru dumneavoastră Luaţi
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el conţine informaţii importante pentru dumneavoastră Luaţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN,
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN, 10 mg, comprimate filmate CITALORAN, 20 mg, comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN, 10 mg, comprimate filmate CITALORAN, 20 mg, comprimate
PRO_3436_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3436/2011/01-20 Anexa 1' 3437/2011/01-20 3438/2011/01-20 3439/2011/01-20 Prospect Prospect: Informaţii pentru utilizator Bisoprolol fumarat Mylan 1,25 mg comprimate filmate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3436/2011/01-20 Anexa 1' 3437/2011/01-20 3438/2011/01-20 3439/2011/01-20 Prospect Prospect: Informaţii pentru utilizator Bisoprolol fumarat Mylan 1,25 mg comprimate filmate
AUTORIZATIE DE PUNERE PE PIATĂ NR
 Certificat de înregistrare al medicamentului - nr. 21488 din 22.01.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU PACIENT Indapamid LPH 1,5 mg comprimate cu eliberare prelungită Indapamidă Citiţi cu atenţie
Certificat de înregistrare al medicamentului - nr. 21488 din 22.01.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU PACIENT Indapamid LPH 1,5 mg comprimate cu eliberare prelungită Indapamidă Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 9
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 90 mg retard, comprimate cu eliberare prelungită Diltiazem
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 90 mg retard, comprimate cu eliberare prelungită Diltiazem
PRO_715_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 715/2008/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PRONORAN 50 mg drajeuri cu eliberare prelungită Piribedil Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 715/2008/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PRONORAN 50 mg drajeuri cu eliberare prelungită Piribedil Citiţi cu atenţie şi în întregime acest
AUTORIZATIE DE PUNERE PE PIATA NR
 AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 43/2007/01; 44/2007/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU PACIENT CAPTOPRIL LPH 25 mg comprimate CAPTOPRIL LPH 50 mg comprimate Captopril Citiţi cu atenţie
AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 43/2007/01; 44/2007/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU PACIENT CAPTOPRIL LPH 25 mg comprimate CAPTOPRIL LPH 50 mg comprimate Captopril Citiţi cu atenţie
PRO_6774_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6774/2006/01-02-03 Anexa 1 6775/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iopamiro 300, soluţie injectabilă, 612,4 mg/m Iopamiro 370, soluţie injectabilă,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6774/2006/01-02-03 Anexa 1 6775/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iopamiro 300, soluţie injectabilă, 612,4 mg/m Iopamiro 370, soluţie injectabilă,
AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extrac
 AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extract uscat de Hyperici herba (iarbă de sunătoare) Ze 117
AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extract uscat de Hyperici herba (iarbă de sunătoare) Ze 117
AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg c
 AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg comprimate filmate Capecitabină Actavis 500 mg comprimate
AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg comprimate filmate Capecitabină Actavis 500 mg comprimate
Microsoft Word - 1st year leaflet_ROM
 Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator Quodixor 150 mg comprimate filmate Acid iba
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator 150 mg comprimate filmate Acid ibandronic Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator 150 mg comprimate filmate Acid ibandronic Citiţi cu atenţie şi în întregime acest prospect înainte
PRO_10425_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.10425/2017/01-12 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lorista HCT 100 mg/12,5 mg comprimate filmate Losartan potasic/hidroclorotiazidă Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.10425/2017/01-12 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lorista HCT 100 mg/12,5 mg comprimate filmate Losartan potasic/hidroclorotiazidă Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/ Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-b
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-butilamină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-butilamină Citiţi cu atenţie şi în întregime acest prospect
PRO_202_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 202/2007/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Amiodaronă LPH 200 mg, comprimate Clorhidrat de amiodaronă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 202/2007/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Amiodaronă LPH 200 mg, comprimate Clorhidrat de amiodaronă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2018/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefixim
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
PRO_3425_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
PACKAGE LEAFLET: INFORMATION FOR THE USER
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4997/2012/01-02-03-04-05-06 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Levelanz 500 mg comprimate filmate Levetiracetam Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4997/2012/01-02-03-04-05-06 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Levelanz 500 mg comprimate filmate Levetiracetam Citiţi cu atenţie şi în întregime
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4586/2012/01-02-03-04-05-06-07-08-09-10 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Doreta 75 mg/650 mg comprimate filmate Clorhidrat de tramadol/paracetamol
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4586/2012/01-02-03-04-05-06-07-08-09-10 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Doreta 75 mg/650 mg comprimate filmate Clorhidrat de tramadol/paracetamol
PRO_6096_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6094/2014/01-02-03-04 Anexa 1 6095/2014/01-02-03-04 6096/2014/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Concor Cor 2,5 mg comprimate filmate Concor
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6094/2014/01-02-03-04 Anexa 1 6095/2014/01-02-03-04 6096/2014/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Concor Cor 2,5 mg comprimate filmate Concor
AUTORIZATIE DE PUNERE PE PIATA NR
 AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
PROSPECT: INFORMAŢII PENTRU UTILIZATOR
 PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentr
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentru soluţie injectabilă Gonadotrofină corionică umană
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentru soluţie injectabilă Gonadotrofină corionică umană
Certificat de înregistrare al medicamentului nr din nr din Modificare din la anexa 1 PROSPECT: INFORMAŢ
 Certificat de înregistrare al medicamentului nr. 21309 din 25.11.2014 nr. 21308 din 25.11.2014 Modificare din 10.12.2015 la anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR Co-Sentor 50 mg/12,5 mg comprimate
Certificat de înregistrare al medicamentului nr. 21309 din 25.11.2014 nr. 21308 din 25.11.2014 Modificare din 10.12.2015 la anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR Co-Sentor 50 mg/12,5 mg comprimate
PRO_278_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 278/2007/01-09 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR STAMARIL Pulbere și solvent pentru suspensie injectabilă în seringă preumplută Vaccin pentru febra
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 278/2007/01-09 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR STAMARIL Pulbere și solvent pentru suspensie injectabilă în seringă preumplută Vaccin pentru febra
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
PRO_11765_ doc
 AUTORIZATIE DE PUNERE PE PIATA NR. 11765/2019/01-02-03-04 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dostinex 0,5 mg comprimate Cabergolină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZATIE DE PUNERE PE PIATA NR. 11765/2019/01-02-03-04 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dostinex 0,5 mg comprimate Cabergolină Citiţi cu atenţie şi în întregime acest prospect
RGD: 57144/E/2
 Prospect: Informaţii pentru consumator/pacient KLION-D 100 comprimate vaginale Metronidazolum/Miconazolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament
Prospect: Informaţii pentru consumator/pacient KLION-D 100 comprimate vaginale Metronidazolum/Miconazolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie injectabilă Sulfat de atropină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie injectabilă Sulfat de atropină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa /2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 40
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa 1 9495/2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 400 mg capsule Gabapentină Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa 1 9495/2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 400 mg capsule Gabapentină Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/ Anexa /2012/ Prospect Prospect: Informaţii pentru pacient
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/01-02-03-04-05-06-07 Anexa 1 5210/2012/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Telmotens 40 mg comprimate filmate Telmotens 80 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/01-02-03-04-05-06-07 Anexa 1 5210/2012/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Telmotens 40 mg comprimate filmate Telmotens 80 mg
PRO_2214_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2214/2009/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR ZOLADEX 3,6 mg implant goserelină Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2214/2009/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR ZOLADEX 3,6 mg implant goserelină Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
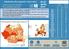 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
PRO_6878_ doc
 AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 6878/2006/01-02-03-04-05; Anexa 1 6879/2006/01-02-03-04 6880/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iomeron 300, soluţie injectabilă, 612,4
AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 6878/2006/01-02-03-04-05; Anexa 1 6879/2006/01-02-03-04 6880/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iomeron 300, soluţie injectabilă, 612,4
ANEXA II
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4133/2011/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR AKINETON 2 mg comprimate Clorhidrat de biperiden Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4133/2011/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR AKINETON 2 mg comprimate Clorhidrat de biperiden Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COM
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6940/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Prospan picături orale soluţie,
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZATIE DE PUNERE PE PIATĂ NR. 8067/2006/01-02-03-04 Anexa 2 8068/2006/01-02-03-04-05-06 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
AUTORIZATIE DE PUNERE PE PIATĂ NR. 8067/2006/01-02-03-04 Anexa 2 8068/2006/01-02-03-04-05-06 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
ЗАТВЕРДЖЕНО
 Prospect: Informaţii pentru consumator/pacient Celestoderm-V 1 mg/gram unguent Betametazonă (de betametazonă 17-valerat) Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi
Prospect: Informaţii pentru consumator/pacient Celestoderm-V 1 mg/gram unguent Betametazonă (de betametazonă 17-valerat) Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi
Denumirea comercială, forma farmaceutică şi concentraţia
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6396/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Azitromicină Terapia 250 mg comprimate filmate Azitromicină Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6396/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Azitromicină Terapia 250 mg comprimate filmate Azitromicină Citiţi cu atenţie şi în întregime
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7286/2015/01-02 Anexa /2015/ /2015/ Prospect Prospect: Informaţii pentru utilizator Nicor
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7286/2015/01-02 Anexa 1 7287/2015/01-02-03 7288/2015/01-02-03 Prospect Prospect: Informaţii pentru utilizator Clear 25 mg/16 ore plasture transdermic Clear 15 mg/16 ore
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7286/2015/01-02 Anexa 1 7287/2015/01-02-03 7288/2015/01-02-03 Prospect Prospect: Informaţii pentru utilizator Clear 25 mg/16 ore plasture transdermic Clear 15 mg/16 ore
PRO_6705_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6705/2006/01 Anexa 1 6706/2006/01 6707/2006/01 Prospect Prospect: Informaţii pentru utilizator Accuzide 10 mg/12,5 mg comprimate filmate Accuzide Forte 20 mg/12,5 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6705/2006/01 Anexa 1 6706/2006/01 6707/2006/01 Prospect Prospect: Informaţii pentru utilizator Accuzide 10 mg/12,5 mg comprimate filmate Accuzide Forte 20 mg/12,5 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate fil
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/01-02-03-04-05-06-07 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate filmate Ibuprofen Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/01-02-03-04-05-06-07 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate filmate Ibuprofen Citiţi cu atenţie şi în întregime acest
PRO_9516_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9516/2016/01-24 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIMOVO 500 mg/20 mg comprimate cu eliberare modificată naproxen şi esomeprazol Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9516/2016/01-24 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIMOVO 500 mg/20 mg comprimate cu eliberare modificată naproxen şi esomeprazol Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
AUTORIZATIE DE PUNERE PE PIATA NR
 Certificat de înregistrare al medicamentului - nr. 21883 din 30.07.2015 nr. 21884 din 30.07.2015 nr. 21882 din 30.07.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR FASTUM GEL 2,5% gel Citiţi cu atenţie
Certificat de înregistrare al medicamentului - nr. 21883 din 30.07.2015 nr. 21884 din 30.07.2015 nr. 21882 din 30.07.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR FASTUM GEL 2,5% gel Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2019/ Anexa 1 Prospect PROSPECT: INSTRUCŢIUNI PENTRU UTILIZATOR OCTAGAM 50 mg/ml soluţie
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 11338/2019/01-02-03-04-05-06-07 Anexa 1 Prospect PROSPECT: INSTRUCŢIUNI PENTRU UTILIZATOR OCTAGAM 50 mg/ml soluţie perfuzabilă Imunoglobulină umană normală (Ig IV) Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 11338/2019/01-02-03-04-05-06-07 Anexa 1 Prospect PROSPECT: INSTRUCŢIUNI PENTRU UTILIZATOR OCTAGAM 50 mg/ml soluţie perfuzabilă Imunoglobulină umană normală (Ig IV) Citiţi
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 675/2008/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Ventolin 100 Inhaler CFC-Free,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 675/2008/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Ventolin 100 Inhaler CFC-Free,
1
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2339/2010/04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Prismasol 2 mmol/l potasiu soluţie pentru hemofiltrare/hemodializă Clorură de calciu dihidrat/ Clorură
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2339/2010/04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Prismasol 2 mmol/l potasiu soluţie pentru hemofiltrare/hemodializă Clorură de calciu dihidrat/ Clorură
VIAȚA CU ASTM Cele mai frecvente întrebări despre astm Broşură destinată pacienţilor cu astm şi aparţinătorilor
 VIAȚA CU ASTM Cele mai frecvente întrebări despre astm Broşură destinată pacienţilor cu astm şi aparţinătorilor www.viatacuastm.ro O campanie Institutul pentru Dezvoltare în Sănătate și Educație Cu sprijinul
VIAȚA CU ASTM Cele mai frecvente întrebări despre astm Broşură destinată pacienţilor cu astm şi aparţinătorilor www.viatacuastm.ro O campanie Institutul pentru Dezvoltare în Sănătate și Educație Cu sprijinul
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofi
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofibrat Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofibrat Citiţi cu atenţie şi în întregime acest prospect
PRO_8548_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8548/2016/01-18 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Folinat de calciu Kabi 10 mg/ml soluţie injectabilă/perfuzabilă Acid folinic Citiţi cu atenție
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8548/2016/01-18 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Folinat de calciu Kabi 10 mg/ml soluţie injectabilă/perfuzabilă Acid folinic Citiţi cu atenție
PRO_7170_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7169/2014/01-02-03-04-05-06 Anexa 1 7170/2014/01-02-03-04-05-06 7171/2014/01-02-03-04-05-06 7172/2014/01-02-03-04-05-06 Prospect Prospect: Informaţii pentru utilizator
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7169/2014/01-02-03-04-05-06 Anexa 1 7170/2014/01-02-03-04-05-06 7171/2014/01-02-03-04-05-06 7172/2014/01-02-03-04-05-06 Prospect Prospect: Informaţii pentru utilizator
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI!
 Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
SPC in English
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
PRO_6041_6042__2013_7_var_2__2018_7.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6041/2013/01-02-03-04-05-06-07 Anexa 1 6042/2013/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Algoxib 100 mg capsule Algoxib 200 mg capsule celecoxib
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6041/2013/01-02-03-04-05-06-07 Anexa 1 6042/2013/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Algoxib 100 mg capsule Algoxib 200 mg capsule celecoxib
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
RCP_4839_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4839/2004/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI KETONAL 25 mg/g gel
PRO_3961_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3961/2011/01 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ibuprofen Arena 400 mg capsule Ibuprofen Citiţi cu atenţie şi în întregime acest prospect, deoarece
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3961/2011/01 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ibuprofen Arena 400 mg capsule Ibuprofen Citiţi cu atenţie şi în întregime acest prospect, deoarece
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa /2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml gran
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa 1 8634/2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml granule pentru suspensie orală CEFALEXIN SANDOZ 250 mg/5
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa 1 8634/2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml granule pentru suspensie orală CEFALEXIN SANDOZ 250 mg/5
PRO_2078_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2078/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Duphaston 10 mg comprimate filmate Didrogesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2078/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Duphaston 10 mg comprimate filmate Didrogesteron Citiţi cu atenţie şi în întregime acest prospect
Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea CE ESTE DMK 1.1
 https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
https://www.printo.it/pediatric-rheumatology/ro/intro Deficitul de Mevalonat Kinază (DMK) (sau sindromul hiper IgD) Versiunea 2016 1. CE ESTE DMK 1.1 Ce este această boală? Deficitul de mevalonat kinază
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE Bine ați venit pe site-ul sondajului online Dedicated
 Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pen
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pentru soluţie perfuzabilă Clorhidrat de irinotecan trihidrat
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1931/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Irinotecan Vipharm 20 mg/ml, concentrat pentru soluţie perfuzabilă Clorhidrat de irinotecan trihidrat
