PROSPECT: INFORMAŢII PENTRU UTILIZATOR
|
|
|
- Geta Oprea
- 4 ani în urmă
- Vzualizari:
Transcriere
1 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4037/2011/01-05 Anexa 1' 4038/2011/01-05 Prospect Prospect: Informaţii pentru utilizator rizatriptan Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să luaţi acest medicament deoarece conţine informaţii importante pentru dumneavoastră. - Păstraţi acest prospect. S-ar putea să fie necesar să-l recitiţi. - Dacă aveţi orice întrebări suplimentare, adresaţi-vă medicului dumneavoastră sau farmacistului. - Acest medicament a fost prescris numai pentru dumneavoastră. Nu trebuie să-l daţi altor persoane. Le poate face rău, chiar dacă au aceleaşi semne de boală ca dumneavoastră. - Dacă manifestaţi orice reacţii adverse, adresaţi-vă medicului dumneavoastră sau farmacistului. Acestea includ orice posibile reacţii adverse nemenţionate în acest prospect. Vezi punctul 4. Ce găsiţi în acest prospect: 1. Ce este MAXALT şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să luaţi MAXALT 3. Cum să luaţi MAXALT 4. Reacţii adverse posibile 5. Cum se păstrează MAXALT 6. Conţinutul ambalajului şi alte informaţii 1. Ce este MAXALT şi pentru ce se utilizează MAXALT aparţine unei clase de medicamente numite agonişti selectivi de receptori serotoninergici 5-HT 1B/1D. MAXALT este utilizat pentru a trata episoadele cu durere de cap din crizele de migrenă, la adulţi. Tratamentul cu MAXALT: Scade dilataţia vaselor de sânge de la nivelul creierului. Această dilataţie determină durerea de cap dintr-o criză de migrenă. 2. Ce trebuie să ştiţi înainte să luaţi MAXALT Nu luaţi MAXALT dacă: - sunteţi alergic la rizatriptan sau la oricare dintre celelalte componente ale acestui medicament (enumerate la punctul 6) - aveţi tensiune arterială mare stadiu moderat-sever sau sever sau aveţi tensiune arterială mare stadiu uşor, dar care nu este controlată prin medicaţie. - aveţi sau aţi avut vreodată probleme cu inima incluzând atac de cord sau durere la nivelul pieptului (angină) sau aţi prezentat simptome ale unei boli de inimă. - aveţi probleme severe cu ficatul sau cu rinichii - aţi avut un accident vascular cerebral (AVC) sau un accident vascular minor (accident ischemic tranzitor AIT). 1
2 - aveţi probleme cu obstrucţia arterelor (boală vasculară periferică). - utilizaţi inhibitori de monoaminoxidază (IMAO) cum sunt moclobemidă, fenelzină, tranilcipromidă, sau pargilină (medicamente împotriva depresiei), sau linezolid (un antibiotic), sau dacă a trecut mai puţin de 2 săptămâni de la întreruperea utilizării de inhibitori de MAO. - utilizaţi acum medicaţie de tip ergotamină, cum sunt ergotamină sau dihidro-ergotamină care sunt folosite pentru a trata migrena dumneavoastră sau metisergidă utilizat pentru prevenirea crizelor de migrenă - utilizaţi alte medicamente din aceeaşi clasă, cum sunt sumatriptan, naratriptan sau zolmitriptan utilizate pentru a trata migrena dumneavoastră. (vezi mai jos, MAXALT împreună cu alte medicamente ) În cazul în care nu sunteţi sigur dacă oricare dintre situaţiile de mai sus se aplică în cazul dumneavoastră, adresaţi-vă medicului dumneavoastră sau farmacistului înainte de a utiliza MAXALT. Atenţionări şi precauţii Înainte să luați MAXALT, adresaţi-vă medicului dumneavoastră sau farmacistului dacă: - aveţi oricare dintre următorii factori de risc pentru afecţiunile de inimă: tensiune arterială mare, diabet zaharat, fumaţi sau utilizaţi tratament de substituţie cu nicotină, familia dumneavoastră are un istoric de afecţiuni de inimă, sunteţi bărbat cu vârsta peste 40 ani, sunteţi la postmenopauză - aveţi probleme cu ficatul sau cu rinichii. - aveţi o problemă specială cu felul în care bate inima dumneavoastră (bloc de ramură). - aveţi sau aţi avut orice fel de alergie - durerea dumneavoastră de cap este asociată cu ameţeală, dificultate la mers, lipsă de coordonare sau slăbiciune la nivelul picioarelor sau a braţelor. - utilizaţi produse din plante care conţin sunătoare. - aţi avut o reacţie alergică cu umflare a feţei, buzelor, limbii şi/sau gâtului care poate determina dificultate în respiraţie şi/sau la înghiţire (angioedem). - utilizaţi inhibitori selectivi ai recaptării serotoninei (ISRS) cum sunt sertralină, oxalat de escitalopram şi fluoxetină sau inhibitori ai recaptării serotoninei şi noradrenalinei(irsn) cum sunt venlafaxină şi duloxetină pentru tratamentul depresiei. - aţi avut simptome de scurtă durată incluzând dureri în piept şi senzaţia de constricţie. Dacă utilizaţi MAXALT de prea multe ori acest lucru poate determina o durere de cap cronică. În astfel de cazuri trebuie să vă adresaţi medicului dumneavoastră deoarece este posibil să întrerupeţi utilizarea de MAXALT. Vă rugăm spuneţi medicului dumneavoastră sau farmacistului despre simptomele dumneavoastră. Medicul dumneavoastră va decide dacă aveţi migrenă. Trebuie să utilizaţi MAXALT doar pentru crizele de migrenă. MAXALT nu trebuie utilizat pentru a trata durerile de cap care ar putea fi determinate de alte afecţiuni mai grave. Vă rugăm să spuneţi medicului dumneavoastră dacă luaţi sau aţi luat recent, sau plănuiţi să luaţi, orice alte medicamente, inclusiv dintre cele eliberate fără prescripţie medicală. Acestea includ produsele din plante şi medicamentele care le luaţi în mod normal pentru migrenă. Aceasta, deoarece MAXALT poate afecta modul în care aceste medicamente acţionează. De asemenea alte medicamente pot afecta modul în care acţionează MAXALT. MAXALT împreună cu alte medicamente Nu luaţi MAXALT: - dacă utilizaţi deja un agonist de 5-HT 1B/1D (uneori denumit în continuare triptani ), cum sunt sumatriptan, naratriptan sau zolmitriptan. - dacă utilizaţi inhibitori de monoaminoxidază (IMAO) cum sunt moclobamidă, fenelzină, tranilcipromină, linezolid, sau pargilină sau dacă au trecut mai puţin de două săptămâni de când aţi întrerup utilizarea de inhibitori de MAO. 2
3 - dacă utilizaţi medicamente de tipul ergotaminei cum sunt ergotamină sau dihidro-ergotamină care vă tratează migrena. - dacă utilizaţi metisergidă care se foloseşte pentru a preveni criza de migrenă. Dacă medicamentele listate mai sus sunt luate împreună cu MAXALT pot creşte riscul apariţiei reacţiilor adverse. Trebuie să aşteptaţi cel puţin 6 ore după ce aţi luat MAXALT înainte de a utiliza un medicament de tip ergotamină cum sunt ergotamina sau dihidro-ergotamina sau metisergida. Trebuie să aşteptaţi cel puţin 24 ore după ce aţi luat medicamente de tipul ergotaminei înainte de a utiliza MAXALT. Întrebaţi medicul dumneavoastră în legătură cu instrucţiunile şi riscurile legate de utilizarea MAXALT: dacă utilizaţi propanolol (vezi punctul 3 : Cum să luaţi MAXALT). dacă utilizaţi ISRS cum sunt sertralină, oxalat de escitalopram, şi fluoxetină sau IRSN cum sunt venlafaxină şi duloxetină pentru depresie. Vă rugăm să spuneţi medicului dumneavoastră sau farmacistului dacă luaţi sau aţi luat recent orice alte medicamente, inclusiv dintre cele eliberate fără prescripţie medicală. MAXALT împreună cu alimente şi băuturi MAXALT va intra în acţiune mai greu în cazul în care este luat după alimente. Cu toate că este mai bine să-l luaţi pe stomacul gol, puteţi totuşi să-l luaţi dacă aţi mâncat. Sarcina şi alăptarea Dacă sunteţi gravidă sau alăptaţi, credeţi că aţi putea fi gravidă sau intenţionaţi să rămâneţi gravidă, adresaţi-vă medicului sau farmacistului pentru recomandări înainte de a lua acest medicament. Nu se cunoaşte dacă MAXALT este dăunător fătului atunci când este utilizat de către o femeie gravidă. Alăptarea trebuie evitată timp de 24 ore după tratament. Copii şi adolescenţi Nu este recomandată utilizarea MAXALT la copii şi adolescenţi cu vârsta sub 18 ani. Utilizarea la vârstnici cu vârsta peste 65 ani Nu există studii complete în ceea ce priveşte siguranţa şi eficacitatea utilizării MAXALT la pacienţii cu vârstă peste 65 ani. Conducerea vehiculelor şi folosirea utilajelor Este posibil să fiţi somnolent sau ameţit în timpul utilizării MAXALT. Dacă acest lucru se întâmplă nu conduceţi vehicule şi nu folosiţi utilaje. Comprimatul de 5 mg conţine lactoză monohidrat 30,25 mg. Dacă medicul dumneavoastră v-a atenţionat că aveţi intoleranţă la unele categorii de glucide, vă rugăm să-l întrebaţi înainte de a lua acest medicament. 3
4 Comprimatul de 10 mg conţine lactoză monohidrat 60,50 mg. Dacă medicul dumneavoastră v-a atenţionat că aveţi intoleranţă la unele categorii de glucide, vă rugăm să-l întrebaţi înainte de a lua acest medicament. 3. Cum să luaţi MAXALT MAXALT este utilizat pentru tratamentul crizelor de migrenă. Luaţi MAXALT cât de repede posibil după ce a început durerea de cap din migrenă. Nu utilizaţi pentru a preveni o criză de migrenă. Luaţi întotdeauna acest medicament exact aşa cum v-a spus medicul dumneavoastră. Trebuie să discutaţi cu medicul dumneavoastră sau cu farmacistul dacă nu sunteţi sigur. Doza uzuală este de 10 mg. Dacă luaţi propanolol sau aveţi probleme cu rinichii sau ficatul trebuie să utilizaţi doza de 5 mg MAXALT. Trebuie să lăsaţi să treacă cel puţin 2 ore între utilizarea de propanolol şi MAXALT şi până puteţi utiliza maxim 2 doze într-o perioadă de 24 ore. Comprimatele de MAXALT (benzoat de rizatriptan) trebuie administrate oral şi înghiţite întregi cu lichid. MAXALT este de asemenea disponibil şi sub formă de liofilizat oral de 5 mg şi 10 mg care se dizolvă în gură. Liofilizatul oral poate fi utilizat în situaţia în care nu sunt disponibile lichide, sau pentru evita greaţa şi vărsăturile care pot acompania ingestia comprimatelor cu apă. Dacă migrena revine în decurs de 24 ore La unii pacienţi, simptomele de migrenă pot reveni într-o perioadă de 24 ore. Dacă migrena dumneavoastră revine puteţi folosi o doză suplimentară de MAXALT. Trebuie întotdeauna să aşteptaţi cel puţin 2 ore între doze. Dacă aveţi în continuare migrenă după 2 ore de la debut Dacă în timpul unei crize migrena nu răspunde la prima doză de MAXALT în timpul unei crize, nu trebuie să luaţi o a doua doză de MAXALT pentru tratamentul aceleaşi crize. Cu toate acestea, există posibilitatea ca MAXALT să vă ajute data viitoare când veţi avea migrenă. Nu luaţi mai mult de două doze de MAXALT într-o perioadă de 24 ore (de exemplu nu luaţi mai mult de două comprimate sau liofilizate orale de 10 mg sau de 5 mg într-o perioadă de 24 ore). Trebuie întotdeauna să aşteptaţi cel puţin 2 ore între doze. Dacă starea dumneavoastră se înrăutăţeşte, solicitaţi asistenţă medicală. Dacă luaţi mai mult MAXALT decât trebuie: Dacă luaţi mai mult MAXALT decât trebuie, adresaţi-vă imediat medicului dumneavoastră sau farmacistului. Luaţi ambalajul medicamentului cu dumneavoastră. Semnele supradozajului pot include ameţeală, somnolenţă, vărsături, leşin şi bătăi lente ale inimii. Dacă aveţi orice întrebări suplimentare cu privire la acest medicament, adresaţi-vă medicului dumneavoastră sau farmacistului. 4
5 4. Reacţii adverse posibile Ca toate medicamentele, acest medicament poate provoca reacţii adverse, cu toate că nu apar la toate persoanele. Următoarele reacții adverse pot apărea la utilizarea acestui medicament. În studiile clinice la adulţi, cele mai frecvente reacții adverse raportate au fost ameţeală, somnolenţă şi oboseală. Frecvente (care afectează 1 până la 10 utilizatori din 100) - furnicături (parestezie), durere de cap, scăderea sensibilităţii la nivelul pielii (hipoestezie), scăderea capacităţilor mintale, tremurături, insomnie. - bătăi rapide sau neregulate ale inimii (tahicardie). - înroşirea trecătoare a feţei (înroşirea feţei care durează o perioadă scurtă de timp), bufeuri, transpiraţii. - disconfort la nivelul gâtului. - senzaţie de rău (greaţă), uscăciune a gurii, vărsături, diaree, indigestie (dispepsie). - senzaţie de greutate în diferite părţi ale corpului, durere la nivelul gâtului, rigiditate. - durere la nivelul abdomenului sau pieptului. Mai puţin frecvent (care afectează1 până la 10 utilizatori din 1000) - gust rău în gură. - instabilitate la mers (ataxie), ameţeală (vertij), vedere înceţoşată, tremurături, leşin (sincopă). - confuzie, nervozitate. - tensiune arterială mare (hipertensiune arterială), sete, bufeuri, transpiraţii. - erupţie trecătoare pe piele; erupţie pe piele cu blânde şi senzaţie de mâncărime (urticarie); umflarea feţei, buzelor, limbii şi/sau a gâtului care poate determina dificultate în respiraţie şi/sau la înghiţire (angioedem), dificultate în respiraţie (dispnee). - durere la nivelul gâtului, senzaţie de constricţie în anumite părţi ale corpului, rigiditate, slăbiciune la nivelul muşchilor. - modificări ale ritmului sau frecvenţei bătăilor inimii (aritmii); anomalii ale electrocardiogramei (un test care înregistrează activitatea electrică a inimii dumneavoastră), ), bătăi foarte rapide ale inimii (tahicardie). - durere la nivelul feţei; dureri musculare. Rare (care afectează 1 până la 10 utilizatori din 10000) - leşin (sincopă). - respiraţie şuierătoare. - reacţii alergice (hipersensibilitate); reacţii alergice bruşte ameninţătoare de viaţă (anafilaxie). - accident vascular cerebral (acesta apare în general la pacienţii care prezintă factori de risc pentru afecţiuni ale inimii sau ale vaselor de sânge (tensiune arterială mare, diabet zaharat, fumători, utilizarea de tratament de substituţie pentru nicotină, istoric familial de afecţiuni ale inimii sau accident vascular cerebral, bărbat cu vârsta peste 40 ani, femei la postmenopauză, probleme speciale cu felul în care bate inima (bloc de ramură)). - bătăi încetinite ale inimii (bradicardie). Cu frecvenţă necunoscută (frecvenţa nu poate fi estimată din datele disponibile): - atac de cord, spasme ale vaselor de sânge de la nivelul inimii (acestea apar în general la pacienţii care prezintă factori de risc pentru afecţiuni ale inimii sau ale vaselor de sânge (tensiune arterială mare, diabet zaharat, fumători, utilizarea de tratament de substituţie pentru nicotină, istoric familial de afecţiuni ale inimii sau accident vascular cerebral, bărbat cu vârsta peste 40 ani, femei la postmenopauză, probleme speciale cu felul în care bate inima (bloc de ramură)). 5
6 - un sindrom numit "sindrom serotoninergic" care poate determina reacţii adverse cum sunt comă, tensiune arterială instabilă, temperatură a corpului extrem de mare, lipsa de coordonare musculară, agitaţie şi halucinaţii. - dezlipirea severă a pielii cu sau fără febră (necroliză epidermică toxică). - crize convulsive (convulsii). - spasme ale vaselor de sânge de la nivelul extremităţilor incluzând senzaţia de răceală şi amorţeală de la nivelul mâinilor sau a picioarelor. - spasme ale vaselor de sânge de la nivelul colonului (intestinul gros), care poate determina dureri abdominale. Spuneţi imediat medicului dumneavoastră dacă prezentaţi simptome ale reacţiilor alergice, sindromului serotoninergic, atacului de cord sau accidentului vascular cerebral. În plus, spuneţi medicului dumneavoastră dacă prezentaţi orice simptom care sugerează apariţia unei reacţii adverse (cum sunt erupţiile trecătoare pe piele sau mâncărime) după ce aţi luat MAXALT. Raportarea reacţiilor adverse Dacă manifestaţi orice reacţii adverse, adresaţi-vă medicului dumneavoastră sau farmacistului. Acestea includ orice reacţii adverse nemenţionate în acest prospect. De asemenea, puteţi raporta reacţiile adverse direct prin intermediul sistemului naţional de raportare, ale cărui detalii sunt publicate pe web-site-ul Agenţiei Naţionale a Medicamentului şi a Dispozitivelor Medicale Raportând reacţiile adverse, puteţi contribui la furnizarea de informaţii suplimentare privind siguranţa acestui medicament. 5. Cum se păstrează MAXALT Nu lăsaţi acest medicament la vederea şi îndemâna copiilor. Nu luaţi acest medicament după data de expirare înscrisă pe cutie/blister după EXP. Data de expirare se referă la ultima zi a lunii respective. A nu se păstra la temperaturi peste 30ºC. Nu aruncaţi niciun medicament pe calea apei sau a reziduurilor menajere. Întrebaţi farmacistul cum să aruncaţi medicamentele pe care nu le mai folosiţi. Aceste măsuri vor ajuta la protejarea mediului. 6. Conţinutul ambalajului şi alte informaţii Ce conţine MAXALT Substanţa activă din MAXALT este rizatriptanul. Un comprimat conţine rizatriptan 5 mg sub formă de benzoat de rizatriptan 7,265 mg. Substanţa activă din MAXALT este rizatriptanul. Un comprimat conţine rizatriptan 10 mg sub formă de benzoat de rizatriptan 14,53 mg. Celelalte componente sunt lactoză monohidrat, celuloză microcristalină (E 460a),amidon pregelatinizat, oxid roşu de fer (E 172) şi stearat de magneziu (E 572). 6
7 Cum arată MAXALT şi conţinutul ambalajului Comprimatele de 5 mg au formă de capsulă, sunt de culoare roz deschis, inscripţionate pe o parte cu MSD şi pe cealaltă parte cu 266. Comprimatele de 10 mg au formă de capsulă, sunt de culoare roz deschis, inscripţionate pe o parte cu MAXALT şi pe cealaltă parte cu MSD 267. Mărimi de ambalaj: Cutii cu 2, 3, 6, 12, 18 comprimate. Este posibil ca nu toate mărimile de ambalaj să fie comercializate. Deţinătorul autorizaţiei de punere pe piaţă şi fabricantul Deţinătorul autorizaţiei de punere pe piaţă MERCK SHARP & DOHME ROMANIA S.R.L. Bucharest Business Park Şoseaua Bucureşti-Ploieşti Nr. 1A, Clădirea C1, Etaj 3, Sector 1, Bucureşti, România Fabricantul MERCK SHARP & DOHME B.V. Waarderweg BN Haarlem Olanda Acest medicament este autorizat în Statele Membre ale Spaţiului Economic European sub următoarele denumiri comerciale: Austria, Cipru, Estonia, Finlanda, Franţa, Grecia, Islanda, Letonia, Malta, Marea Britanie, Norvegia, Olanda, Polonia, Portugalia, Suedia Belgia, Luxemburg Bulgaria Republica Cehă Danemarca Germania Irlanda Italia Lituania România Slovacia Slovenia Ungaria MAXALT MAXALT 5 mg МAКСАЛТ 5 mg таблетки MAXALT 5 mg, tablety MAXALT, tabletter MAXALT 5 mg Tabletten Rizatriptan MSD 5 mg Tablets MAXALT 5 mg compresse MAXALT 5 mg tabletės Rizalief 5 mg Maxalt 5 mg tablete MAXALT 5 mg tabletta 7
8 Austria, Cipru, Estonia, Finlanda, Franţa, Grecia, Islanda, Letonia, Malta, Marea Britanie, Norvegia, Olanda, Polonia Portugalia şi Suedia Belgia, Luxemburg şi Spania Bulgaria Republica Cehă Danemarca Germania Irlanda Italia Lituania România Slovacia Slovenia Ungaria MAXALT MAXALT 10 mg МAКСАЛТ 10 mg таблетки MAXALT 10 mg, tablety MAXALT, tabletter MAXALT 10 mg Tabletten Rizatriptan MSD 10 mg Tablets MAXALT 10 mg compresse MAXALT 10 mg tabletės Rizalief 10 mg Maxalt 10 mg tablete MAXALT 10 mg tabletta Acest prospect a fost revizuit în Iulie
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
VISINE®
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6026/2013/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Osetron 4 mg comprimate filmate Ondansetron Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6026/2013/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Osetron 4 mg comprimate filmate Ondansetron Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progeste
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7218/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lutinus 100 mg comprimate vaginale Progesteron Citiţi cu atenţie şi în întregime acest prospect
PRO_3712_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
simva leaflet
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2786/2010/01-02-03-04-05-06 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Escepran 25 mg comprimate filmate Exemestan Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/ Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7264/2014/01-02-03-04-05 Anexa 1 Prospect Prospect: informaţii pentru utilizator Betaserc 24 mg comprimate orodispersabile Diclorhidrat de betahistină Citiţi cu atenţie
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a înc
 Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru utilizator Imodium 2mg, capsule Clorhidrat de loperamidă Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
PRO_4804_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4064/2011/01-02-03-04-05-06-07 NR. 4065/2011/01-02-03-04-05-06-07 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Asolfena 5 mg comprimate filmate Asolfena 10
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg co
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6652/2006/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator LERIDIP 20 mg comprimate filmate Clorhidrat de lercanidipină Citiţi
PRO_4755_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4755/2012/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Technescan PYP 20 mg kit pentru preparat radiofarmaceutic Pirofosfat de sodiu decahidrat Citiţi cu
PRO_900_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 900 /2008/01-02-03 Anexa 1 Prospect PROSPECT: Informaţii pentru utilizator Brival 125 mg comprimate Brivudină Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 900 /2008/01-02-03 Anexa 1 Prospect PROSPECT: Informaţii pentru utilizator Brival 125 mg comprimate Brivudină Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/ Anexa /2012/ /2012/ Prospect Prospect: Informaţii pe
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4957/2012/01-02-03-04-05 Anexa 1 4958/2012/01-02-03-04-05 4959/2012/01-02-03-04-05 Prospect Prospect: Informaţii pentru utilizator Sildenafil Dr. Reddy s 25 mg comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN,
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN, 10 mg, comprimate filmate CITALORAN, 20 mg, comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7362/2006/01 Anexa 1' NR. 7363/2006/01 NR. 7364/2006/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CITALORAN, 10 mg, comprimate filmate CITALORAN, 20 mg, comprimate
PARTICULARS TO APPEAR ON <THE OUTER PACKAGING> <AND> <THE IMMEDIATE PACKAGING>
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4586/2012/01-02-03-04-05-06-07-08-09-10 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Doreta 75 mg/650 mg comprimate filmate Clorhidrat de tramadol/paracetamol
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4586/2012/01-02-03-04-05-06-07-08-09-10 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Doreta 75 mg/650 mg comprimate filmate Clorhidrat de tramadol/paracetamol
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabil
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabile Montelukast Pentru copii cu vârsta cuprinsă între
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3155/2011/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Montelukast Alvogen 4 mg comprimate masticabile Montelukast Pentru copii cu vârsta cuprinsă între
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6637/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DIAZEPAM 10 mg comprimate Diazepam Citiţi cu atenţie şi în întregime acest prospect înainte de a
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6637/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DIAZEPAM 10 mg comprimate Diazepam Citiţi cu atenţie şi în întregime acest prospect înainte de a
AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg c
 AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg comprimate filmate Capecitabină Actavis 500 mg comprimate
AUTORIZATIE DE PUNERE PE PIATA NR. 5177/2012/01 Anexa 1 NR. 5178/2012/01 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Capecitabină Actavis 150 mg comprimate filmate Capecitabină Actavis 500 mg comprimate
B
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3872/2011/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru pacient 25 mg comprimate filmate Sildenafil Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3872/2011/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru pacient 25 mg comprimate filmate Sildenafil Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule
 AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule pentru suspensie orală Keflex 250 mg/5 ml granule
AUTORIZATIE DE PUNERE PE PIAŢĂ NR. 5294/2005/01-02, 5295/2005/01-02 Anexa 1 Prospect Prospect: Informații pentru utilizator Keflex 125 mg/5 ml granule pentru suspensie orală Keflex 250 mg/5 ml granule
PACKAGE LEAFLET: INFORMATION FOR THE USER
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4997/2012/01-02-03-04-05-06 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Levelanz 500 mg comprimate filmate Levetiracetam Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4997/2012/01-02-03-04-05-06 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Levelanz 500 mg comprimate filmate Levetiracetam Citiţi cu atenţie şi în întregime
PRO_1053_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1053/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator NEBIVOLOL TERAPIA 5 mg comprimate Nebivolol Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1053/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator NEBIVOLOL TERAPIA 5 mg comprimate Nebivolol Citiţi cu atenţie şi în întregime acest prospect
AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extrac
 AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extract uscat de Hyperici herba (iarbă de sunătoare) Ze 117
AUTORIZATIE DE PUNERE PE PIATĂ NR. 8271/2015/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator REMOTIV 250 mg comprimate filmate Extract uscat de Hyperici herba (iarbă de sunătoare) Ze 117
PRO_715_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 715/2008/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PRONORAN 50 mg drajeuri cu eliberare prelungită Piribedil Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 715/2008/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PRONORAN 50 mg drajeuri cu eliberare prelungită Piribedil Citiţi cu atenţie şi în întregime acest
Проспект: Информация для пациента, потребителя
 Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
Prospect: Informaţii pentru consumator/pacient Duphalac 667 mg/ml, soluţie orală Lactuloză Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece conţine
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9213/2016/01-02-03-04-05 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dutasteridă Zentiva 0,5 mg capsule moi Dutasteridă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/ Anexa /2012/ Prospect Prospect: Informaţii pentru pacient
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/01-02-03-04-05-06-07 Anexa 1 5210/2012/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Telmotens 40 mg comprimate filmate Telmotens 80 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5209/2012/01-02-03-04-05-06-07 Anexa 1 5210/2012/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Telmotens 40 mg comprimate filmate Telmotens 80 mg
AUTORIZATIE DE PUNERE PE PIATA NR
 AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 43/2007/01; 44/2007/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU PACIENT CAPTOPRIL LPH 25 mg comprimate CAPTOPRIL LPH 50 mg comprimate Captopril Citiţi cu atenţie
AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 43/2007/01; 44/2007/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU PACIENT CAPTOPRIL LPH 25 mg comprimate CAPTOPRIL LPH 50 mg comprimate Captopril Citiţi cu atenţie
PRO_671_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 671/2008/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIBROCIL ACTILONG MENTOL 1 mg/ml spray nazal cu doze măsurate soluţie Clorhidrat de xilometazolină
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu aten
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9184/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Ketof 1 mg/5 ml sirop Ketotifen Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin n
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10302/2017/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator VENTOLIN 5 mg/ml soluţie de inhalat prin nebulizator Salbutamol Citiţi cu atenţie şi în întregime
RGD: 57144/E/2
 Prospect: Informaţii pentru consumator/pacient KLION-D 100 comprimate vaginale Metronidazolum/Miconazolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament
Prospect: Informaţii pentru consumator/pacient KLION-D 100 comprimate vaginale Metronidazolum/Miconazolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator Quodixor 150 mg comprimate filmate Acid iba
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator 150 mg comprimate filmate Acid ibandronic Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3157/2011/01-02 Anexa 1 Prospect Prospect: informaţii pentru utilizator 150 mg comprimate filmate Acid ibandronic Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofi
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2018/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefixim
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 10962/2018/01-02-03 Anexa 1 Prospect Prospect: Informaţii pentru utilizator XIFIA 400 mg comprimate filmate cefiximă Citiţi cu atenţie şi în întregime acest prospect
PRO_837_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 837/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator Diclac 50 mg/g gel Diclofenac sodic Citiţi cu atenţie şi în întregime acest prospect înainte de
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 837/2008/01-02 Anexa 1' Prospect Prospect: Informaţii pentru utilizator Diclac 50 mg/g gel Diclofenac sodic Citiţi cu atenţie şi în întregime acest prospect înainte de
Microsoft Word _Perfalgan 100ml_UK PIL_II-44+ UT.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6274/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Paracetamol Sandoz 10 mg/ml soluţie perfuzabilă Paracetamol Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/ Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-b
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-butilamină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3177/2011/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR PERYL 8 mg comprimate Perindopril terţ-butilamină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa /2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 40
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa 1 9495/2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 400 mg capsule Gabapentină Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9494/2016/01 Anexa 1 9495/2016/01 Prospect Prospect: Informaţii pentru utilizator Gabaran 300 mg capsule Gabaran 400 mg capsule Gabapentină Citiţi cu atenţie şi în întregime
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
Denumirea comercială, forma farmaceutică şi concentraţia
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6396/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Azitromicină Terapia 250 mg comprimate filmate Azitromicină Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6396/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Azitromicină Terapia 250 mg comprimate filmate Azitromicină Citiţi cu atenţie şi în întregime
ANEXA II
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4133/2011/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR AKINETON 2 mg comprimate Clorhidrat de biperiden Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4133/2011/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR AKINETON 2 mg comprimate Clorhidrat de biperiden Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 9
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 90 mg retard, comprimate cu eliberare prelungită Diltiazem
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.5926/2005/01; 5927/2005/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR DILZEM 60 mg, comprimate DILZEM 90 mg retard, comprimate cu eliberare prelungită Diltiazem
AUTORIZATIE DE PUNERE PE PIATA NR
 AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
AUTORIZATIE DE PUNERE PE PIATA NR. 7550/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIROLEX 250 mg pulbere pentru soluţie injectabilă/perfuzabilă Aciclovir Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentr
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentru soluţie injectabilă Gonadotrofină corionică umană
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7695/2014/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator PREGNYL 5000 UI/ml pulbere şi solvent pentru soluţie injectabilă Gonadotrofină corionică umană
PRO_202_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 202/2007/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Amiodaronă LPH 200 mg, comprimate Clorhidrat de amiodaronă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 202/2007/01-02-03 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Amiodaronă LPH 200 mg, comprimate Clorhidrat de amiodaronă Citiţi cu atenţie şi în întregime
REZUMATUL CARACTERISTICILOR PRODUSULUI
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 11591/2019/01-02-03-04-05 Anexa 2 11592/2019/01-02-03-04-05 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 11591/2019/01-02-03-04-05 Anexa 2 11592/2019/01-02-03-04-05 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
PRO_2078_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2078/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Duphaston 10 mg comprimate filmate Didrogesteron Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2078/2009/01-02 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Duphaston 10 mg comprimate filmate Didrogesteron Citiţi cu atenţie şi în întregime acest prospect
PRO_3436_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3436/2011/01-20 Anexa 1' 3437/2011/01-20 3438/2011/01-20 3439/2011/01-20 Prospect Prospect: Informaţii pentru utilizator Bisoprolol fumarat Mylan 1,25 mg comprimate filmate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3436/2011/01-20 Anexa 1' 3437/2011/01-20 3438/2011/01-20 3439/2011/01-20 Prospect Prospect: Informaţii pentru utilizator Bisoprolol fumarat Mylan 1,25 mg comprimate filmate
PRO_10425_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.10425/2017/01-12 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lorista HCT 100 mg/12,5 mg comprimate filmate Losartan potasic/hidroclorotiazidă Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR.10425/2017/01-12 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lorista HCT 100 mg/12,5 mg comprimate filmate Losartan potasic/hidroclorotiazidă Citiţi cu atenţie
PRO_11765_ doc
 AUTORIZATIE DE PUNERE PE PIATA NR. 11765/2019/01-02-03-04 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dostinex 0,5 mg comprimate Cabergolină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZATIE DE PUNERE PE PIATA NR. 11765/2019/01-02-03-04 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Dostinex 0,5 mg comprimate Cabergolină Citiţi cu atenţie şi în întregime acest prospect
PRO_6774_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6774/2006/01-02-03 Anexa 1 6775/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iopamiro 300, soluţie injectabilă, 612,4 mg/m Iopamiro 370, soluţie injectabilă,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6774/2006/01-02-03 Anexa 1 6775/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iopamiro 300, soluţie injectabilă, 612,4 mg/m Iopamiro 370, soluţie injectabilă,
PROSPECT: INFORMAŢII PENTRU UTILIZATOR
 PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT AQUADETRIM VITAMINA D 3, 15 000 UI/ml, picături orale, soluţie Cholecalciferolum Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să
PRO_278_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 278/2007/01-09 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR STAMARIL Pulbere și solvent pentru suspensie injectabilă în seringă preumplută Vaccin pentru febra
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 278/2007/01-09 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR STAMARIL Pulbere și solvent pentru suspensie injectabilă în seringă preumplută Vaccin pentru febra
Microsoft Word - 1st year leaflet_ROM
 Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
Vaccinuri pentru a vă proteja copilul împotriva HPV, MenACWY şi Tdap Informaţii pentru părinţi şi elevii care încep liceul în 2019 Despre această broşură Această broşură este destinată părinţilor şi elevilor
PRO_6096_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6094/2014/01-02-03-04 Anexa 1 6095/2014/01-02-03-04 6096/2014/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Concor Cor 2,5 mg comprimate filmate Concor
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6094/2014/01-02-03-04 Anexa 1 6095/2014/01-02-03-04 6096/2014/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Concor Cor 2,5 mg comprimate filmate Concor
PRO_3425_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3425/2011/01 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR BETADERM 1 mg/g unguent Betametazonă valerat Citiţi cu atenţie şi în întregime acest prospect înainte
Certificat de înregistrare al medicamentului nr din nr din Modificare din la anexa 1 PROSPECT: INFORMAŢ
 Certificat de înregistrare al medicamentului nr. 21309 din 25.11.2014 nr. 21308 din 25.11.2014 Modificare din 10.12.2015 la anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR Co-Sentor 50 mg/12,5 mg comprimate
Certificat de înregistrare al medicamentului nr. 21309 din 25.11.2014 nr. 21308 din 25.11.2014 Modificare din 10.12.2015 la anexa 1 PROSPECT: INFORMAŢII PENTRU UTILIZATOR Co-Sentor 50 mg/12,5 mg comprimate
08/06/2015 MD/C/500/1 Prospect: Informaţii pentru utilizator MILDRONAT 500 mg capsule Meldonium Citiţi cu atenţie şi în întregime acest prospect înain
 08/06/2015 MD/C/500/1 Prospect: Informaţii pentru utilizator MILDRONAT 500 mg capsule Meldonium Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece
08/06/2015 MD/C/500/1 Prospect: Informaţii pentru utilizator MILDRONAT 500 mg capsule Meldonium Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament, deoarece
AUTORIZATIE DE PUNERE PE PIATĂ NR
 Certificat de înregistrare al medicamentului - nr. 21488 din 22.01.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU PACIENT Indapamid LPH 1,5 mg comprimate cu eliberare prelungită Indapamidă Citiţi cu atenţie
Certificat de înregistrare al medicamentului - nr. 21488 din 22.01.2015 Anexa 1 PROSPECT: INFORMAŢII PENTRU PACIENT Indapamid LPH 1,5 mg comprimate cu eliberare prelungită Indapamidă Citiţi cu atenţie
PRO_3961_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3961/2011/01 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ibuprofen Arena 400 mg capsule Ibuprofen Citiţi cu atenţie şi în întregime acest prospect, deoarece
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3961/2011/01 Anexa 1` Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ibuprofen Arena 400 mg capsule Ibuprofen Citiţi cu atenţie şi în întregime acest prospect, deoarece
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el con
 PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el conţine informaţii importante pentru dumneavoastră Luaţi
PROSPECT: INFORMAŢII PENTRU CONSUMATOR / PACIENT Diclofenac 10 mg/g gel Diclofenacum Citiţi cu atenţie şi în întregime acest prospect, deoarece el conţine informaţii importante pentru dumneavoastră Luaţi
ANEXA II
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7270/2014/01-02-03-04-05-06-07-08-09 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Voltaren Forte 23,2 mg/g gel Diclofenac dietilamină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7270/2014/01-02-03-04-05-06-07-08-09 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Voltaren Forte 23,2 mg/g gel Diclofenac dietilamină Citiţi cu atenţie şi
PRO_4616_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4616/2004/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator FEVARIN 50 mg comprimate filmate Maleat de fluvoxamină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4616/2004/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator FEVARIN 50 mg comprimate filmate Maleat de fluvoxamină Citiţi cu atenţie şi în întregime acest prospect
PRO_6705_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6705/2006/01 Anexa 1 6706/2006/01 6707/2006/01 Prospect Prospect: Informaţii pentru utilizator Accuzide 10 mg/12,5 mg comprimate filmate Accuzide Forte 20 mg/12,5 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6705/2006/01 Anexa 1 6706/2006/01 6707/2006/01 Prospect Prospect: Informaţii pentru utilizator Accuzide 10 mg/12,5 mg comprimate filmate Accuzide Forte 20 mg/12,5 mg
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate fil
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/01-02-03-04-05-06-07 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate filmate Ibuprofen Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7460/2015/01-02-03-04-05-06-07 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 400 mg comprimate filmate Ibuprofen Citiţi cu atenţie şi în întregime acest
PRO_7051_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7051/2014/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7051/2014/01-02-03-04-05-06-07-08-09-10-11 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Symbicort Turbuhaler 160 micrograme/4,5 micrograme/inhalaţie, pulbere
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
PRO_6041_6042__2013_7_var_2__2018_7.doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6041/2013/01-02-03-04-05-06-07 Anexa 1 6042/2013/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Algoxib 100 mg capsule Algoxib 200 mg capsule celecoxib
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6041/2013/01-02-03-04-05-06-07 Anexa 1 6042/2013/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Algoxib 100 mg capsule Algoxib 200 mg capsule celecoxib
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie injectabilă Sulfat de atropină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1266/2008/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Sulfat de atropină Takeda 1 mg/ml, soluţie injectabilă Sulfat de atropină Citiţi cu atenţie şi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9256/2016/01-17 Anexa 1 Prospect Prospect: Informaţii pentru utilizator CIPRALEX 10 mg comprimate filmate Escitalop
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9256/2016/01-17 Anexa 1 Prospect Prospect: Informaţii pentru utilizator CIPRALEX 10 mg comprimate filmate Escitalopram Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9256/2016/01-17 Anexa 1 Prospect Prospect: Informaţii pentru utilizator CIPRALEX 10 mg comprimate filmate Escitalopram Citiţi cu atenţie şi în întregime acest prospect
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI!
 Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
Agenţia Naţională pentru Ocuparea Forţei de Muncă Valorifică pentru viitor ORICE perioadă lucrată ORIUNDE în SEE! INVESTEŞTE ÎN OAMENI! Reglementări Regulamentul CE 883/2004 privind coordonarea sistemelor
PRO_6337_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6337/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DICLOFENAC 50 mg comprimate gastrorezistente Diclofenac sodic Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6337/2006/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator DICLOFENAC 50 mg comprimate gastrorezistente Diclofenac sodic Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa /2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml gran
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa 1 8634/2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml granule pentru suspensie orală CEFALEXIN SANDOZ 250 mg/5
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8633/2016/01 Anexa 1 8634/2016/01 Prospect Prospect: Informaţii pentru utilizator CEFALEXIN SANDOZ 125 mg/5 ml granule pentru suspensie orală CEFALEXIN SANDOZ 250 mg/5
PRO_9516_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9516/2016/01-24 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIMOVO 500 mg/20 mg comprimate cu eliberare modificată naproxen şi esomeprazol Citiţi cu atenţie
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9516/2016/01-24 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR VIMOVO 500 mg/20 mg comprimate cu eliberare modificată naproxen şi esomeprazol Citiţi cu atenţie
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7459/2015/ Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 20 mg/ml suspensie orală
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7459/2015/01-02-03-04-05-06 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 20 mg/ml suspensie orală Ibuprofen Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7459/2015/01-02-03-04-05-06 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Brufen 20 mg/ml suspensie orală Ibuprofen Citiţi cu atenţie şi în întregime acest
PRO_7170_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7169/2014/01-02-03-04-05-06 Anexa 1 7170/2014/01-02-03-04-05-06 7171/2014/01-02-03-04-05-06 7172/2014/01-02-03-04-05-06 Prospect Prospect: Informaţii pentru utilizator
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7169/2014/01-02-03-04-05-06 Anexa 1 7170/2014/01-02-03-04-05-06 7171/2014/01-02-03-04-05-06 7172/2014/01-02-03-04-05-06 Prospect Prospect: Informaţii pentru utilizator
PRO_6878_ doc
 AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 6878/2006/01-02-03-04-05; Anexa 1 6879/2006/01-02-03-04 6880/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iomeron 300, soluţie injectabilă, 612,4
AUTORIZAȚIE DE PUNERE PE PIAȚĂ NR. 6878/2006/01-02-03-04-05; Anexa 1 6879/2006/01-02-03-04 6880/2006/01-02-03-04 Prospect Prospect: Informaţii pentru utilizator Iomeron 300, soluţie injectabilă, 612,4
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofi
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofibrat Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9126/2016/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Lipantil Nano 145 mg comprimate filmate Fenofibrat Citiţi cu atenţie şi în întregime acest prospect
PRO_5945_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5945/2005/01 Anexa 1 Prospect Prospect: Informații pentru utilizator DOXICICLINA SANDOZ 100 mg capsule Clorhidrat de doxiciclină Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5945/2005/01 Anexa 1 Prospect Prospect: Informații pentru utilizator DOXICICLINA SANDOZ 100 mg capsule Clorhidrat de doxiciclină Citiţi cu atenţie şi în întregime acest
SPC in English
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3864/2011/01-20 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1.DENUMIREA COMERCIALĂ A MEDICAMENTULUI Molaxole pulbere pentru
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7596/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ketonal Retard 150 mg comprimate cu eliberare
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7596/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ketonal Retard 150 mg comprimate cu eliberare prelungită Ketoprofen Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7596/2006/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR Ketonal Retard 150 mg comprimate cu eliberare prelungită Ketoprofen Citiţi cu atenţie şi în întregime
PRO_1745_ docx
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1745/2009/01 Anexa 1 1746/2009/01-13 Prospect Prospect: Informaţii pentru utilizator Lamictal 2 mg comprimate masticabile/dispersabile Lamictal 5 mg comprimate masticabile/dispersabile
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 1745/2009/01 Anexa 1 1746/2009/01-13 Prospect Prospect: Informaţii pentru utilizator Lamictal 2 mg comprimate masticabile/dispersabile Lamictal 5 mg comprimate masticabile/dispersabile
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9028/2016/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Norfloxacin Helcor 400 mg comprimate filmat
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9028/2016/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Norfloxacin Helcor 400 mg comprimate filmate Norfloxacină Citiţi cu atenţie şi în întregime acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 9028/2016/01-02 Anexa 1 Prospect Prospect: Informaţii pentru utilizator Norfloxacin Helcor 400 mg comprimate filmate Norfloxacină Citiţi cu atenţie şi în întregime acest
COMISIA EUROPEANĂ Bruxelles, COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea
 COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
COMISIA EUROPEANĂ Bruxelles, 28.3.2019 COM(2019) 157 final RAPORT AL COMISIEI CĂTRE CONSILIU privind progresele înregistrate de statele membre în ceea ce privește aderarea la Convenția internațională a
PRO_886_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 885/2008/01 Anexa 1' 886/2008/01 887/2008/01 Prospect Prospect: Informaţii pentru utilizator Seretide Inhaler CFC-Free 25 micrograme/50 micrograme suspensie de inhalat
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 885/2008/01 Anexa 1' 886/2008/01 887/2008/01 Prospect Prospect: Informaţii pentru utilizator Seretide Inhaler CFC-Free 25 micrograme/50 micrograme suspensie de inhalat
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
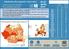 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
Arterita Takayasu Arterita Takayasu Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 Arterita Takayasu
 Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
Tradusă de Georgiana Elena Stoian după Cleveland clinic, accesată pe 22 iulie 2019 este o formă de vasculită în care vasele mari și mijlocii sunt inflamate și deteriorate. Corticosteroizii sunt prima linie
ЗАТВЕРДЖЕНО
 Prospect: Informaţii pentru consumator/pacient Celestoderm-V 1 mg/gram unguent Betametazonă (de betametazonă 17-valerat) Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi
Prospect: Informaţii pentru consumator/pacient Celestoderm-V 1 mg/gram unguent Betametazonă (de betametazonă 17-valerat) Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi
PRO_7026_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7026/2014/01-02-03-04-05-06-07 Anexa 1 7027/2014/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Lipocomb 10 mg/10 mg capsule Lipocomb 20 mg/10 mg capsule
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 7026/2014/01-02-03-04-05-06-07 Anexa 1 7027/2014/01-02-03-04-05-06-07 Prospect Prospect: Informaţii pentru pacient Lipocomb 10 mg/10 mg capsule Lipocomb 20 mg/10 mg capsule
Furosemide Vitabalans Annex I_II_ro
 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6560/2014/01-12 Anexa 1 Prospect Prospect: Informaţii pentru pacient Moflaxa 400 mg comprimate filmate Moxifloxacin
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6560/2014/01-12 Anexa 1 Prospect Prospect: Informaţii pentru pacient Moflaxa 400 mg comprimate filmate Moxifloxacină Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 6560/2014/01-12 Anexa 1 Prospect Prospect: Informaţii pentru pacient Moflaxa 400 mg comprimate filmate Moxifloxacină Citiţi cu atenţie şi în întregime acest prospect
PRO_2214_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2214/2009/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR ZOLADEX 3,6 mg implant goserelină Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2214/2009/01 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR ZOLADEX 3,6 mg implant goserelină Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
