Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
|
|
|
- Voicu Mocanu
- 4 ani în urmă
- Vzualizari:
Transcriere
1 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: INSULINUM DEGLUDEC INDICAŢIA: TRATAMENTUL DIABETULUI ZAHARAT LA ADULȚI Data depunerii dosarului Număr dosar PUNCTAJ: 85
2 1. DATE GENERALE 1.1. DCI: Insulinum degludec 1.2. DC: Tresiba 100 unități/ml soluție injectabilă în cartuș 1.3 Cod ATC: A10AE Data eliberării APP: 21 ianuarie Deținătorul APP: NOVO NORDISK A/S DANEMARCA-reprezentată prin NOVO NORDISK FARMA SRL 1.6. Tip DCI: nou 1.7. Forma farmaceutica, concentratia, calea de administrare, marimea ambalajului Forma farmaceutică Concentraţia Calea de administrare Mărimea ambalajului Soluție injectabilă (Penfil) 100 unități/ml subcutanată Cutie cu 5 cartușe X 3ml de soluție în cartuș 1.8. Preț conform Ordinului ministrului sănătății nr din 21 noiembrie 2018 Preţul cu amănuntul pe ambalaj 292,71 lei Preţul cu amănuntul pe unitatea terapeutică 58,54 lei 1.9. Indicația terapeutică și doza de administrare conform RCP Tresiba 100 unități/ml soluție injectabilă în cartuș Indicaţie terapeutică Doza recomandată Durata medie a tratamentului conform RCP Tresiba 100 unități/ml soluție injectabilă este indicată în tratamentul diabetului zaharat la adulți, la adolescenți și copii de la vârsta de 1 an. La pacienţii cu diabet de tip 2: Tresiba poate fi administrat în monoterapie sau în oricare asociere cu medicamente antidiabetice orale, agoniști de receptor GLP-1 sau insulină de tip bolus. Iniţierea tratamentului: Pacienţi cu diabet zaharat de tip 2 : doza zilnică recomandată pentru inițierea tratamentului este de 10 unităţi urmată de ajustări individuale ale dozei. Pacienţi cu diabet zaharat de tip 1: Tresiba este recomandat o dată pe zi, în asociere cu insulina prandială şi necesită ajustări ulterioare individuale ale dozei. Trecerea de la administrarea altor medicamente pe bază de insulină: Se recomandă supravegherea atentă a glicemiei în timpul trecerii şi în săptămânile următoare. Este posibil să fie nevoie de ajustarea dozelor sau a Nu se menționează.
3 La pacienţii cu diabet de tip 1: Tresiba trebuie asociat cu insuline cu acţiune scurtă/rapidă pentru a acoperi necesarul de insulină în timpul meselor. o o momentul administrării insulinelor cu acţiune rapidă sau cu durată scurtă de acţiune asociate sau altor tratamente antidiabetice concomitente. Pacienţi cu diabet zaharat de tip 2 în tratament cu insulină în regim bazal, bazalbolus în doză unică, premixat sau auto-mixat, schimbarea insulinei bazale cu Tresiba se poate face unitate la unitate, pe baza dozelor anterioare de insulină bazală, urmată de ajustări individuale ale dozei. se va lua în considerare o scădere a dozei cu 20% pe baza dozei de insulină bazală anterioară, urmată de ajustări indiviuale de doză la: - schimbarea insulinei bazale administrate de două ori pe zi cu Tresiba; - schimbarea insulinei glargin (300 unități/ml) cu Tresiba. Pacienţi cu diabet zaharat de tip 1 - se va lua în considerare o scădere a dozei cu 20% pe baza dozelor anterioare de insulină bazală sau componentei bazale dintr-un tratament perfuzabil subcutanat cu insulină, cu ajustări individuale subsecvente ale dozei în funcție de răspunsul glicemic. Utilizarea Tresiba în asociere cu agoniști de receptor GLP-1 la pacienți cu diabet zaharat tip 2: În cazul asocierii Tresiba la agoniştii de receptor GLP-1 doza zilnică recomandată este de 10 unități și se ajustează apoi individual. În cazul asocierii agoniştilor de receptor GLP-1 la Tresiba se recomandă reducerea dozei de Tresiba cu 20% pentru a micșora riscul de hipoglicemie. După aceea, doza se ajustează individual. Tresiba trebuie administrat în doze conform nevoilor individuale ale pacienţilor. Se recomandă ca ajustările de doze să se bazeze în primul rând pe măsurătorile glicemiei
4 efectuate în condiții de repaus alimentar. Poate fi necesară ajustarea dozei dacă pacienţii depun efort fizic crescut, îşi schimbă dieta uzuală sau în timpul bolilor concomitente. Potenţa analogilor de insulină, inclusiv a insulinei degludec, este exprimată în unităţi. O (1) unitate de insulină degludec corespunde la 1 unitate internaţională de insulină umană, 1 unitate de insulină glargin (100 unităţi/ml) sau 1 unitate de insulină detemir. Pacienţi vârstnici (cu vârstă de 65 de ani și peste): Tresiba poate fi utilizat la vârstnici. Monitorizarea glicemiei trebuie intensificată şi doza ajustată în funcţie de necesităţile individuale. Insuficienţă renală și hepatică: Tresiba poate fi utilizat la pacienţii cu insuficienţă hepatică sau renală. Monitorizarea glicemiei trebuie intensificată şi doza ajustată în funcţie de necesităţile individuale. Copii şi adolescenţi: Nu există experienţă clinică privind utilizarea acestui medicament la copii cu vârsta sub 1 an. Acest medicament poate fi utilizat la adolescenţi şi copii de la vârsta de 1 an. Când se trece de la insulina bazală la Tresiba, se va considera în mod individual reducerea dozei de insulină bazală și bolus în scopul scăderii riscului de hipoglicemie. Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru insulinum degludec este de 40 unități. 2. EVALUĂRI HTA INTERNAȚIONALE 2.1. ETM bazată pe estimarea beneficiului terapeutic (SMR) - HAS Autorităţile franceze compentente au publicat două rapoarte de evaluare referitor la medicamentul cu DC Tresiba 100 unități/ml soluție injectabilă în cartuș, după cum urmează: Data Referință Indicație SMR CT12822 CT16983 Tratamentul diabetului zaharat tip 1 și 2 la adulți. Tratamentul diabetului zaharat de tip 1 la adolescenți și copii de la 1 an. Important Important
5 Primul raport de evaluare a fost publicat pe site-ul oficial francez la data de 02 aprilie Comisia a concluzionat că: Beneficiul terapeutic estimat (SMR ) adus de Tresiba 100 unități/ml soluție injectabilă în cartuș este important în tratamentul diabetului zaharat tip 1 și 2 la adulți. Tresiba nu aduce o îmbunătățire a beneficiului terapeutic adițional (ASMR V, inexistent ) comparativ cu analogii de insulină cu acțiune prelungită (LANTUS și LEVEMIR), în tratamentul diabetului zaharat tip 1 și 2 la adulți. Comisia de Transparenta a dat aviz favorabil pentru utilizarea în spital și pentru includerea Tresiba în sistemul de compensare. Procentul de rambursare propus pentru această indicație a fost de 65%. Experții au concluzionat că: În diabetul de tip 1 la adulți, comparatorii relevanți din punct de vedere clinic pentru insulina degludec (TRESIBA) sunt următorii: insulinele utilizate ca insuline bazale într-un regim bazal-bolus sau într-un regim cu 2 până la 5 injecții pe zi (insulină NPH cu acțiune intermediară sau insulină glargin LANTUS, insulină detemir LEVEMIR), în asociere cu o insulină sau un analog cu acțiune rapidă sau ultrarapidă*, insulinele administrate ca insuline bazale prin intermediul unei pompe portabile sub-cutanate (insulină sau analog cu acțiune rapidă). În diabetul de tip 2 la adulți, comparatorii relevanți din punct de vedere clinic pentru insulina degludec sunt următorii: în momentul instituirii insulino-terapiei: insulinele utilizate ca insuline bazale injectabile o dată pe zi (insulină NPH cu acțiune intermediară sau insulină glargine- LANTUS, insulină detemir -LEVEMIR) sau de două ori pe zi (LEVEMIR), și în asociere cu cel puțin un antidiabetic oral; în momentul instituirii unei scheme intensificate de insulină: - insulinele utilizate ca insuline bazale într-un regim bazal-bolus (insulină NPH cu acțiune intermediară sau insulină glargine - LANTUS, insulină detemir - LEVEMIR), în asociere cu o insulină sau un analog cu acțiune rapidă sau ultrarapidă*, - insulinele amestecate (sau pre-mixate) administrate în 1 până la 3 injecții pe zi. * Insulină NPH cu acțiune intermediară sau insulină detemir LEVEMIR. Poziția în strategia terapeutică În diabetul de tip 1, TRESIBA poate fi utilizată ca insulină bazală într-un regim bazal-bolus (în asociere cu o insulină cu acțiune rapidă sau un analog cu acțiune rapidă), similar altor analogi cu durată de acțiune prelungită. În diabetul de tip 2, TRESIBA, similar altor analogi cu acțiune prelungită, poate fi utilizată astfel: - în momentul instituirii terapiei cu insulină, ca insulină bazală (în asociere cu unul sau mai multe medicamente antidiabetice orale) - în momentul instituirii unui tratament intensificat cu insulină, ca insulină bazală într-un regim bazal-bolus (în asociere cu o insulină sau un analog cu acțiune rapidă sau ultrarapidă). Atunci când administrarea dozei nu este posibilă la aceeași oră din zi, Tresiba oferă flexibilitate în ceea ce privește ora de administrare a insulinei.
6 Populația țintă Următorii pacienți sunt eligibili pentru insulino-terapie: - toți pacienții cu diabet de tip 1 (DZ tip 1); - anumiți pacienți cu diabet de tip 2 (DZ tip 2), în principal cei la care terapia triplă orală (metformină + sulfamidă hipoglicemiantă + alt ADO) a eșuat, precum și cei la care terapia dublă orală (metformină + sulfamidă hipoglicemiantă) a eșuat, cu o abatere de la obiectivul glicemic 1% HbA1c. Populația țintă este reprezentată din suma pacienților diabetici deja tratați cu insulină (pacienți cu diabet de tip 1 și pacienți cu diabet de tip 2) și a pacienților cu diabet de tip 2 tratați doar cu ADO, neechilibrați și eligibili pentru insulino-terapie. Au fost reținute următoarele ipoteze: - 70% dintre pacienții cu DT2 tratați doar cu ADO, neechilibrați cu HbA1c 8% sunt eligibili pentru insulinoterapie (analiză de sensibilitate: limita inferioară 0%; limita superioară 95%); - 10% dintre pacienții cu DT2 tratați doar cu ADO, neechilibrați cu 7% HbA1c < 8% sunt eligibili pentru insulinoterapie (analiză de sensibilitate: limita inferioară 0%; limita superioară 25%); În total, populația țintă a Tresiba poate fi estimată la aprox de pacienți cu diabet (DZ tip 1 și DZ tip 2), adică suma dintre de pacienți diabetici tratați deja cu insulină (din care cu DZ tip 1 și cu DZ tip 2) și de pacienți cu DZ tip 2 tratați doar cu ADO, neechilibrați și eligibili pentru insulinoterapie, cu un interval de plauzibilitate cuprins între de pacienți (limita inferioară) și de pacienți (limita superioară). (Insulinum detemir) 100 U/ml NovoNordisk, Lantus (Insulinum glargin) 100 U/ml Sanofi, Abasaglar (Insulinum glargin) 100 U/ml Lilly. 2.2 ETM bazată pe cost-eficacitate - NICE Nu a fost publicat până în prezent de către National Institute for Health and Care Excellence raportul de evaluare tehnică bazată pe cost-eficacitate a DCI insulinum degludec ETM bazată pe cost-eficacitate - SMC Tresiba 100 unități/ml soluție injectabilă în cartuș a fost evaluată pentru tratamentul tratamentul diabetului zaharat la adulți de către The Scottish Medicines Consortium (SMC), iar raportul (856/13) a fost publicat în data de 08 martie Comitetul a concluzionat că: Tresiba 100 unități/ml soluție injectabilă în cartuș nu este recomandată pentru utilizare la nivelul NHS Scoția în tratamentul diabetului zaharat la adulți. Insulina degludec nu este inferioară altor analogi de insulină cu acțiune prelungită pentru tratamentul diabetului zaharat de tip 1 și 2, evaluată prin prisma valorilor de hemoglobina glicată (HbA1c) și este superioară unui inhibitor de dipeptidil peptidază-4 în diabetul zaharat de tip 2. Compania solicitantă nu a prezentat o analiză economică suficient de robustă pentru a obține aprobarea din partea SMC.
7 Experții au concluzionat că comparatorii relevanți pentru practica clinică din Scoția sunt alte insuline cu acțiune prelungită: insulină izofan (NPH), insulină detemir și insulină glargin. Tresiba 100 unități/ml soluție injectabilă în cartuș a fost reevaluată pentru tratamentul diabetului zaharat la adulți de către SMC, iar raportul a fost publicat în data de 07 februarie Comitetul a concluzionat că Tresiba 100 unități/ml soluție injectabilă în cartuș nu este recomandată pentru utilizare la nivelul NHS Scoția în tratamentul diabetului zaharat la adulți. Tresiba 100 unități/ml soluție injectabilă în cartuș a fost reevaluată pentru tratamentul diabetului zaharat la adulți de către SMC, iar raportul a fost publicat în data de 08 iulie Comitetul a concluzionat că: Tresiba 100 unități/ml soluție injectabilă în cartuș este acceptată pentru utilizarea în cadrul NHS Scoția pentru tratamentul diabetului zaharat la adulți. Trei studii de fază III la adulți cu diabet zaharat de tip 1 și cinci studii de fază III la adulți cu diabet zaharat de tip 2 au arătat non-inferioritatea insulinei degludec în raport cu alți analogi de insulină cu acțiune prelungită, evaluată prin măsurarea modificării mediane a valorii hemoglobinei glicate (HbA1c). Insulinum degludec este de asemenea indicată pentru tratamentul diabetului zaharat la adolescenți și copii cu vârsta peste 1 an. Deţinătorul autorizaţiei de punere pe piaţă nu a depus un dosar la SMC cu privire la această indicație, astfel că SMC nu poate recomanda utilizarea acestuia în acest scop la nivelul NHS Scoţia. Experții au concluzionat că comparatorii relevanți pentru practica clinică din Scoția sunt: Levemir (insulină detemir), Lantus (insulină glargin), Toujeo (insulină glargin), Abasaglar (insulină glargin). 2.4 ETM bazată pe cost-eficacitate IQWIG Medicamentul insulinum degludec a fost evaluat de către autoritățile competente din Germania, pe site-ul instituției germane (IQWiG) fiind publicate mai multe rapoarte de evaluare a medicamentului amintit: A14-13, datat 30 iulie 2014, A15-10, datat 28 mai 2015, A15-26, datat 7 august 2015 (supliment la Mandatul A15-10). Medicamentul insulinum degludec are mai multe indicații terapeutice. Scopul primului raport de evaluare publicat (A14-13), modului I, a fost de a determina beneficiul adițional al insulinum degludec în asociere cu o insulină cu acțiune scurtă/rapidă comparativ cu terapia comparatoare adecvată (ACT), insulina umană specificată de G-BA, la pacienții adulți cu diabet zaharat de tip 1.
8 Analiza gradului de probabilitate și amploarea beneficiului terapeutic suplimentar prezentat de medicamentului insulinum degludec versus comparatorul potrivit în practica clinică din Germania pentru indicația terapeutică diabet zaharat de tip 1 la adulți a indicat următoarele: Din datele prezentate nu s-a putut desprinde nicio dovadă cu privire la beneficiul adițional al insulinum degludec în indicația terapeutică diabet zaharat de tip 1 comparativ cu ACT, specificată de G-BA. Prin urmare, nu există nici grupuri de pacienți care ar putea obține un beneficiu adițional important din punct de vedere terapeutic. Această evaluare diferă de cea a companiei, care a obținut o indicație privind un beneficiu adițional considerabil al insulinei degludec în combinație cu o insulină cu acțiune scurtă/rapidă la pacienții cu diabet zaharat de tip 1. Rezultatul evaluării beneficiului suplimentar al insulinum degludec comparativ cu ATC pentru indicația terapeutică diabet zaharat de tip 1 este prezentat succint mai jos: Tabel 1: Insulina degludec (diabetul zaharat de tip 1): amploarea și probabilitatea beneficiului adițional Indicație terapeutică Terapie comparatoare adecvată Amploarea și probabilitatea beneficiului adițional Diabet zaharat de tip 1 la pacienții adulți Insulină umană Beneficiu adițional nedovedit Procedura pentru obtinerea unei declaratii globale privind beneficiul suplimentar reprezinta o propunere a IQWiG. G-BA va decide cu privire la beneficiile suplimentare. Scopul modulului de evaluare II al raportului A14-13 a fost de a determina beneficiul adițional al insulinum degludec în tratamentul adulților cu diabet zaharat de tip 2 în monoterapie, în asociere cu antidiabetice orale (ADO) și în asociere cu o insulină bolus. Evaluarea a fost realizată separat pentru 3 sub-indicații, prin raportare la terapia comparatoare adecvată (ACT) specificată de G-BA. Tabel 2: Obiectul cercetării, sub-indicații și ACT privind insulinum degludec pentru indicația diabet de tip 2 evaluată în modulul de evaluare II: Obiectul cercetării a Sub-indicație ACT specificată de G-BA A Insulină degludec în monoterapie Insulină umană
9 B Insulină degludec + ADO b Insulină umană + metformină (Notă: Dacă metformina nu este indicată conform RCP, se utilizează insulina umană ca opțiune de tratament). C Insulină degludec + insulină bolus ± ADO Insulină umană ± metformină c a: Denumirea corespunde codificării din dosarul companiei. b: Mandatul stabilit de G-BA viza asocierea de insulinum degludec cu unul sau mai multe alte antidiabetice (cu excepția insulinei). Potrivit statusului de aprobare valabil la momentul depunerii dosarului, această sub-indicație a fost limitată la asocierea insulinum degludec cu ADO, în analogie cu abordarea companiei. c: În general, nu este indicată administrarea suplimentară de metformină în combinație cu o insulină bolus (fără ADO) în contextul unui tratament convențional intensificat cu insulină. ACT: terapie comparatoare adecvată; G-BA: Comisia Federală Mixtă; ADO: antidiabetice orale; RCP: Rezumatul Caracteristicilor Produsului Pentru diferitele sub-indicații ale insulinei degludec în tratamentul diabetului zaharat de tip 2 la pacienții adulți, amploarea și probabilitatea beneficiului adițional comparativ cu ACT relevantă sunt sintetizate în tabelul de mai jos. Tabel 3: Insulina degludec (diabetul zaharat de tip 2): amploarea și probabilitatea beneficiului adițional Obiectul cercetării a A Sub-indicație ACT Amploarea și probabilitatea beneficiului adițional Insulină degludec în monoterapie Insulină umană B Insulină degludec + ADO b Insulină umană + metformină C Insulină degludec + insulină bolus ± ADO (Notă: Dacă metformina nu este indicată conform RCP, se utilizează insulina umană ca opțiune de tratament). Insulină umană ± metformină c Beneficiu adițional nedovedit Beneficiu adițional nedovedit Beneficiu adițional nedovedit a: Denumirea corespunde codificării din dosarul companiei. b: Mandatul stabilit de G-BA viza combinația de insulinum degludec cu unul sau mai multe alte antidiabetice (cu excepția insulinei). Potrivit statusului de aprobare valabil la momentul depunerii dosarului, această sub-indicație a fost limitată la asocierea insulinum degludec cu ADO, în analogie cu abordarea companiei. c: În general, nu este indicată administrarea suplimentară de metformină în combinație cu o insulină bolus (fără ADO) în contextul unui tratament convențional intensificat cu insulină. ACT: terapie comparatoare adecvată; G-BA: Comisia Federală Mixtă; ADO: antidiabetice orale; RCP: Rezumatul Caracteristicilor Produsului Această evaluare diferă de cea a companiei, care a pretins o indicație privind un beneficiu adițional considerabil pentru sub-indicația insulinum degludec + ADO (obiectul cercetării B) și pentru sub-indicația insulinum degludec + insulină bolus ± ADO (obiectul cercetării C) în tratamentul diabetului zaharat de tip 2. G-BA decide cu privire la beneficiul adițional.
10 2.5 ETM bazată pe cost-eficacitate - G-BA Raportul de evaluare bazată pe cost-eficacitate G-BA a DCI insulinum degludec in tratamentul diabetului zaharat la adulti a fost publicat pe data de 16 mai Comparatorii relevanți pentru practica clinică din Germania sunt: insulina umana+metformina sau insulina umana+empagliflozin sau insulina umana+liraglutida sau insulina umana. Nu a fost demonstrat un beneficiu suplimentar pentru insulinum degludec comparativ cu ACT (terapie comparatoare adecvata), specificata de G-BA. Medicamentul Insulinum degludec a primit aviz pozitiv conform indicatiei din RCP (tratamentul diabetului zaharat la adulți, la adolescenți și copii de la vârsta de 1 an) și este rambursat prin decizia G-BA din 16 mai 2019 în Germania. 3. RAMBURSAREA MEDICAMENTULUI ÎN STATELE MEMBRE ALE UNIUNII EUROPENE Solicitantul a declarat pe propria răspundere că Insulinum degludec este rambursat în 19 state membre ale Uniunii Europene: Bulgaria, Cipru, Croația, Danemarca, Estonia, Finlanda, Franța, Grecia, Germania, Ungaria, Irlanda, Italia, Lituania, Luxemburg, Marea Britanie, Olanda, Slovacia, Slovenia și Suedia. 4. DATE PRIVIND COSTURILE TERAPIEI Solicitantul a propus drept comparator relevant Levemir (DCI : insulina detemir), conform OMS 861/2014 actualizat. Acesta se regăsește pe Lista cuprinzând denumirile comune internaționale corespunzătoare medicamentelor de care beneficiază asigurații, cu sau fără contribuție personală, pe bază de prescripție medicală, în sistemul de asigurări sociale de sănătate, DCI-uri corespunzătoare medicamentelor de care beneficiază asiguraţii în regim de compensare 100%, Secțiunea C2 (tratamentul ambulatoriu și spitalicesc), P5: Programul național de diabet zaharat, Tratamentul medicamentos al pacienților cu diabet zaharat. Insulinum detemir respectă condiţiile prevăzute în OMS 861/2014 privind definiția comparatorului. Conform O.M.S 487/2017, costul/doza zilnică recomandată (DDD anuale) se face pentru aceeaşi concentraţie, formă farmaceutică sau cale de administrare a DCI, iar, în cazul în care există pe piaţă atât medicamentul inovator, cât şi genericele pentru componentele combinaţiei fixe, suma costurilor/ddd anuale ale componentelor luate separat se face la nivelul medicamentelor generice cu cele mai mici preţuri cu amănuntul maximal cu TVA prezente în Catalogul naţional al preţurilor medicamentelor de uz uman, aprobat la data evaluării. În vederea efectuării calculului costurilor terapiei a fost utilizat prețul medicamentelor publicat în CaNaMed versiunea publicată la 21 noiembrie 2018.
11 Calculul costului terapiei cu DCI INSULINUM DEGLUDEC (DC TRESIBA) Monoterapie Insulinum degludec (DC TRESIBA) Tresiba 100 unități/ml soluție injectabilă în cartuș (Novo Nordisk A/S-Danemarca) este comercializat în cutie cu 5 cartușe x 3 ml soluție injectabilă (un cartuș conţine insulină degludec 300 unităţi în 3 ml soluţie, 1 ml soluţie conţine insulină degludec* 100 unităţi), care are un preţ cu amănuntul maximal cu TVA conform CaNaMed de 292,71 lei (58,54 lei/cartuș). Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru insulinum degludec este de 40 unități. Conform RCP-ului, Tresiba este o insulină bazală pentru administrare subcutanată o dată pe zi în orice moment al zilei. La pacienţii cu diabet de tip 2, acest medicament poate fi administrat în monoterapie sau în oricare asociere cu medicamente antidiabetice orale, agoniști de receptor GLP-1 sau insulină de tip bolus. La pacienţii cu diabet de tip 1, Tresiba trebuie asociat cu insuline cu acţiune scurtă/rapidă pentru a acoperi necesarul de insulină în timpul meselor. Costul anual al tratamentului cu insulinum degudec, luând în considerare doza zilnică medie de 40 U, este 2848,94 lei (365 X 40 /300 X 58,54 ). INSULINUM DETEMIR (DC LEVEMIR) Levemir Penfil 100 U/ml, soluție injectabilă în cartuș (Novo Nordisk A/S-Danemarca) este comercializat în cutie cu 5 cartușe x 3 ml soluție injectabilă (1 ml soluţie conţine insulină detemir* 100 unități, 1 cartuş conţine 3 ml echivalent cu 300 unităţi), care are un preţ cu amănuntul maximal cu TVA conform CaNaMed de 279,04 lei (55,80 lei/cartuș). Conform RCP, Levemir poate fi utilizat în monoterapie ca insulină bazală sau în combinaţie cu o insulină bolus. De asemenea, poate fi utilizat în combinaţie cu medicamente antidiabetice orale şi/sau agonişti de receptor GLP-1. În situaţiile în care Levemir este administrat în combinaţie cu medicamente antidiabetice orale sau este adăugat la agonişti de receptor GLP-1, se recomandă ca Levemir să fie administrat o dată pe zi, iniţial într-o doză de 0,1-0,2 unităţi/kg sau de 10 unităţi la pacienţi adulţi. Când se utilizează ca parte a unei terapii insulinice de tip bazal-bolus, Levemir trebuie administrat o dată sau de două ori pe zi, în concordanţă cu necesităţile pacientului. Doza de Levemir trebuie ajustată individual. Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru insulinum detemir este de 40 unități. Costul anual al tratamentului cu insulinum detemir, luând în considerare doza zilnică medie de 40 unități, este 2715,6 lei (365 X 40/300 X 55,80).
12 Din compararea costurilor celor două terapii, pe aceeaşi perioadă (1 an), se constată că medicamentul evaluat determină un impact bugetar neutru (4,91%) faţă de comparator, medicamentul Tresiba fiind cu 4,91% mai scump față de Levemir. Asociere cu ADO Conform CaNaMed prețul cu amânuntul maximal cu TVA cel mai mic aferent medicamentului cu DCI metformin de concentrație 1000 mg este 4,95 lei (0,165 lei/cp). Acesta corespunde DC Metformin Aurobindo 1000 mg, medicament condiționat în cutie x blistere PVC/ Al x 30 comprimate filmate. Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru metformin este de 2 g. Costul anual al tratamentului cu metformin, luând în considerare doza zilnică medie de 2 g, este 120, 45 lei (365 X 2 X 0, 165). Prin urmare, costul anual terapiei cu insulinum degludec + metformin este 2969,39 lei (2848, ,45). costul anual al terapiei cu insulinum detemir + metformin este 2836,05 lei (2715,6+ 120,45). Din compararea costurilor anuale ale celor două terapii, se constată că prețul terapiei insulinum degludec + metformin este mai mare cu 4,7 % comparativ cu prețul terapiei insulinum detemir + metformin, determinând un impact bugetar neutru. Asociere cu agoniști de receptor GLP-1 Lyxumia 10 micrograme soluție injectabilă în stilou injector (Sanofi-Aventis Groupe - Franța) este comercializat în cutie cu 1 stilou injector (pen) preumplut x 3ml soluție (1x14 doze) ( fiecare doză (0,2 ml) conţine lixisenatidum 10 micrograme (µg)) care are un preţ cu amănuntul maximal cu TVA conform CaNaMed de 190,22 lei. Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru lixisenatidum este de 20 micrograme. Costul anual al tratamentului cu lixisenatidum, luând în considerare doza zilnică medie de 20 micrograme, este 9918,61 lei (365 X 20/140 X 190,22 ). Prin urmare, costul anual terapiei cu insulinum degludec + lixisenatidum este 12767,55 lei (2848, ,61). costul anual al terapiei cu insulinum detemir + lixisenatidum este 12634,21 lei (2715,6+9918,61).
13 Din compararea costurilor anuale ale celor două terapii, se constată că prețul terapiei insulinum degludec + lixisenatidum este mai mare cu 1,05 % comparativ cu prețul terapiei insulinum detemir + lixisenatidum, determinând un impact bugetar neutru. Asociere cu insulină cu acțiune rapidă Humalog 100 U/ml soluție injectabilă (Eli Lilly Nederland BV-Olanda) este comercializat în cutie cu 5 cartușe x 3 ml soluție injectabilă ( fiecare cartuș conţine insulinum lispro 300 unități în 3 ml soluție), care are un preţ cu amănuntul maximal cu TVA conform CaNaMed de 151,28 lei (30,25 lei/cartuș). Conform informațiilor de pe site-ul WHO-ATC, doza zilnică medie (DDD) pentru insulinum lispro este de 40 unități. Costul anual al tratamentului cu inulinum lispro, luând în considerare doza zilnică medie de 40 unități, este 1472,16 lei (365 X 40/300 X 30,25 ). Prin urmare, costul anual terapiei cu insulinum degludec + insulinum lispro este lei (2848, ,16). costul anual al terapiei cu insulinum detemir + insulinum lispro este lei (2715,6+1472,16). Din compararea costurilor anuale ale celor două terapii, se constată că prețul terapiei insulinum degludec + insulinum lispro este mai mare cu 3,18 % comparativ cu prețul terapiei insulinum detemir + insulinum lispro, determinând un impact bugetar neutru. 5. PUNCTAJ OBȚINUT Criterii de evaluare Punctaj 1. ETM bazată pe estimarea beneficiului terapeutic (SMR) HAS BT 1-Beneficiu terapeutic important în următoarea indicație: Tratamentul diabetului zaharat tip 1 și 2 la adulți ETM bazată pe cost-eficacitate 2.1. NICE - nu a fost publicat raportul SMC: recomandă rambursarea fără restricții față de RCP în tratamentul diabetului zaharat tip 1 și 2 la adulți; IQWIG/ G-BA- fara restrictii Tratamentul diabetului zaharat la adulți Statutul de compensare al DCI Insulinum degludec în statele membre ale UE 19 țări Costurile terapiei
14 Impact bugetar neutru față de comparator în monoterapie și pentru următoarele asocieri: insulinum degludec + metformin 15 insulinum degludec + lixisenatidum insulinum degludec + insulinum lispro TOTAL PUNCTAJ: 85 puncte 6. CONCLUZIE Conform O.M.S. 861/2014 cu modificările și completările ulterioare, medicamentul cu DCI insulinum degludec pentru indicația:,, tratamentul diabetului zaharat la adulți,, întrunește punctajul de admitere necondiționată în Lista care cuprinde denumirile comune internaționale corespunzătoare medicamentelor de care beneficiază asigurații, cu sau fără contribuție personală, pe bază de prescripție medicală, în sistemul de asigurări sociale de sănătate. 7. RECOMANDĂRI Recomandăm elaborarea protocolului terapeutic pentru medicamentul cu DCI insulinum degludec pentru indicația:,, tratamentul diabetului zaharat la adulți,,. Șef DETM Dr. Farm. Pr. Felicia Ciulu-Costinescu
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE NIVOLUMABUM INDICAȚIA: MONOTERAPIE PENTRU TRATAMENTUL CANCERULUI SCUAMOS DE CAP SI GAT LA ADULTI LA CARE BOALA PROGRESEAZA IN TIMPUL SAU DUPA TERAPIE DE BAZA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE EPLERENONUM INDICAȚIA: INSUFICIENŢA CARDIACĂ Data de depunere dosar 20.08.2014 Numar dosar 3160 PUNCTAJ: 55 1. DATE GENERALE 1.1. DCI: Eplerenonum 1.2.1. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DABRAFENIBUM INDICAȚIA: MELANOM INOPERABIL SAU METASTATIC POZITIV LA MUTATIA BRAF V600 Data de depunere dosar 11.08.2014 Numar dosar 3035 PUNCTAJ: 65 1. DATE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE MINOCYCLINUM INDICAȚIA: Acnee (determinată de Propionibacterium acnes) Data de depunere dosar 08.09.2014 Numar dosar 3281 PUNCTAJ: 40 1. DATE GENERALE 1.1. DCI:
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI VEMURAFENIBUM INDICAȚIA: MELONOM MALIGN Data de depunere dosar 04.08.2014 Numar dosar 2906 PUNCTAJ: 70 1. DATE GENERALE 1.1. DCI: vemurafenib 1.2. DC: Zelboraf
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI VEMURAFENIBUM INDICAȚIA: MELONOM MALIGN Data de depunere dosar 04.08.2014 Numar dosar 2906 PUNCTAJ: 70 1. DATE GENERALE 1.1. DCI: vemurafenib 1.2. DC: Zelboraf
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE BENDAMUSTINUM INDICAȚIA: LIMFOM nonhodkin Data de depunere dosar 18.08.2014 Numar dosar 3143 PUNCTAJ: 65 1 1. DATE GENERALE 1.1. DCI: BENDAMUSTINUM 1.2. DC:
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE BENDAMUSTINUM INDICAȚIA: LIMFOM nonhodkin Data de depunere dosar 18.08.2014 Numar dosar 3143 PUNCTAJ: 65 1 1. DATE GENERALE 1.1. DCI: BENDAMUSTINUM 1.2. DC:
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: RIOCIGUAT INDICAȚII: HIPERTENSIUNE ARTERIALĂ PULMONARĂ CRONICĂ HIPOEMBOLICĂ (HAPCTE) HIPERTENSIUNE ARTERIALĂ PULMONARĂ (HAP) Data depunerii dosarului 08.04.2015
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologie
 MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂŢII ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 861/2014 pentru aprobarea criteriilor şi metodologiei de evaluare a tehnologiilor medicale, a documentaţiei
MINISTERUL SĂNĂTĂȚII AGENȚIA NAȚIONALĂ A MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Departamentul de Evaluare a Tehnologiilor Medicale Str. Aviator S
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE I: ACIDUM IBANDRONICUM INDICAȚIA: TRATAMENTUL OSTEOPOROZEI LA PACIENTELE ÎN POSTMENOPAUZĂ CU RISC CRESCUT DE FRACTURĂ Reducerea riscului fracturilor vertebrale
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: BRENTUXIMAB VEDOTIN INDICAŢIA: LIMFOM HODGKIN CD30+ RECIDIVAT SAU REFRACTAR: 1. DUPĂ TRANSPLANT DE CELULE STEM AUTOLOGE (TCSA) 2. DUPĂ CEL PUŢIN DOUĂ TRATAMENTE
Vokanamet, INN-canagliflozin-metformin
 ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
ANEXA IV Concluzii științifice 1 Concluzii științifice Inhibitorii co-transportorului 2 de sodiu-glucoză (SGLT2) se utilizează în asociere cu regim alimentar și exercițiu fizic la pacienții cu diabet de
Enurace Annexes I-II-III
 ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ANEXA I NUME, FORMA FARMACEUTICĂ, DOZAJUL PRODUSULUI MEDICAMENTOS, SPECII ANIMALE, CĂI DE ADMINISTRARE ŞI DEŢINĂTORUL AUTORIZAŢIEI DE COMERCIALIZARE 1/7 State membre Solicitant sau deţinătorul autorizaţiei
ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții c
 ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții cu SCA tratați invaziv cu stent, în baza unui contract
ÎMPREUNĂ PENTRU PACIENTUL CU SCA ÎN PRIMUL AN POST EVENIMENTUL ACUT Medicamentul BRILIQUE 90mg, DCI Ticagrelor, este 100% compensat pentru pacienții cu SCA tratați invaziv cu stent, în baza unui contract
MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr / Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDR
 MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr. 29288/17.05.2019 Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDRESCU Aprob, MINISTRU SORINA PINTEA REFERAT DE APROBARE
MINISTERUL SĂNĂTĂȚII DIRECȚIA POLITICA MEDICAMENTULUI ȘI A DISPOZITIVELOR MEDICALE Nr. 29288/17.05.2019 Avizat, SECRETAR DE STAT DAN OCTAVIAN ALEXANDRESCU Aprob, MINISTRU SORINA PINTEA REFERAT DE APROBARE
I n t r a l e g i s C T C E P i a t r a N e a m ţ, w w w. c t c e. r o ORDIN nr din 16 decembrie 2016 privind modificarea şi com
 I n t r a l e g i s 6. 2 - C T C E P i a t r a N e a m ţ, 2 0 1 7 w w w. c t c e. r o ORDIN nr. 1.463 din 16 decembrie 2016 privind modificarea şi completarea anexei nr. 1 la Ordinul ministrului sănătăţii
I n t r a l e g i s 6. 2 - C T C E P i a t r a N e a m ţ, 2 0 1 7 w w w. c t c e. r o ORDIN nr. 1.463 din 16 decembrie 2016 privind modificarea şi completarea anexei nr. 1 la Ordinul ministrului sănătăţii
NOTA
 NOTĂ DE FUNDAMENTARE SECŢIUNEA 1 TITLUL PROIECTULUI DE ACT NORMATIV Hotărâre de Guvern pentru modificarea și completarea Anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile
NOTĂ DE FUNDAMENTARE SECŢIUNEA 1 TITLUL PROIECTULUI DE ACT NORMATIV Hotărâre de Guvern pentru modificarea și completarea Anexei la Hotărârea Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile
Furosemide Vitabalans Annex I_II_ro
 Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
Anexa I Lista numelor, formelor farmaceutice, concentraţiilor medicamentului, calea de administrare, aplicantul în Statele Membre 1 Statele Membre UE/AEE Solicitantul Denumire comercială Concentraţia Forma
TRULICITY, INN-dulaglutide
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 Acest medicament face obiectul unei monitorizări suplimentare. Acest lucru va permite identificarea rapidă de noi informaţii referitoare la siguranţă. Profesioniştii
EllaOne,INN-ulipristal acetate
 Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Anexa IV Concluzii ştiinţifice şi motive pentru modificarea condiţiilor autorizaţiilor de introducere pe piaţă 27 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru medicamentele contraceptive
Furosemide Vitabalans Annex I_II_ro
 Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
Anexa II Concluzii ştiinţifice şi motive pentru refuz prezentate de Agenţia Europeană pentru Medicamente 4 Concluzii ştiinţifice Rezumat general al evaluării ştiinţifice pentru Furosemide Vitabalans şi
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura d
 ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
ORDIN privind modificarea şi completarea Ordinului ministrului sănătăţii nr. 368/2017 pentru aprobarea Normelor privind modul de calcul și procedura de aprobare a prețurilor maximale ale medicamentelor
PRO_4657_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4657/2004/01-02-03-04-05 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR LACTECON 667 g/l lichid oral Lactuloză Citiţi cu atenţie şi în întregime acest prospect
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIE: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIE: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
COMUNICAT DE PRESĂ
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1
 Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Codul EFPIA privind prezentarea de informații Informări 2017 Shire Pharmaceuticals (inclusiv Baxalta US Inc.) 1 Secțiunea 1: Abordarea privind raportarea datelor din 2017 Pe 3 iunie 2016, Shire a achiziționat
Lectia de economie. Derapaje fiscal bugetare majore in
 Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
Lectia de economie. Derapaje fiscal bugetare majore in Uniunea Europeana. 12 tari in Procedura de Deviere semnificativa. Jumatate nu indeplinesc regulile fiscalbugetare Cristian Socol, Sistemul de reguli
BYDUREON,INN-exenatide
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Bydureon 2 mg pulbere și solvent pentru suspensie injectabilă cu eliberare prelungită. 2. COMPOZIȚIA CALITATIVĂ
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Bydureon 2 mg pulbere și solvent pentru suspensie injectabilă cu eliberare prelungită. 2. COMPOZIȚIA CALITATIVĂ
Apidra, INN-insulin glulisine
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Apidra 100 Unităţi/ml soluţie injectabilă în flacon Apidra 100 Unităţi/ml soluţie injectabilă în cartuş Apidra
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Apidra 100 Unităţi/ml soluţie injectabilă în flacon Apidra 100 Unităţi/ml soluţie injectabilă în cartuş Apidra
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă d
 Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
Anexa I Lista denumirilor, formelor farmaceutice, concentraţiilor medicamentelor, calea de administrare, deţinătorii autorizaţiei de punere pe piaţă din statele membre 1 Stat membru EU/EEA Deţinătorul
EMA ENRO
 Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
Anexa II Concluzii ştiinţifice şi motive pentru modificarea rezumatului caracteristicilor produsului, etichetării şi prospectului prezentate de Agenţia Europeană pentru Medicamente 23 Concluzii ştiinţifice
PRO_3712_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3712/2003/01 Anexa 1 Prospect Prospect: Informaţii pentru utilizator KETOTIFEN HELCOR 1 mg, comprimate Citiţi cu atenţie şi în întregime acest prospect înainte de a începe
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatu
 COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
COMUNICAT DE PRESĂ Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale prezintă în cele ce urmează traducerea în limba română a comunicatului de presă al Agenţiei Europene a Medicamentului
HOTĂRÂRE
 Hotărâre 18 2017-01-12 Guvernul României pentru modificarea şi completarea Hotărârii Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale corespunzătoare medicamentelor
Hotărâre 18 2017-01-12 Guvernul României pentru modificarea şi completarea Hotărârii Guvernului nr. 720/2008 pentru aprobarea Listei cuprinzând denumirile comune internaţionale corespunzătoare medicamentelor
MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedin
 MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedinte REFERAT DE APROBARE In conformitate cu prevederile
MINISTERUL SĂNĂTĂŢII APROB, Ministru Sorina PINTEA CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE APROB, p. Președinte Razvan Teohari VULCANESCU Vicepresedinte REFERAT DE APROBARE In conformitate cu prevederile
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 2065/2009/01 Anexa 1` Prospect Aciclovir Laropharm 200 mg, comprimate Aciclovir Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comi
 CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
CEL DE AL 4-LEA RAPORT AL COMISIEI EUROPENE PRIVIND STAREA UNIUNII ENERGETICE Conform Comunicatului Comisiei Europene din data de 9 aprilie 2019, Comisia Europeană și-a îndeplinit pe deplin angajamentele
Microsoft Word - EMEA ENRO
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA (CONCENTRAŢIILE) PRODUSULUI MEDICAMENTOS, CALEA DE ADMINISTRARE, SOLICITANTUL, TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN
Onglyza, INN-saxagliptin
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Onglyza 2,5 mg comprimate filmate Onglyza 5 mg comprimate filmate 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Onglyza
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Onglyza 2,5 mg comprimate filmate Onglyza 5 mg comprimate filmate 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Onglyza
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SE
 Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Cod formular specific: L012C FORMULAR PENTRU VERIFICAREA RESPECTĂRII CRITERIILOR DE ELIGIBILITATE AFERENTE PROTOCOLULUI TERAPEUTIC DCI BORTEZOMIBUM SECŢIUNEA I - DATE GENERALE 1.Unitatea medicală:....
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIA: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: DOLUTEGRAVIRUM INDICAȚIA: ÎN ASOCIERE CU ALTE MEDICAMENTE ANTIRETROVIRALE DESTINATE TRATAMENTULUI INFECŢIEI CU VIRUSUL IMUNODEFICIENŢEI UMANE (HUMAN IMMUNODEFICIENCY
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la
 Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Consiliul Uniunii Europene Bruxelles, 8 noiembrie 2016 (OR. en) 13583/16 BUDGET 29 EXPUNERE DE MOTIVE Subiect: Proiect de buget rectificativ nr. 4 la bugetul general pentru exercițiul financiar 2016: Actualizarea
Săptămâna Europeană a Vaccinării # Vaccinurile sunt benefice Prevenire Să ne protejăm împreună Protecție Vaccinare aprilie 2019 Între 1 ianuarie
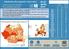 Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
Săptămâna Europeană a Vaccinării 20-25 aprilie 2019 Între 1 ianuarie 2018 și 31 decembrie 2018, 30 de State Membre UE/SEE au raportat 12352 cazuri de rujeolă, din care 8596 (70%) au fost confirmate cu
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: Cerliponasum alfa INDICAȚIA: LIPOFUSCINOZA CEROIDĂ TIP2 (DEFICIT DE TRIPEPTIDIL PEPTIDAZA- TPP1) Data depunerii dosarului 12.12.2018 Numărul dosarului 30478
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: Cerliponasum alfa INDICAȚIA: LIPOFUSCINOZA CEROIDĂ TIP2 (DEFICIT DE TRIPEPTIDIL PEPTIDAZA- TPP1) Data depunerii dosarului 12.12.2018 Numărul dosarului 30478
Microsoft Word - ORDIN pmod si comp anexei 1 la o privind aprobarea formularelor specifice pentru verificarea criteriilor
 ORDIN nr. 271 din 4 aprilie 2017 pentru modificarea şi completarea anexei nr. 1 la Ordinul preşedintelui Casei Naţionale de Asigurări de Sănătate nr. 141/2017 privind aprobarea formularelor specifice pentru
ORDIN nr. 271 din 4 aprilie 2017 pentru modificarea şi completarea anexei nr. 1 la Ordinul preşedintelui Casei Naţionale de Asigurări de Sănătate nr. 141/2017 privind aprobarea formularelor specifice pentru
CNAS
 FIŞĂ DE INIŢIERE A TRATAMENTULUI CU ORLISTATUM (XENICAL) PENTRU PACIENTUL CU TULBURĂRI DE NUTRIŢIE ŞI METABOLISM I. Date de identificare a. Numele şi prenumele pacientului Data naşterii (zi, luna, an)
FIŞĂ DE INIŢIERE A TRATAMENTULUI CU ORLISTATUM (XENICAL) PENTRU PACIENTUL CU TULBURĂRI DE NUTRIŢIE ŞI METABOLISM I. Date de identificare a. Numele şi prenumele pacientului Data naşterii (zi, luna, an)
RCP_3764_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 3764/2011/01-02-03 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Mastodynon comprimate
FAQs as published on the web - EN version
 13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
13 februarie 2017 EMA/527628/2011 Rev.1 Direcția Prezentul document oferă răspunsuri la cele mai frecvente întrebări adresate Agenției Europene pentru Medicamente (EMA). Dacă nu găsiți răspunsul la întrebările
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/ Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injec
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5000/2012/01-02-03 Anexa 1 Prospect Prospect: informaţii pentru pacient Aprokam 50 mg, pulbere pentru soluţie injectabilă Cefuroximă Citiţi cu atenţie şi în întregime
Microsoft Word - societatea informationala.doc
 I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
I Principalii indicatori ai societăţii informaţionale la nivel naţional Indicator 2013 2014 Număr de linii telefonice fixe la 1000 de locuitori 218,4 212,6 Număr de abonaţi la telefonie mobilă la 1000
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara
 Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Activitatea filialelor străine în România Realitatea economică arată că pe măsura dezvoltării întreprinderile tind să-şi extindă activitatea în afara graniţelor ţării în care ele au fost înfiinţate, acest
Microsoft Word - procedura mobilitati.doc
 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr.1 Educaţia şi formarea profesională în sprijinul creşterii economice
Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr.1 Educaţia şi formarea profesională în sprijinul creşterii economice
Microsoft Word - Lansoprazole_Annex_I-III_ro
 ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
ANEXA I LISTA CU DENUMIRILE COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIILE MEDICAMENTULUI, CALEA DE ADMINISTRARE, SOLICITANŢII, DEŢINĂTORII AUTORIZAŢIEI DE PUNERE PE PIAŢĂ ÎN STATELE MEMBRE Statul Membru
NOTE EXPLICATIVE SI POLITICI CONTABILE
 RAPORT PRIVIND PROGRAMUL NATIONAL CU SCOP CURATIV 2017 Programele nationale cu scop curativ finantate din bugetul Fondului national unic de asigurari sociale de sanatate reprezinta un ansamblu de actiuni
RAPORT PRIVIND PROGRAMUL NATIONAL CU SCOP CURATIV 2017 Programele nationale cu scop curativ finantate din bugetul Fondului national unic de asigurari sociale de sanatate reprezinta un ansamblu de actiuni
Microsoft Word - RO_EMEA
 ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
ANEXA I LISTA DENUMIRILOR COMERCIALE, FORMA FARMACEUTICĂ, CONCENTRAŢIA PRODUSELOR MEDICAMENTOASE, CALEA DE ADMINISTRARE, SOLICITANŢII/ TITULARUL AUTORIZAŢIEI DE INTRODUCERE PE PIAŢĂ ÎN STATELE MEMBRE 1
Ristfor (clone Janumet), INN-sitagliptin/metformin HCl
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Ristfor 50 mg/850 mg comprimate filmate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare comprimat conţine fosfat
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Ristfor 50 mg/850 mg comprimate filmate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare comprimat conţine fosfat
C(2015)6507/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
COMISIA EUROPEANĂ Bruxelles, 25.9.2015 C(2015) 6507 final REGULAMENTUL DELEGAT (UE) / AL COMISIEI din 25.9.2015 de completare a Regulamentului (UE) nr. 609/2013 al Parlamentului European și al Consiliului
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1
 Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
Codul EFPIA privind prezentarea de informații Informări 2018 Shire Pharmaceuticals 1 Secțiunea 1: Abordarea privind raportarea datelor din 2018 Pe 3 iunie 2016, Shire a achiziționat Baxalta. În conformitate
FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galati 1.2 Facultatea / Departamentul M
 FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galati 1.2 Facultatea / Departamentul Medicină si Farmacie / Clinic Medical 1.3 Catedra -
FIŞA DISCIPLINEI 1. Date despre program 1.1 Instituţia de învăţământ superior Universitatea Dunărea de Jos din Galati 1.2 Facultatea / Departamentul Medicină si Farmacie / Clinic Medical 1.3 Catedra -
PRO_4804_ doc
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 4804/2012/01-02-03-04 Anexa 1 Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR CEREBROLYSIN 215,2 mg/ml soluţie injectabilă/concentrat pentru soluţie perfuzabilă Citiţi
Act LexBrowser
 MINISTERUL SĂNĂTĂŢII ORDIN pentru modificarea şi completarea Ordinului ministrului sănătăţii nr. 426/2009 privind aprobarea Listei şi preţurilor de decontare ale medicamentelor care se acordă bolnavilor
MINISTERUL SĂNĂTĂŢII ORDIN pentru modificarea şi completarea Ordinului ministrului sănătăţii nr. 426/2009 privind aprobarea Listei şi preţurilor de decontare ale medicamentelor care se acordă bolnavilor
Protocol clinic naţional Diabetul zaharat, Chişinău 2017 Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evolu
 Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evoluţie cronică apărută prin alterarea secreţiei de insulină, care determină modificări majore în metabolismul glucozei
Anexa 6. Informaţie pentru pacientul cu diabet zaharat Diabetul zaharat este o boală cu evoluţie cronică apărută prin alterarea secreţiei de insulină, care determină modificări majore în metabolismul glucozei
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: LENALIDOMIDUM INDICAȚIE: LENALIDOMIDĂ SANDOZ ESTE INDICAT, ÎN ASOCIERE CU DEXAMETAZONĂ, PENTRU TRATAMENTUL PACIENŢILOR ADULŢI CU MIELOM MULTIPLU CĂRORA
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: LENALIDOMIDUM INDICAȚIE: LENALIDOMIDĂ SANDOZ ESTE INDICAT, ÎN ASOCIERE CU DEXAMETAZONĂ, PENTRU TRATAMENTUL PACIENŢILOR ADULŢI CU MIELOM MULTIPLU CĂRORA
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CERITINIBUM INDICAŢIA: ÎN MONOTERAPIE ESTE INDICAT PENTRU TRATAMENTUL PACIENȚILOR ADULȚI CU CANCER PULMONAR CU CELULE NON-MICI, ÎN STADIU AVANSAT (NSCLC),
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CERITINIBUM INDICAŢIA: ÎN MONOTERAPIE ESTE INDICAT PENTRU TRATAMENTUL PACIENȚILOR ADULȚI CU CANCER PULMONAR CU CELULE NON-MICI, ÎN STADIU AVANSAT (NSCLC),
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR
 Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
Stimate pacient, Pe această cale vă aducem la cunoştinţă faptul că s-a semnat contractul cost-volum-rezultat pentru tratamentul cu Harvoni (SOFOSBUVIR+LEDIPASVIR) al cirozei hepatice cu virus C, forma
Microsoft Word - 663E5DA5.doc
 Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
Regulamentul (CE) nr. 2743/98 al Consiliului din 14 decembrie 1998 de modificare a Regulamentului (CE) nr. 297/95 privind taxele datorate Agenţiei Europene pentru Evaluarea Medicamentelor CONSILIUL UNIUNII
st00TSCG26.ro12
 Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
Obiectul: TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE TRATATUL PRIVIND STABILITATEA, COORDONAREA ŞI GUVERNANŢA ÎN CADRUL UNIUNII ECONOMICE ŞI MONETARE
Microsoft Word - DOLJ - RAPORT_DE_EVALUARE_control_2007 .doc
 RAPORT DE EVALUARE la nivelul judetului DOLJ in urma controlului efectuat in conformitate cu Ordinul comun al ministrului sanatatii publice si al presedintelui CNAS nr. 888/270/2007 Comisia mixta formata
RAPORT DE EVALUARE la nivelul judetului DOLJ in urma controlului efectuat in conformitate cu Ordinul comun al ministrului sanatatii publice si al presedintelui CNAS nr. 888/270/2007 Comisia mixta formata
EMA ENRO
 Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Anexa I Lista cu denumirile comerciale, forma farmaceutică, concentraţia medicamentelor de uz veterinar, speciile de animale, calea de administrare, deţinătorul autorizaţiilor de punere pe piaţă din statele
Raportare TRIMESTRUL III 2007.xls
 CASA DE ASIGURARI DE SANATATE Subprogram 3. TRATAMENTUL BOLNAVILOR CU AFECTIUNI CARDIOVASCULARE PRIN CHIRURGIE CARDIOVASCULARA SI PRIN CARDIOLOGIE INTERVENTIONALA SI ELECTROFIZIOLOGIE Tabel 3.1 SITUATIA
CASA DE ASIGURARI DE SANATATE Subprogram 3. TRATAMENTUL BOLNAVILOR CU AFECTIUNI CARDIOVASCULARE PRIN CHIRURGIE CARDIOVASCULARA SI PRIN CARDIOLOGIE INTERVENTIONALA SI ELECTROFIZIOLOGIE Tabel 3.1 SITUATIA
New product information wording - Dec RO
 17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
17 December 2015 EMA/PRAC/835765/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Text nou în informațiile referitoare la produs Extrase din recomandările PRAC privind semnalele Adoptat la reuniunea
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COME
 AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
AUTORIZAŢIE DE PUNERE PE PIAŢǍ NR.6227/2006/01 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A A MEDICAMENTULUI Rowatinex picături orale,
RAPORT
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CRIZOTINIBUM INDICAȚIE: TRATAMENTUL ADULTILOR CU NEOPLASM BRONHO-PULMONAR ALTUL DECAT CEL CU CELULE MICI (NSCLC) AVANSAT, POZITIV PENTRU ROS 1 Data depunerii
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: CRIZOTINIBUM INDICAȚIE: TRATAMENTUL ADULTILOR CU NEOPLASM BRONHO-PULMONAR ALTUL DECAT CEL CU CELULE MICI (NSCLC) AVANSAT, POZITIV PENTRU ROS 1 Data depunerii
Strategia IT&C a Agenţiei Naţională a Medicamentului şi Dispozitivelor Medicale
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: COMBINAȚII (BRINZOLAMIDUM + BRIMONIDINUM) INDICAȚIE: SCĂDEREA PRESIUNII INTRAOCULARE (PIO) CRESCUTE, LA PACIENŢI ADULŢI CU GLAUCOM CU UNGHI DESCHIS SAU
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: COMBINAȚII (BRINZOLAMIDUM + BRIMONIDINUM) INDICAȚIE: SCĂDEREA PRESIUNII INTRAOCULARE (PIO) CRESCUTE, LA PACIENŢI ADULŢI CU GLAUCOM CU UNGHI DESCHIS SAU
Iron IV-A _DHPC
 Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Octombrie 2013 Recomandări ferme cu privire la riscul de apariţie a unor reacţii grave de hipersensibilitate la medicamentele care conţin fier şi cu administrare intravenoasă Stimate profesionist din domeniul
Casa Națională de Asigurări de Sănătate ORDIN Nr. 113/ privind modificarea şi completarea Normelor tehnice de realizare a programelor națion
 Casa Națională de Asigurări de Sănătate ORDIN Nr. 113/09.02.2017 privind modificarea şi completarea Normelor tehnice de realizare a programelor naționale de sănătate curative pentru anii 2015 și 2016,
Casa Națională de Asigurări de Sănătate ORDIN Nr. 113/09.02.2017 privind modificarea şi completarea Normelor tehnice de realizare a programelor naționale de sănătate curative pentru anii 2015 și 2016,
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE
 RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: APIXABANUM INDICAŢIA: prevenirea evenimentelor tromboembolice venoase la pacienţii adulţi care sunt supuşi unei intervenţii chirurgicale de artroplastie
RAPORT DE EVALUARE A TEHNOLOGIILOR MEDICALE DCI: APIXABANUM INDICAŢIA: prevenirea evenimentelor tromboembolice venoase la pacienţii adulţi care sunt supuşi unei intervenţii chirurgicale de artroplastie
Microsoft Word - Referat proiect ordin.doc
 CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE DIRECŢIA GENERALĂ RELAŢII CONTRACTUALE Nr. Avizat, Director General Radu ŢIBICHI Aprobat, Preşedinte Vasile CIURCHEA REFERAT DE APROBARE În temeiul prevederilor:
CASA NAŢIONALĂ DE ASIGURĂRI DE SĂNĂTATE DIRECŢIA GENERALĂ RELAŢII CONTRACTUALE Nr. Avizat, Director General Radu ŢIBICHI Aprobat, Preşedinte Vasile CIURCHEA REFERAT DE APROBARE În temeiul prevederilor:
Harmonised DHPC letter_BCR-ABLTKIs_HepBreactivation_19Feb2016_PRAC version
 Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
Martie 2016 Comunicare directă către profesioniştii din domeniul sănătăţii Inhibitori de tirozin-kinază BCR-ABL (imatinib, dasatinib, nilotinib, bosutinib, ponatinib) Necesitatea de a efectua o testare
AUTORIZATIE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5251/2005/01-02-03-04-05-06-07 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Telfast
Microsoft Word - anunt prealabil selectie 2018.doc
 INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
INFORMAŢII PRIVIND CONCURSURILE DE SELECŢIE PENTRU MOBILITÃŢI ERASMUS+ (KA103) IN TARILE PROGRAMULUI ERASMUS+ In perioada urmãtoare va trebui sa fiti foarte atenti la continututul anunturilor privind sesiunile
Jardiance, INN-Empagliflozin
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Jardiance 10 mg comprimate filmate Jardiance 25 mg comprimate filmate 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Jardiance
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Jardiance 10 mg comprimate filmate Jardiance 25 mg comprimate filmate 2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ Jardiance
Sepioglin, INN-pioglitazone
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Sepioglin 15 mg comprimate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare comprimat conţine pioglitazonă 15 mg
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Sepioglin 15 mg comprimate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare comprimat conţine pioglitazonă 15 mg
Anexe PO concurs
 B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
B I B L I O G R A F I E pentru ocuparea funcției de conducere de Șef Serviciu Administrare Procedură Națională din cadrul Departamentului Procedură Națională 1. Hotărârea Guvernului nr. 734/2010 privind
Eucreas, INN-vildagliptin/metformin hydrochloride
 ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Eucreas 50 mg/850 mg comprimate filmate Eucreas 50 mg/1000 mg comprimate filmate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
ANEXA I REZUMATUL CARACTERISTICILOR PRODUSULUI 1 1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Eucreas 50 mg/850 mg comprimate filmate Eucreas 50 mg/1000 mg comprimate filmate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ
PowerPoint Presentation
 PROVOCARILE GESTIONARII DESEURILOR PE PIATA DIN ROMANIA IN CONTEXT EUROPEAN Bucuresti, 3 Iulie 2018 1 Economia circulara RESURSE NATURALE EXPLOATARE UTILIZARE ELIMINARE Sursa: EC 2 Tintele prevazute in
PROVOCARILE GESTIONARII DESEURILOR PE PIATA DIN ROMANIA IN CONTEXT EUROPEAN Bucuresti, 3 Iulie 2018 1 Economia circulara RESURSE NATURALE EXPLOATARE UTILIZARE ELIMINARE Sursa: EC 2 Tintele prevazute in
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE Bine ați venit pe site-ul sondajului online Dedicated
 Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Vă rugăm să selectați limba English STUDIU DE CONFORMITATE PENTRU SUPPLY CHAIN INITIATIVE - 2017 Bine ați venit pe site-ul sondajului online Dedicated. Metodologia bazată pe rețeaua web garantează confidențialitatea
Metodologia privind implementarea raportării sponsorizărilor și a altor cheltuieli, în conformitate cu Legea nr. 95/2006 (art. 814, alineatul 1) și a
 Metodologia privind implementarea raportării sponsorizărilor și a altor cheltuieli, în conformitate cu Legea nr. 95/2006 (art. 814, alineatul 1) și a Codul de Transparență EFPIA, cel din urmă fiind transpus
Metodologia privind implementarea raportării sponsorizărilor și a altor cheltuieli, în conformitate cu Legea nr. 95/2006 (art. 814, alineatul 1) și a Codul de Transparență EFPIA, cel din urmă fiind transpus
Microsoft Word - decizia docx
 1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
1 www.untrr.ro www.e-rovinieta.ro DECIZIE nr. 2 din 4 decembrie 2018 privind modificarea Convenţiei privind regimul de tranzit comun [2018/1988] având în vedere Convenţia din 20 mai 1987 privind regimul
LISTA PROTOCOALELOR TERAPEUTICE APROBATE PRIN ORDINUL MS/CNAS NR 854/562/ iunie 2019 COD DENUMIRE PROTOCOL sublista/cod boala/cod P continuare p
 LISTA PROTOCOALELOR TERAPEUTICE APROBATE PRIN ORDINUL MS/CNAS NR 854/562/2019 - iunie 2019 COD DENUMIRE PROTOCOL sublista/cod boala/cod P continuare prescriere medic familie A008E IMIGLUCERASUM C1-G29
LISTA PROTOCOALELOR TERAPEUTICE APROBATE PRIN ORDINUL MS/CNAS NR 854/562/2019 - iunie 2019 COD DENUMIRE PROTOCOL sublista/cod boala/cod P continuare prescriere medic familie A008E IMIGLUCERASUM C1-G29
AUTORIZARE DE PUNERE PE PIATĂ NR
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5385/2005/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS METFORMIN LPH
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 5385/2005/01-02 Anexa 2 Rezumatul caracteristicilor produsului REZUMATUL CARACTERISTICILOR PRODUSULUI 1. DENUMIREA COMERCIALĂ A PRODUSULUI MEDICAMENTOS METFORMIN LPH
Cuprins Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac
 Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
Abrevieri XIII Cuvânt-înainte XV Capitolul I. Sistemul achiziţiilor publice: concepte definitorii, evoluţie, instituţii implicate, căi de atac 1 1. Aspecte preliminare 1 2. Sediul normativ al materiei
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR /2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofi
 AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
AUTORIZAŢIE DE PUNERE PE PIAŢĂ NR. 8031-8032-8033/2006/01-02 Anexa 1' Prospect PROSPECT: INFORMAŢII PENTRU UTILIZATOR MINIRIN MELT 60 micrograme liofilizat oral MINIRIN MELT 120 micrograme liofilizat oral
csr_romania_ro.doc
 COMISIA EUROPEANĂ Bruxelles, 7.6.2011 SEC(2011) 825 final Recomandare de RECOMANDARE A CONSILIULUI privind Programul național de reformă din 2011 al României și de emitere a unui aviz al Consiliului privind
COMISIA EUROPEANĂ Bruxelles, 7.6.2011 SEC(2011) 825 final Recomandare de RECOMANDARE A CONSILIULUI privind Programul național de reformă din 2011 al României și de emitere a unui aviz al Consiliului privind
Raport de Solvabilitate si Situatia Financiara 2018 al Grupului – Rezumat
 Raport de Solvabilitate si Situatia Financiara 2018 al Grupului Rezumat 2018 Rezumat In continuare este prezentat rezumatul Raportului de Solvabilitate si Situatia Financiara al Grupului ETHNIKI Hellenic
Raport de Solvabilitate si Situatia Financiara 2018 al Grupului Rezumat 2018 Rezumat In continuare este prezentat rezumatul Raportului de Solvabilitate si Situatia Financiara al Grupului ETHNIKI Hellenic
/14:46 ifrom:medic SEF ;To:Maramureş ; ;# 2/ 10 CNA.S Cxsa Naţională de Asigurări de Sănătate CABINET PREŞEDINTE Calea Călăraşilor
 19-01-21/14:46 ifrom:medic SEF ;To:Maramureş ;00372309248 ;# 2/ 10 CNA.S Cxsa Naţională de Asigurări de Sănătate CABINET PREŞEDINTE Calea Călăraşilor nr. 248, Bloc SI9, Sector 3, Bucureşti E-maii: cabinet
19-01-21/14:46 ifrom:medic SEF ;To:Maramureş ;00372309248 ;# 2/ 10 CNA.S Cxsa Naţională de Asigurări de Sănătate CABINET PREŞEDINTE Calea Călăraşilor nr. 248, Bloc SI9, Sector 3, Bucureşti E-maii: cabinet
Sumar executiv
 SISTEM DE MONITORIZARE A POLITICILOR DE CLIMĂ DIN UNIUNEA EUROPEANĂ Sumar Ţările industrializate trebuie să reducă emisiile cu efect de seră cu 80-95% până în anul 2050, pentru a putea crea o economie
SISTEM DE MONITORIZARE A POLITICILOR DE CLIMĂ DIN UNIUNEA EUROPEANĂ Sumar Ţările industrializate trebuie să reducă emisiile cu efect de seră cu 80-95% până în anul 2050, pentru a putea crea o economie
COM(2019)113/F1 - RO
 COMISIA EUROPEANĂ Bruxelles, 28.2.2019 COM(2019) 113 final RAPORT AL COMISIEI CĂTRE PARLAMENTUL EUROPEAN ȘI CONSILIU privind punerea în aplicare a Regulamentului (CE) nr. 450/2003 al Parlamentului European
COMISIA EUROPEANĂ Bruxelles, 28.2.2019 COM(2019) 113 final RAPORT AL COMISIEI CĂTRE PARLAMENTUL EUROPEAN ȘI CONSILIU privind punerea în aplicare a Regulamentului (CE) nr. 450/2003 al Parlamentului European
Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu I. Contul cure
 Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu 15.07.2019 I. Contul curent standard A. SERVICII DE CONT CURENT CONTURI CURENTE
Anexa 2 la Conditiile Generale de Afaceri Lista de dobanzi, taxe si comisioane pentru persoane fizice In vigoare incepand cu 15.07.2019 I. Contul curent standard A. SERVICII DE CONT CURENT CONTURI CURENTE
Ordin MS_163_2015
 Casa Naţională a Asigurărilor de Sănătate - CNAS Ordinul nr. 163/2015 pentru modificarea şi completarea Normelor metodologice privind rambursarea şi recuperarea cheltuielilor reprezentând asistenţa medicală
Casa Naţională a Asigurărilor de Sănătate - CNAS Ordinul nr. 163/2015 pentru modificarea şi completarea Normelor metodologice privind rambursarea şi recuperarea cheltuielilor reprezentând asistenţa medicală
